Oxid chromu: vzorec, vlastnosti a chemické vlastnosti
Mezi různými chemickými prvky a jejich sloučeninami je obtížné vybrat nejužitečnější látku pro lidstvo. Každý je jedinečný ve svých vlastnostech a možnostech aplikace. Technický pokrok značně usnadňuje výzkumný proces, ale pro něj také vytváří nové úkoly. Chemické prvky, objevené před několika staletími a studované ve všech projevech, dostávají v moderním světě technologické využití. Tento trend se týká sloučenin, které existují v přírodě a jsou vytvořeny lidmi.
Oxid
V zemské kůře a v nesrovnatelnosti Vesmíru existuje mnoho chemických sloučenin, které se liší ve třídách, typech, charakteristikách. Jedním z nejběžnějších typů sloučenin je oxid (oxid, oxid). Patří sem písek, voda, oxid uhličitý, to jsou základní látky pro existenci lidstva a celé biosféry Země. Oxidy jsou látky, které obsahují atomy kyslíku oxidační stav -2, zatímco spojení mezi prvky je binární. Výsledkem je jejich vznik chemická reakce, podmínky, které se mění v závislosti na složení oxidu.
Charakteristické znaky této látky jsou tři polohy: látka je složitá, sestává ze dvou atomů, z nichž jeden je kyslík. Množství existujících oxidů je způsobeno skutečností, že mnoho chemických prvků tvoří několik látek. Jsou stejné složení, ale atom, který reaguje s kyslíkem, vykazuje několik stupňů valence. Například oxid chromu (2, 3, 4, 6), dusík (1, 2, 3, 4, 5) atd. Avšak jejich vlastnosti závisí na stupni valence prvku vstupujícího do oxidační reakce.
Podle přijatelné klasifikace jsou oxidy zásadité a kyselé. Také se uvolňuje amfoterní druh, který vykazuje vlastnosti základního oxidu. Oxidy kyselin jsou sloučeniny nekovů nebo prvků s vysokou valencí, jejich hydráty jsou kyseliny. Hlavní oxidy zahrnují všechny látky, které mají vazbu kyslík + kov, jejich hydráty jsou báze.

Chrome
V 18. století objevil chemik I. G. Lehmann neznámý minerál, který se nazýval červený sibiřský olovo. Profesor Pařížské mineralogické školy, Wokelen, provedl řadu chemických reakcí s získaným vzorkem, v důsledku čehož byl izolován neznámý kov. Hlavní vlastnosti, které vědec identifikoval, se stal jeho odolností vůči kyselým prostředím a žáruvzdornosti (tepelná odolnost). Název "chrom" (Chromium) vznikl v důsledku širokého rozsahu barev, který se vyznačuje složením prvku. Kov je spíše inertní, ve své čisté formě se nevyskytuje v přírodních podmínkách.
Hlavní minerály obsahující chrom jsou: chromit (FeCr 2 O 4 ), melanochroit, vocelenit, ditseit, tarapacait. Chemický prvek Cr se nachází v 6. skupině periodického systému DI Mendeleev, má atomové číslo 24. Elektronické uspořádání atomu chromu dovoluje prvku mít valence +2, +3, +6 s nejstabilnějšími sloučeninami trojmocného kovu. Možné reakce, při kterých je stupeň oxidace +1, +5, +4. Chrom není chemicky aktivní, kovový povrch je pokryt filmem (pasivační účinek), který brání reakci s kyslíkem a vodou za normálních podmínek. Oxid chromu, který se vytváří na povrchu, brání tomu, aby kov reagoval s kyselinami a halogeny v nepřítomnosti katalyzátorů. Sloučeniny s jednoduchými látkami (ne kovy) jsou možné při teplotě 300 ° C (chlor, brom, síra).
Při interakci s komplexními látkami jsou vyžadovány další podmínky, například s alkalickým roztokem, reakce nedochází, při jeho taveních je proces velmi pomalý. Chrom reaguje s kyselinami, když je jako katalyzátor vysoká teplota. Oxid chromitý lze získat z různých minerálů vystavením působení teploty. V závislosti na budoucím stupni oxidace prvku se používají koncentrované kyseliny. V tomto případě se míra chromu ve sloučenině pohybuje od +2 do +6 (vyšší oxid chrómu).

Aplikace
Díky jedinečným protikorozním vlastnostem a tepelné odolnosti jsou slitiny na bázi chromu velmi důležité. Současně by jeho podíl nesmí překročit polovinu celkového objemu. Velkou nevýhodou chrómu je jeho křehkost, která snižuje zpracovatelské schopnosti slitin. Nejčastějším způsobem použití kovu je nátěry (chromování). Ochranná fólie může být vrstva 0,005 mm, ale spolehlivě ochrání kovový výrobek před korozí a vnějšími vlivy. Chromové sloučeniny se používají k výrobě tepelně odolných konstrukcí v metalurgickém průmyslu (tavící pece). Protikorozní povlaky dekorativního směru (kovová keramika), speciální legovaná ocel, elektrody pro svařovací stroje, slitiny na bázi křemíku, hliníku jsou na poptávku na světových trzích. Oxid chromu způsobený nízkou možností oxidace a vysokou tepelnou odolností slouží jako katalyzátor mnoha chemických reakcí, k nimž dochází při vysokých teplotách (1000 o C).

Bivalentní sloučeniny
Oxid chromitý (2) CrO (oxid dusný) je prášek jasně červené nebo černé barvy. Je nerozpustný ve vodě, za normálních podmínek neoxiduje, vykazuje výrazné základní vlastnosti. Látka je pevná, žáruvzdorná (1550 o C), není toxická. Při procesu ohřevu na 100 ° C se oxiduje na Cr 2 O 3 . V slabých řešeních dusičnanu a kyselina sírová se nerozpustí, reakce probíhá s kyselinou chlorovodíkovou.

Příjem, aplikace
Tato látka je považována za nižší oxid. Má poměrně úzký rozsah. V chemickém průmyslu se oxid chrómu 2 používá k čištění uhlovodíků z kyslíku, který přitahuje při oxidaci při teplotách nad 100 o C. Existují tři způsoby, jak získat bivalentní oxid chrómu:
- Rozkladem karbonylu Cr (CO) 6 v přítomnosti vysoké teploty jako katalyzátoru.
- Obnova pomocí kyselina fosforečná oxid chrómu 3.
- Chromový amalgam je oxidován kyslíkem nebo kyselinou dusičnou.
Trivalentní sloučeniny

U oxidů chrómu je stupeň oxidace +3 nejstabilnější formou látky. Cr2O3 (chromové zelené, seskvioxid, eskolid) je chemicky inertní, nerozpustný ve vodě, má vysokou teplotu tání (více než 2000 oC). Oxid chromitý 3 - zelený žáruvzdorný prášek, velmi pevné, má amfoterní vlastnosti. Látka je rozpustná v koncentrovaných kyselinách, reakce s alkáliemi vzniká v důsledku fúze. Při interakci se silným redukčním činidlem může být redukován na čistý kov.
Příprava a použití
Vzhledem k vysoké tvrdosti (srovnatelné s korundem) je použití látky v abrazivních a lešticích materiálech nejběžnější. Oxid chromitý (vzorec Cr 2 O 3 ) má zelenou barvu, takže se používá jako pigment při výrobě skla, barvy, keramiky. Pro chemický průmysl se tato látka používá jako katalyzátor reakcí s organickými sloučeninami (syntéza amoniaku). Trivalentní oxid chrómu se používá k výrobě umělých drahých kamenů a spinelů. Získat použité několik typů chemických reakcí:
- Oxidace oxidu chromitého.
- Ohřívací (kalcinační) dichromát nebo chroman amonný.
- Rozklad trojmocného hydroxidu chrómu nebo hexavalentního oxidu.
- Kalcinace chromanů nebo dichromanu rtuťnatého.
Šestimocné sloučeniny
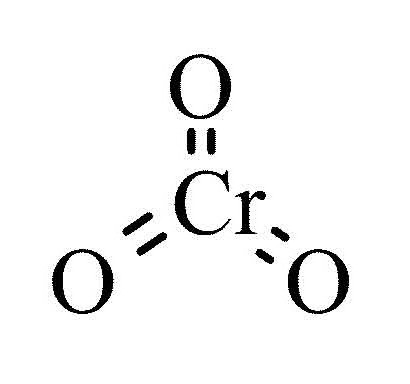
Vzorec pro vyšší oxid chrómu je CrO3. Látka má purpurovou nebo tmavě červenou barvu, může existovat ve formě krystalů, jehel, talířů. Chemicky aktivní, toxické, při interakci s organických sloučenin hrozí nebezpečí spontánního spalování a výbuchu. Oxid chromitý 6 - chromanhydrid, oxid chromitý - je vysoce rozpustný ve vodě, za normálních podmínek interaguje se vzduchem (rozmazáváním), teplota tání je 196 o C. Látka má výrazné kyselé vlastnosti. Když chemická reakce s vodou vytváří dichromid nebo kyselinu chromovou, bez dalších katalyzátorů interaguje s alkalickými látkami (žlutými chromáty). Pro halogeny (jód, síra, fosfor) je silné oxidační činidlo. V důsledku zahřívání nad 250 ° C se vytváří volný kyslík a trojmocný oxid chrómu.

Jak se dostat a kde se používá
Oxid chromitý 6 se získá zpracováním chromanů sodného nebo draselného (dichromáty) koncentrovanou kyselinou sírovou nebo reakcí chromátu stříbrného s kyselinou chlorovodíkovou. Vysoká chemická aktivita látky určuje hlavní směry jejího použití:
- Získání čistého kovu - chrómu.
- Při výrobě chromovaných povrchů včetně elektrolytické metody.
- Oxidace alkoholů (organických sloučenin) v chemickém průmyslu.
- V raketové technice se používá jako zapalovač.
- V chemických laboratořích čistí nádobí z organických sloučenin.
- Používá se v pyrotechnickém průmyslu.