Koloidní roztoky: metody přípravy a použití
Mnoho lidí, kteří se nezajímá o chemii, slyší frázi "koloidní roztoky", představují něco jako gel, viskózní směs. Faktem je, že původně vzniklo toto jméno z řeckého slova, přeložené jako "lepkavé". Když není rovnovážný systém vyvážený, sóly se vysráží a připomínají želé.
Koloidní roztoky jsou zpravidla absolutně transparentní kapalinou. V závislosti na složení může být bezbarvý nebo barevný. Na první pohled se soly neliší od skutečných řešení. Studium tohoto druhu látky probíhá v celé sekci - koloidní chemie.

Obecné charakteristiky
Každé řešení je jednofázový systém obsahující dva nebo více komponent. Naproti tomu suspenze nebo emulze jsou méně stabilní. V kapalných roztocích během skladování může docházet ke srážení, například když jsou umístěny v nepevně uzavřené nádobě a dochází k odpařování kapaliny. V jiných případech je to inertní systém, kde součásti nereagují navzájem, a proto může zůstat nezměněné po dlouhou dobu.
Vlastnosti koloidních roztoků

Molekuly látky jsou rovnoměrně rozloženy v rozpouštědle, ale neustále dělají Brownian (oscilační) pohyb. Výsledkem je úplné míchání komponent systému. Vlastnosti koloidních roztoků v tomto procesu jsou mírně odlišné. Částice takového systému se nazývají micely. Rozkládají se z jedné vrstvy kapaliny na druhou pomaleji (100 krát). Důvodem nízké rychlosti je větší objem micel v porovnání s molekulami pravých roztoků.
V závislosti na velikosti částic se jejich množství, koloidní roztoky liší viskozitou. Často existují systémy, které se dostávají do gelového stavu se sníženou teplotou. Přítomnost příliš velkých micel a překračování limitu rozpustnosti vede k zákalu.
Koloidní částice, na rozdíl od molekul, mají větší rozměry a jsou proto schopny rozptýlit světlo. Takto lze tato řešení rozlišit od těch pravých. Při průchodu takovým systémem bude viditelný paprsek světla.
Micelová struktura
Příprava koloidních roztoků je založena na tvorbě micel, které musí zůstat zachovat vlastnosti systému v stabilním stavu. Částice má složitou strukturu, která se skládá z jádra, které je tvořeno lehce rozpustnou látkou. Jde o vrstvu potenciálně určujících iontů. Obvykle jsou stejné jako u látek s nízkou rozpustností, které se nacházejí ve středu micely (pravidlo Paneth - Faience). Takové ionty určují náboj jádra.
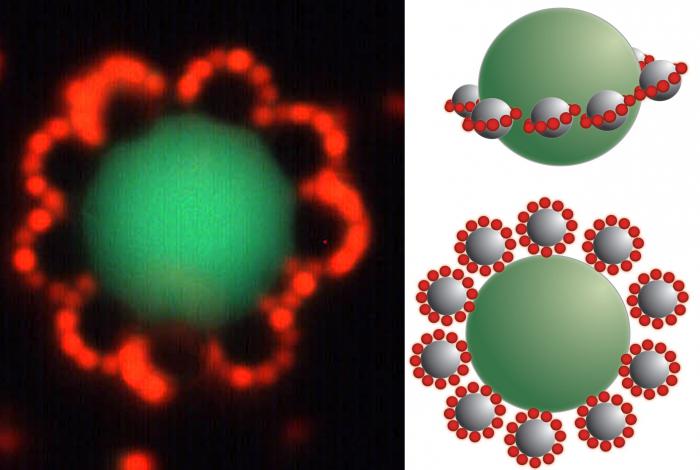
Například při interakci jodidu draselného a dusičnan stříbrný tvoří se micely. Jádrem těchto částic je jodid stříbrný (AgI). Pokud převládá druhá složka, potenciálně určující ionty budou Ag + , pokud první je I - . Další vrstva je protiionty látky, která byla převzata. Formují dvě zóny. První je umístěna blízko povrchu jádra, je součástí adsorbované vrstvy. Druhá část je součástí difuzní vrstvy, sestávající z iontů pohybujících se volně blízko povrchu.
Koloidní částice je jádro s adsorbovanou vrstvou, která obsahuje ionty určující potenciál a protiionty. Tato forma má náboj. Micela obsahuje koloidní částice a difúzní vrstvu protiiontů a je neutrální.
Jak se tvoří micely
Jakékoli způsoby získání koloidních roztoků jsou založeny na interakci špatně rozpustných sloučenin s elektrolytem. Například AgNO 3 (dusičnan stříbrný) s KI (jodid draselný). Výsledkem reakce jsou Agl a KN03 (dusičnan draselný). Struktura micela může být znázorněna schematicky. Existují 2 možnosti tvorby koloidních částic výše uvedených sloučenin:
- S přebytkem AgN03 - {n (Agl) mAg + (mx) NO 3 " xNO 3" .
- S přebytkem KI - {n (AgI) mI (mx) K + } xK + .
Nejprve je indikováno jádro, potom potenciálně určující ionty a protiiony adsorbované a difúzní vrstvy. Elektrokinetický potenciál, který určuje náboj koloidní částice, je označen písmenem "x". Vzniká kvůli rozdílu v povrchové energii jádra částice s potenciálně určujícími ionty.
Stabilita

Koloidní roztoky mohou zůstat nezměněny po dlouhou dobu. Stabilita takových systémů je důsledkem toho, že náboje micela mají stejný název, což vede k jejich odrazení od sebe. Nicméně, s příliš velkými rozměry a vysokou koncentrací, částice se mohou srazit a sloučit. Stabilita koloidních roztoků je relativní koncept. Mohou být uloženy beze změn dostatečně dlouho.
Koagulace koloidních roztoků je proces vzájemného přilepení micel. Se stabilním stavem systému se tento jev objevuje pomalu, což mu umožňuje dlouhodobě trvat (až 100 let) v jednomfázovém stavu. Tento jev se nazývá agregační nestabilita.
Míra koagulace
Rychlost agregace částic a v důsledku toho fázová separace závisí na mnoha faktorech, včetně velikosti a koncentrace micel, při teplotě skladování. Zrychlení procesu koagulace je výsledkem přidání elektrolytu. Tento jev je pozorován v hydrofilních systémech. Známé metody zpomalení procesu agregace částic. Například míchání lipofilního koloidu s hydrofilním. Ztráta stability solí může být ovlivněna zahříváním nebo chlazením, mechanickým namáháním.
Koagulace koloidních roztoků pomocí elektrolytů
Existují určité vzorce vlivu elektrolytů na koloidní roztok. Takže pro zahájení procesu potřebujete určitou koncentraci druhého, nikoli pod určitou úroveň - prahovou koagulaci. Elektrolyt je látka schopná provést elektrického proudu jako výsledek disociace v roztoku nebo roztavení na ionty. Stav koloidního roztoku je ovlivněn iontem, jehož náboj je opačný než náboj micely. Akce je posílena stupněm nabití (Schulze-Gardové pravidlo).
Dalším faktorem, který určuje stupeň iontového vlivu, je jejich hydratace. Částice se stejným nábojem mají odlišnou úroveň působení na koagulační proces. Při separaci koloidního roztoku jsou koagulační ionty přítomny v sedimentech. Při přidávání směsi elektrolytů mohou jeho složky oslabit vzájemný účinek (antagonismus) nebo naopak (synergismus). Zřídka pozorovaný nezávislý (aditivní) účinek.
Způsoby, jak se dostat

Způsoby získání koloidních roztoků jsou sníženy na dvě. Jednou z možností je disperze (broušení) velkých částic na velikosti odpovídající koloidu. Takový proces může být prováděn například pomocí ultrazvukových zařízení (mechanické broušení). Různými disperzními metodami je tvorba koloidních částic v důsledku přidání elektrolytů, které jsou adsorbovány na povrchu koloidních jader a přenesou částice do rozpuštěného stavu.
Opačný k disperzní metodě je metoda kondenzace, která spočívá v agregaci malých částic do větších. Tento jev nastává například při nahrazení rozpouštědla. Jak lze tento efekt dosáhnout? Prudký pokles rozpustnosti způsobený změnami prostředí nastává. Dále látka tvoří koloidní částice. Molekuly rozpouštědla se podílejí na jeho tvorbě, s níž se lépe mísí. Tento účinek se například dosahuje postupným přidáváním kalafuny rozpuštěné v ethanolu do vody.
Různé kondenzační reakce, včetně těch popsaných výše, platí také pro agregační metody. Další příklady mohou být hydrolýza soli kovů, zejména chloridu železitého (FeCl3), neutralizační reakce vzniklé interakcí hydroxidu barnatého (Ba (OH) 2 ) s kyselinou sírovou (H2S04).
Solubilizace
Hodnota koloidních roztoků v lidském životě je velká kvůli schopnosti povrchově aktivních látek zvýšit rozpouštění hydrofobních sloučenin ve vodě. Tento jev se nazývá "solubilizace". Jádro tohoto procesu představuje rozpuštění sloučenin v micelách. Kvůli tomuto jevu jsou prášky schopné odstranit znečištění z tkanin, což vede ke stabilní emulzi uhlovodíků a barviv ve vodě.
Solubilizace může probíhat různými způsoby. Nepolární uhlovodíky tak pronikají do jádra micel, zatímco sloučeniny s hydrofilními a hydrofobními částmi (aminy, alkoholy) jsou zapuštěny tak, že první je venku a druhý jde hluboko do koloidní částice. Existuje také fenomén reverzní solubilizace, který spočívá v rozpouštění vody v olejích. V případě neiontových povrchově aktivních látek je identifikován další způsob zvýšení rozpustnosti hydrofobních sloučenin, který je spojen s povrchem micel prostřednictvím chemických vazeb (zejména vodíku).
Všudypřítomné rozdělení
Koloidní roztoky jsou vždy přítomny uvnitř a kolem osoby. Mezi ně patří krevní, lymfatická, lepidla a barvy často používané v různých stavebních a dokončovacích pracích. Gely jsou získány z koloidních roztoků v důsledku koagulace a srážení. Patří sem například želé, marmeláda, agar-agar, želatina, karagenan. Ty se používají ke zlepšení struktury produktů, zejména past. V lidském těle jsou všude koloidní roztoky obohacené bílkovinami.
Použití v lékařství

V lékařství se používají koloidní roztoky všude. Zde jsou některé příklady jejich použití. Koloidní stříbro, které je malé kovové částice rozptýlené ve vodě, se používá při léčení popálení, žaludeční vředy a dvanáctníku, pro promytí nosní sliznice, aby se zabránilo šíření virových infekcí.
Farmaceutický průmysl nabízí velký výběr koloidních roztoků pro různé účely. Mezi nimi jsou univerzální léky, které lze použít jako hojení ran pro popáleniny, hemoroidy; protizánětlivá - se studeným, bolavým hrdlem, sinusitidou; analgetika - pro zmírnění bolesti zubů a nejenom. Mezi ně patří koloidní roztok Milénia. Gel obsahuje aloe, pšeničný protein, ženšen, vitamín E a další užitečné doplňky. Mnoho farmaceutických přípravků pro vnější použití je ve skutečnosti koloidním roztokem. U kloubů se používá například Artro Complex, který obsahuje takový užitečný prvek jako žraločí chrupavka.
Aplikace v životě a průmyslu
Koloidní roztoky tvoří základ pro praní a čištění povrchově aktivních látek. Kontaminanty pronikají do micel a jsou tak odstraněny z povrchu.
Dalším důležitým aspektem použití povrchově aktivních činidel vytvářejících micely je výroba polymerů, zejména latexů, polyvinylalkoholu a lepidla rostlinného původu. Různé plasty, kožené náhražky jsou založeny na emulzi. Povrchově aktivní látky se také používají při čištění kanalizace a pitné vody.
Výhodou kosmetiky na bázi koloidních roztoků je penetrace aktivních látek lidskou kůží a strukturou vlasů. Takové prostředky se účinně používají proti stárnutí. Jedná se zejména o Millennium Neo gel. Koloidní roztok pomáhá složkám, které jsou v něm obsaženy, aby dosáhly hlubších vrstev pokožky a obcházejí epidermis.