Diethylether: vzorec. Diethylether: fyzikální a chemické vlastnosti
Před sto lety, slavný vědec té doby, Lully, který po jeho smrti byl nazván alchymistou, dokázal objevit nezbytný diethylether. Vzorec, vlastnosti, bod varu, metody získání látek budou podrobně popsány v tomto článku. 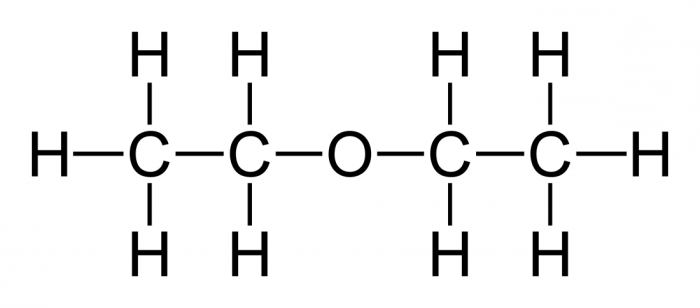
Dějiny
Ve 13. století objevil známý španělský vědec Raymond Llull diethylether. Jeho vlastnosti byly popsány v roce 1540 ne méně známým vědcem Paracelsusem. V roce 1846 se nejdříve pokusil použít éter jako anestezii. Operace vedená americkým doktorem D. Warrenem s použitím této látky byla úspěšná. Vynálezci anestezie jsou považováni za zubaře W. Mortona a jeho mentora - lékaře a chemik C. Jackson.
Metody získávání éteru v 16. století popsal Valerius Cordus, známý botanik a farmaceut původně z Kasselu. Od počátku 18. století byla směs alkoholu a etheru použita jako sedativa - to byl návrh Friedricha Hoffmanna. Petersburgský lékárník Thomas Lovits v roce 1796 obdržel čistý diethylether, jehož vzorec má mimo jiné dvě možnosti (více o tom později). Zásada působení výše zmíněné substance na lidské tělo byla oznámena anglickým fyzikem M. Faradayem, poté v roce 1818 byl publikován i vědecký článek věnovaný tomuto tématu. 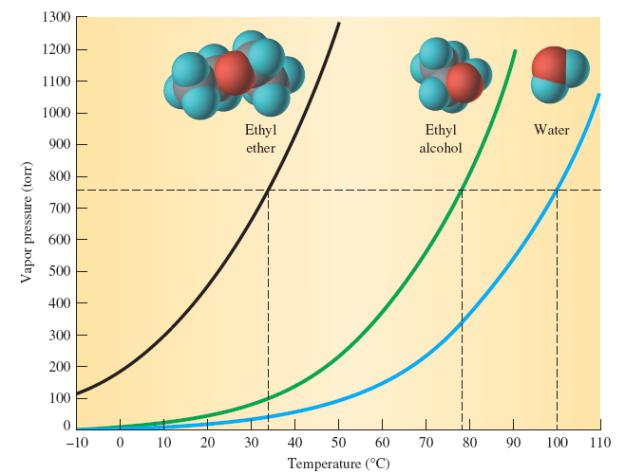
Charakteristický
Co se nazývá jednoduchý éter? To je organické sloučeniny jejichž molekuly se skládají ze dvou uhlovodíkových radikálů a atomu kyslíku. Nejdůležitější jednoduchý, diethylether, jehož vzorec má následující podobu:
(C2H5) 2O nebo C4H10O.
Jedná se o bezbarvou, průhlednou, velmi pohyblivou těkavou kapalinu se zvláštní vůní a pálící chutí.
Pod vlivem světla, vzduchu, tepla a vlhkosti se éter rozkládá, tvoří toxické aldehydy, peroxidy a ketony, které dráždí dýchací cesty.
Když je teplota vody 20 stupňů rozpuštěna o 6,5%. Dobře se mísí s mastnými a éterickými oleji, benzenem a alkoholem, bez ohledu na poměr.
Samotný ether, stejně jako jeho výpary, je snadno hořlavý. V určité míře s kyslíkem nebo vzduchem jsou pary diethyletheru používané pro anestezii výbušné. 
Chemické vlastnosti
Všechny chemické vlastnosti etherů jsou charakteristické pro diethylether. Takže se podrobněji zabývejme touto problematikou. Je to spíše inertní látka. Hlavní rozdíl od esterů je absence hydrolýzy, i když existují výjimky. Při nachlazení neovlivňuje chlorid fosforitý, kovový sodík a mnoho zředěných minerálních kyselin. Navzdory tomu se soustředil kyseliny (sírové) a jodid vodíku) rozkládají tyto estery dokonce i při nízkých teplotách a vyhřívaný kovový sodík je rozděluje.
Eter s dvojitými elektronovými páry interaguje s protonem silná kyselina což vede k nestabilní sloučenině oxonia:
- Acidolýza. Kyseliny sírové a jodovodíkové, stejně jako FeCl3 v acetanhydridu, jsou schopny štěpit ethery. Chemická reakce je následující: CH3-CH2-0-CH2-CH3 + HJ-CH3-CH2-OH + J-CH2-CH3.
- Reakce metalace, nazvaná reakce Shorygin. Vyhřívaný kovový sodík rozděluje diethylether: C2H5-O-C2H5 + 2Na → C2H5ONa + C2H5Na
- Relativní chemická inertnost nebrání tvorbě esterů ve vzduchu vytvářet peroxidy, což často vede k výbuchu na konci destilace.
Diethylether: fyzikální vlastnosti
Zvláštní zápach, nízká teplota varu etherů - důkaz slabých intermolekulárních účinků, což naznačuje nízkou polaritu a absenci předpokladů pro tvorbu vodíkových vazeb. Na rozdíl od alkoholů mají estery silnější elektronové vlastnosti, což je potvrzeno hodnotou ionizačních potenciálů. Zvýšení těchto vlastností je spojeno s pozitivním indukčním účinkem skupiny atomů, které jsou získány z alkanů, když je odstraněn atom vodíku. 
Bod varu diethyletheru je 35,6 stupňů Celsia (je mnohem nižší než teplota izomerních alkoholů) a zmrazení je 117 ° C. Étery se téměř nemísí s vodou. Vysvětlení je poměrně jednoduché: nemohou vytvářet vodíkové vazby, protože jejich molekuly nemají polární vazby. Špatně rozpustný ve vodě a diethyletheru, jehož hustota vzhledem k oxidům vodíku je 0,714. Jedním z rysů dotyčné látky je sklon k elektrifikaci. Pravděpodobnost statického výboje je obzvláště vysoká při transfuzi nebo vypouštění chemického složení, což může mít za následek vznícení. Páry éteru tvoří se vzduchem, což je 2,5 krát lehčí, výbušné směsi. Nižší mez výbušnosti je 1,7% a horní 49%. Při práci s éterem bychom neměli zapomínat na to, že jeho páry mají tendenci se šířit na dlouhé vzdálenosti, aniž by ztratily schopnost hořet. Hlavní preventivní opatření je tedy absence otevřeného plamene a jiných zdrojů vznícení.
Eter je nízká účinná látka, méně reaktivní než alkoholy. Pozoruhodně rozpouští většinu organické hmoty, takže se používá jako rozpouštědlo. Výjimkou není dietyléter. Fyzikální vlastnosti, stejně jako chemické vlastnosti, umožňují jeho použití v lékařství av průmyslu.
Získá se diethylether
Etery se nevyskytují v přírodě - jsou získávány synteticky. Pod vlivem kyselých katalyzátorů ethylalkoholu při zvýšené teplotě se získá diethylether (výše uvedený vzorec). Nejjednodušší způsob získání této látky je destilací směsi obsahující kyselinu sírovou a alkohol. K tomu je třeba zahřát na 140-150 stupňů Celsia. Budeme potřebovat ethylalkohol a kyselinu sírovou (ve stejných poměrech), pipety, zkumavky a parní trubky.
Po přípravě zařízení a reagencií můžete experiment spustit. Ve zkumavce (musí být suché) nalijte 2-3 ml směsi alkoholu a kyseliny a pomalu ho zahřejte. Jakmile začne varu, hořák se odstraní a do horké směsi se přidá 5 až 10 kapek ethylalkoholu pipetou podél stěny zkumavky. Reakce probíhá následovně:
- CH3-CH2-OH (kyselina ethylsírová) + H2SO4CH3-CH2-OS03H + H20;
- CH3-CH2-OS03H + CH3-CH3-0;
- CH3-CH2-O-CH2-CH3 (diethylether) + H2S04.
Tvorba diethyletheru je doložena vůní, která se objevila. 
Použití v lékařství
Lékaři používají jako obecné anestetikum diethylether. Vlastnosti této látky neumožňují použití v elektrických nástrojích, jelikož jsou hořlavé a při kombinování se vzduchem mohou explodovat. Dietyléter je široce distribuován v chirurgii, kde se používá k inhalační anestezii. Ve stomatologii jsou ošetřovány zubními kořenovými kanály a karyózními místy, čímž připravují ústní dutinu pro plnění. 
Diethylether jako palivo
Látka má vysoké cetánové číslo (85-96), takže může být použita jako výchozí kapalina pro benzínové a naftové motory. Vzhledem k vysoké variabilitě a nízkým bodům vzplanutí se jako součást palivové směsi používá jako příklad dieselových motorů diethylether. Ukazuje se, že tato látka je podobná ethanolu.
Správné ukládání
Diethylether se doporučuje skladovat v tmavě zbarvených lahvích (pečlivě utěsněných) na chladném místě, protože se rozkládá ve světle, v teple a pod vlivem vlhkosti, což vede k toxickým látkám.