Fyzikálně-chemické vlastnosti toluenu, reakční rovnice
Toluen je methylbenzen, což je bezbarvá kapalina patřící do třídy arén, které jsou organických sloučenin s aromatickým systémem ve složení.
Klíčovou vlastností této látky lze považovat za její specifický zápach. To však není jediný "rozlišovací znak" látky. Toluen má mnoho vlastností a vlastností a všechny by měly být stručně popsány.

Trochu historie
Chemické vlastnosti toluenu se začaly studovat o něco dříve než před 200 lety, kdy byly poprvé získány. Tato látka byla objevena v roce 1835 francouzským lékárníkem a chemikem Pierre Joseph Pelletier. Vědec získal toluen během destilace borovicové pryskyřice.
O tři roky později francouzský fyzikál chemik Henri St. Clair Deville tuto látku izoloval z balzámu, který přivezl z kolumbijského města Tolu. Na počest tohoto nápoje, ve skutečnosti, spojení a dostal jeho jméno.
Obecné informace
A co vlastnosti a chemické vlastnosti toluenu? Látka je těkavá pohyblivá kapalina se silným zápachem. Má mírný narkotický účinek. Reaguje s neomezeným množstvím uhlovodíků, reaguje s étery a estery s alkoholy. Nesmí se mísit s vodou.
Vlastnosti jsou následující:
- Látka je označena vzorcem C7H8.
- Jeho molární hmotnost je 92,14 g / mol.
- Hustota je 0,86694 g / cm3.
- Teploty tání a varu jsou -95 a 110,6.
- Specifické odpařování je 364 kJ / kg.
- Kritická fázová fáze přechodu je 320 ° C.
Tato látka je také hořlavá. Spálil s kouřovým plamenem.
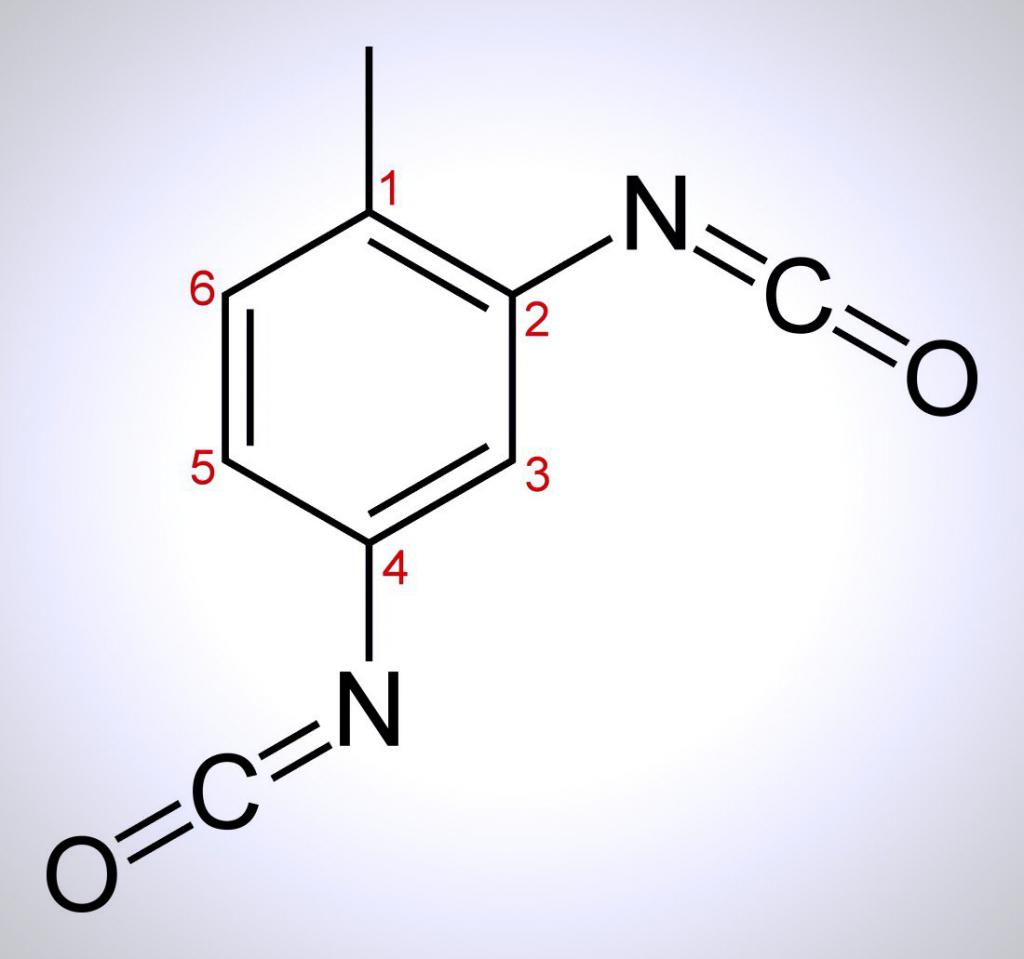
Základní chemické vlastnosti
Toluen je látka, která je charakterizována elektrofilními substitučními reakcemi. Vyskytují se v takzvaném aromatickém kruhu, který vykazuje abnormálně vysokou stabilitu. Tyto reakce probíhají hlavně v pozicích para a orto v poměru k methylové skupině -CH3.
Viz chemické vlastnosti toluenu, reakce ozonolýzy a adice (hydrogenace). Pod vlivem určitých oxidačních činidel se methylová skupina stává karboxylovou skupinou. Pro tento účel se nejčastěji používá alkalický roztok manganistanu draselného nebo nekoncentrovaného roztoku. kyselina dusičná.
Je také třeba poznamenat, že toluen se může spontánně vznítit. To vyžaduje teplotu 535 ° C. Blesky se vyskytují při teplotě 4 ° C.

Tvorba kyseliny benzoové
Schopnost látky, o níž se diskutuje, se účastní tohoto procesu také kvůli jeho chemickým vlastnostem. Toluen, reagující se silnými oxidačními činidly, tvoří nejjednodušší monobázickou benzoovou karboxylovou kyselinu patřící do aromatické řady. Její vzorec je C6H5COOH.
Kyselina má formu bílých krystalů, které se dobře rozpouštějí v diethyletheru, chloroformu a ethanolu. Získává se následujícími reakcemi:
- Toluen a manganistan draselný, interagující v kyselém prostředí. Vzorec je následující: 5C 6H 5CH 3 + 6KMnO 4 + 9H 2SO 4 → 5C 6H 5 COOH + 6MnSO 4 + 3K 2 SO 4 + 14H 2 O.
- Toluen a manganistan draselný, které interagují v neutrálním prostředí. Vzorec je následující: C 6 H 5 CH 3 + 2 KMnO 4 → C 6 H 5 COOK + 2MnO 2 + KOH + H 2 O.
- Toluen, interagující ve světle s halogeny, energetické oxidační činidla. Vyvolává se podle vzorce: C 6 H 5 CH 3 + X 2 → C 6 H 5 CH 2 X + HX.
Kyselina benzoová, získaná v důsledku těchto reakcí, se používá v mnoha oblastech. V zásadě se používá k získání reakčních činidel - benzoylchloridu, benzoátových plastifikátorů, fenolu.
Používá se také při konzervování. Přísady E213, E212, E211 a E210 se vyrábějí na bázi kyseliny benzoové. Blokuje enzymy a zpomaluje metabolismus, zabraňuje růstu kvasinek, plísní a bakterií.
A kyselina benzoová se používá v medicíně pro léčení kožních onemocnění a jako expektorant.

Příjem látky
Reakční rovnice, které demonstrují výše uvedené chemické vlastnosti toluenu, nejsou všechny, které bych chtěl vzít v úvahu. Je důležité mluvit o procesu získávání této látky.
Toluen je produkt průmyslového zpracování benzínových frakcí ropy. Toto se také nazývá katalytické reformování. Látka se izoluje selektivní extrakcí, po níž se destilace provádí - směs se oddělí protiproudým teplem a přenosem hmoty mezi kapalinou a párou.
Tento proces je často nahrazen katalytickou dehydrogenací heptanu. Jedná se o organický alkan vzorce CH3 (CH2) 5CH3. Dehydrogenace probíhá prostřednictvím methylcyklohexan-cykloalkanu vzorce C7H14. Jedná se o monocyklický uhlovodík, jehož methylová skupina má jeden substituovaný atom vodíku.
Čistěte toluen stejným způsobem jako benzen. To je pouze v případě, že je použito kyselina sírová je třeba vzít v úvahu - tato látka je sulfurizována snadněji. To znamená, že při čištění toluenu je nutné udržovat nižší teplotu. Nižší než 30 ° C, přesně.

Toluen a benzen
Vzhledem k tomu, že tyto dvě látky jsou podobné, je vhodné provést srovnání chemických vlastností. Benzen a toluen podstupují substituční reakce. Jejich průtoky jsou však odlišné. Vzhledem k tomu, že methylová skupina v molekule toluenu ovlivňuje aromatický kruh, reaguje rychleji.
Avšak benzen vykazuje odolnost proti oxidaci. Takže například, když to ovlivňuje manganistan draselný, nic se nestane. Ale toluen v této reakci vytváří kyselinu benzoovou, jak již bylo dříve uvedeno.
Současně je známo, že nasycené uhlovodíky nereagují s roztokem manganistanu draselného. Takže oxidace toluenu je způsobena účinkem benzenového kruhu na methylovou skupinu. Toto tvrzení je potvrzeno teorií Butlerova. V souladu s tím mají atomy a jejich skupiny v molekulách vzájemný vliv.
Friedel-Craftsova reakce
Hodně bylo řečeno o formulaci a chemických vlastnostech toluenu. Ale ještě nebylo uvedeno, že tato látka je zcela možné získat z benzenu, pokud provedete Friedel-Craftsovu reakci. Tímto způsobem se provádí acylace a alkylace aromatických sloučenin za použití kyselých katalyzátorů. Patří k nim fluorid boritý (BF 3 ), chlorid zinečnatý (ZnCl2), hliník (AICI3) a železo (FeCl3).
To je jen v případě toluenu, můžete použít pouze jeden katalyzátor. A to je bromid železa, což je komplexní binární sloučenina anorganické povahy s receptorem FeBr 3 . Reakce je následující: C6H6 + CH3Br FeBr3C6H5CH3 + HBr. Tak se kombinují nejen chemické vlastnosti benzenu a toluenu, ale i schopnost získat jednu látku od druhého.

Nebezpečí požáru
Nemluvě o tom o chemických a fyzikálních vlastnostech toluenu. Koneckonců je to velmi hořlavá látka.
Patří do třídy 3.1 hořlavých kapalin. Do této kategorie patří motorová nafta, plynový olej a znecitlivěné výbušniny.
Nedovolte, aby se v blízkosti toluenu objevily otevřené plameny, jiskry nebo kouř. Dokonce i směs výparů této látky se vzduchem je výbušná. Pokud jsou prováděny odvodňovací operace, je zásadní význam dodržování pravidel ochrany proti statické elektřině.
Výrobní zařízení určená pro práci s toluenem jsou vybavena napájecí a odsávací ventilací a zařízeními s odsáváním. Zakázáno použití nástrojů, které mohou vyvolat jiskru. Pokud se látka zapálí, měla by být uhasena pouze vodní mlhou, vzduchem mechanickou nebo chemickou pěnou. Rozlitý toluen se neutralizuje pískem.
Nebezpečí pro člověka
Vlastnosti a chemické vlastnosti toluenu určují jeho toxicitu. Jak již bylo zmíněno, jeho páry mají narkotický účinek. Je zvláště silný ve zvýšených koncentracích. Osoba, která má inhalační výpary, má silné halucinace. Jen málo lidí ví, ale do roku 1998 tato látka byla součástí lepidla Moment. Proto byl mezi závislými tak populární.
Vysoké koncentrace této látky také negativně ovlivňují nervový systém, sliznice očí a kůži. Funkce tvorby krve je narušena, protože toluen je vysoce toxický jed. Z tohoto důvodu mohou nastat choroby, jako je hypoxie a cyanóza.
Existuje i pojem toluenová toxikomanie. Má karcinogenní účinek. Koneckonců, pár, který se dostává přes kůži nebo dýchací orgány do lidského těla, ovlivňuje nervový systém. Někdy tyto procesy nelze obrátit.
Kromě toho mohou páry způsobit letargii a narušit funkci vestibulárního aparátu. Proto lidé, kteří pracují s touto látkou, pracují v dobře větraných prostorách, vždy pod napětím a používají speciální gumové rukavice.

Aplikace
K dokončení tématu fyzikálně-chemických vlastností toluenu je třeba zvážit oblasti, v nichž se tato látka aktivně účastní.
Používá se hlavně jako surovina pro výrobu nitrotoluenů, benzylchloridu, kyseliny benzoové a dalších organické látky.
Tato sloučenina je také účinným rozpouštědlem pro mnoho polymerů (amorfní krystalické látky s vysokou molekulovou hmotností). A to je často přidáno do složení komerčních rozpouštědel pro barvy a laky, některé léky. Dokonce i při výrobě výbušnin je tato sloučenina použitelná. Trinitrotoluen a trotiltol se vyrábějí s jeho přidáním.