Funkce a struktura proteinu
Proteiny jsou organické vysokomolekulární sloučeniny. Tyto látky se také nazývají proteiny, polypeptidy. Dále zvažte strukturu a funkci proteinů.
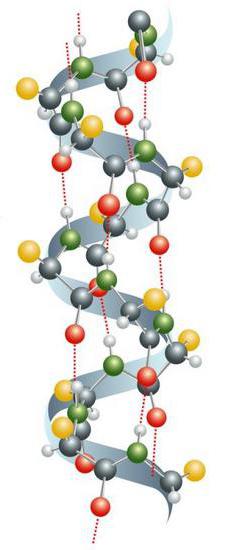
Obecné informace
Chemická struktura proteinů je reprezentována alfa-aminokyselinami spojenými v řetězci přes peptidovou vazbu. V živých organizmech kompozice určuje genetický kód. Při syntéze se ve většině případů používá 20 standardních aminokyselin. Mnoho z jejich kombinací tvoří molekuly proteinů se širokou škálou vlastností. Aminokyselinové zbytky jsou často podrobeny posttranslačním modifikacím. Mohou se vyskytnout dříve, než protein začne plnit své funkce a v průběhu své aktivity v buňce. V živých organismech často tvoří několik molekul komplexní komplexy. Příkladem je fotosyntetická asociace.
Přiřazení připojení
Bílkoviny jsou považovány za důležitou složku výživy lidí a zvířat kvůli tomu, že ve svých organismech nelze všechny nezbytné aminokyseliny syntetizovat. Někteří z nich by měli přijít spolu bílkovinné potraviny. Hlavními zdroji sloučenin jsou maso, ořechy, mléko, ryby, obiloviny. V menší míře jsou proteiny přítomny v zelenině, houbách a bobulích. Během trávení enzymy se spotřebované bílkoviny zničí na aminokyseliny. Jsou již používány v biosyntéze vlastních bílkovin v těle nebo procházejí dalšími rozpady - pro energii.
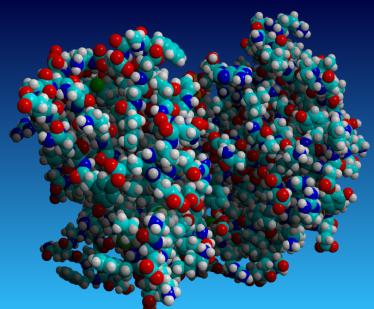
Historické pozadí
Sekvence struktury inzulinového proteinu byla poprvé stanovena Frederiem Sengerem. Za svou práci získal Nobelovu cenu v roce 1958. Sanger použil metodu sekvenování. Použití difrakce rentgenové záření následně byly získány trojrozměrné struktury myoglobinu a hemoglobinu (koncem padesátých let). Práce provedly John Kendrew a Max Perutz.
Struktura molekulové bílkoviny
Obsahuje lineární polymery. Na druhé straně se skládají z alfa-aminokyselinových zbytků, které jsou monomery. Navíc proteinová struktura může zahrnovat složky mající neaminokyselinovou povahu a aminokyselinové zbytky modifikovaného typu. Při označování použitých složek používaly 1 nebo 3 písmena zkratky. Sloučenina, která obsahuje od dvou do několika desítek zbytků, se často označuje jako "polypeptid". V důsledku interakce alfa-karboxylové skupiny jedné aminokyseliny s alfa-aminoskupinou druhé se objevují vazby (během tvorby struktury proteinu). Ve sloučenině jsou izolovány C- a N-konce, v závislosti na tom, která skupina aminokyselinových zbytků je volná: -COOH nebo -NH2. Probíhá syntézy proteinů na ribozómu jako první terminál zpravidla působí metioninový zbytek; příchod dalšího se provádí na konci C předchozích.
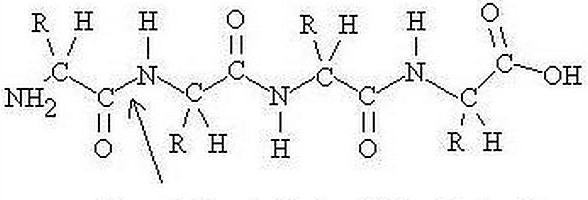
Úrovně organizace
Byly jim nabídnuty Lindrem-Lang. Přestože je tato divize poněkud zastaralá, stále se používá. Bylo navrženo rozlišit čtyři úrovně organizace připojení. Primární struktura molekuly proteinu je určena genetickým kódem a charakteristikami genu. Pro vyšší úrovně je charakteristická tvorba při skládání proteinů. Prostorová struktura proteinu je určena v celém řetězci aminokyselin. Nicméně je poměrně labilní. To může být ovlivněno vnějšími faktory. V tomto ohledu je správnější mluvit o konformaci sloučeniny, nejvýhodnější a nejvýhodnější energii.
Úroveň 1
Je reprezentován sekvencí aminokyselinových zbytků polypeptidového řetězce. Zpravidla se popisuje pomocí jedno- nebo třípísmenných označení. Primární struktura proteinů je charakterizována stabilními kombinacemi aminokyselinových zbytků. Vykonávají určité úkoly. Takové "konzervativní motivy" zůstávají zachovány v průběhu evoluce druhů. Podle nich docela často můžete předpovědět problém s neznámým proteinem. Posouzením stupně podobnosti (homologie) aminokyselinových řetězců různých organismů je možné určit evoluční vzdálenost vytvořenou mezi taxony, které tvoří tyto organismy. Primární struktura proteinů se určuje sekvenováním nebo počátečním komplexem jeho mRNA pomocí tabulky genetického kódu.
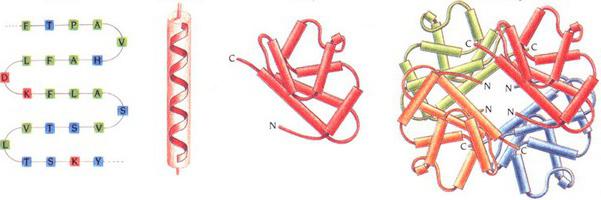
Místní uspořádání řetězu
Toto je další úroveň organizace - sekundární struktura bílkovin. Existuje několik typů. Místní uspořádání místa řetězce polypeptidu je stabilizováno vodíkovými vazbami. Nejoblíbenější typy jsou:
- Alfa helix Jsou prezentovány ve formě hustých cívek kolem dlouhé molekulární osy. Jeden z nich je tvořen 3,6 aminokyselinovými zbytky. Stoupání šroubovice je 0,54 nm. Tato sekundární proteinová struktura je stabilizována interakcemi H- a O-peptidových skupin, které jsou 4 jednotky za sebou. Alfa šroubovice může být levou rukou nebo pravou rukou. Posledně jmenovaná je však nejčastěji detekována v proteinových sloučeninách. Elektrostatické interakce argininu, lysinu, kyseliny glutamové. V bezprostředním okolí mohou zbytky leucinu, threoninu, serinu a asparaginu způsobit sterickou interferenci s tvorbou. Porušení alfa-šroubovice (jeho ohyb) je způsobeno částmi prolinu.
- Seznamy beta. Jsou prezentovány ve formě několika zigzag polypeptidových řetězců. V nich jsou vodíkové vazby tvořeny mezi aminokyselinami, relativně vzdálenými v primární struktuře nebo různými řetězci proteinů. Spojení jsou obvykle orientovány N-konce v opačném směru (antiparalelní orientace). Při vytváření seznamů beta je důležitá malá velikost bočních skupin aminokyselin.
- Neurčené fragmenty.
- 310- a π - šroubovice a další.

Prostorová struktura
Terciární struktura proteinů obsahuje prvky předchozí úrovně. Jsou stabilizovány různými typy interakcí. Nejdůležitější jsou hydrofobní vazby. Při stabilizaci se jedná:
- Kovalentní interakce.
- Ionické vazby, které se vytvářejí mezi skupinami aminokyselin, které mají opačné náboje.
- Vodíkové interakce.
- Hydrofobní vazby. V procesu interakce s okolními prvky H2O dochází k skládání proteinů tak, že boční nepolární aminokyselinové skupiny jsou izolovány z vodného roztoku. Na povrchu molekuly se objevují hydrofilní skupiny (polární).
Terciární struktura proteinů je určována magnetickými (nukleárními) rezonančními metodami, některými typy mikroskopie a dalšími metodami.
Princip pokládky
Studie ukázaly, že mezi 2 a 3 úrovněmi je vhodné přidělit další. Nazývá se "architektura", "styl styl". Je určena relativní pozicí složek sekundární struktury (beta vlákna a alfa helixy) uvnitř hranic kompaktního globule, proteinové domény. Může existovat nezávisle nebo může být součástí složení většího proteinu spolu s jinými podobnými. Je zjištěno, že stylingové motivy jsou poměrně konzervativní. Nacházejí se v proteinech, které nemají ani evoluční ani funkční vazby. Definice architektury je základem racionální (fyzické) klasifikace.
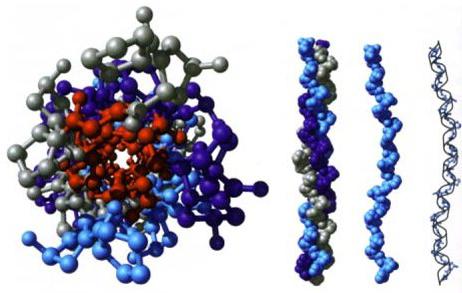
Organizace domén
Při vzájemném uspořádání několika polypeptidových řetězců v rámci jediného komplexu proteinu se vytvoří kvartérní proteinová struktura. Prvky obsažené v jeho složení jsou vytvořeny samostatně na ribozómech. Pouze na konci syntézy se začne vytvářet tato proteinová struktura. Může obsahovat jak odlišné, tak identické polypeptidové řetězce. Kvarterní struktura proteinů je stabilizována kvůli stejným interakcím jako na předchozí úrovni. Některé komplexy mohou obsahovat několik desítek proteinů.
Proteinová struktura: obranné cíle
Polypeptidy cytoskeletu, působící nějakým způsobem jako armatura, poskytují tvar mnoha organoidům, se podílejí na jeho změně. Strukturní proteiny poskytují ochranu tělu. Tento protein je například kolagen. Tvoří základ intercelulární substance spojivových tkání. Keratin má také ochrannou funkci. To tvoří základ rohů, peří, vlasů a dalších derivátů pokožky. Když se protein v mnoha případech váže na toxiny, dochází k jeho detoxikaci. To je úkol chemické obrany těla. Zvláště důležitou roli v procesu neutralizace toxinů v lidském těle hrají jaterní enzymy. Jsou schopny rozdělit jedy nebo je převést do rozpustné formy. To přispívá k rychlejšímu transportu z těla. Proteiny přítomné v krvi a jiných biologických tekutinách poskytují imunitní ochranu a způsobují reakci jak na napadení patogenů, tak na poškození. Imunoglobuliny (protilátky a složky komplementového systému) jsou schopné neutralizovat bakterie, cizí proteiny a viry.
Mechanismus regulace
Proteinové molekuly, které nepůsobí jako zdroj energie nebo jako stavební materiál, kontrolují mnoho intracelulárních procesů. Takže kvůli nim se provádí regulace translace, transkripce, krájení, aktivity jiných polypeptidů. Mechanismus regulace je založen na enzymatické aktivitě nebo se projevuje díky specifické vazbě na jiné molekuly. Například transkripční faktory, aktivátorové polypeptidy a represorové proteiny jsou schopné kontrolovat intenzitu transkripce genu. Zároveň interagují s regulačními sekvencemi genů. Nejdůležitější úlohu při řízení průběhu intracelulárních procesů je přiřazena proteinovým fosfatázám a proteinovým kinázám. Tyto enzymy spouštějí nebo inhibují aktivitu jiných proteinů přidáním nebo štěpením fosfátových skupin z nich.
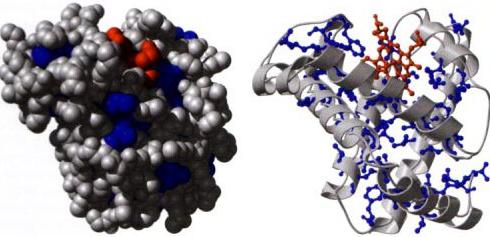
Signalizační úkol
Často se kombinuje s regulační funkcí. To je způsobeno skutečností, že mnoho intracelulárních, stejně jako extracelulárních polypeptidů může přenášet signály. Růstové faktory, cytokiny, hormony a další sloučeniny mají tuto schopnost. Steroidy jsou transportovány krví. Hormonální interakce s receptory působí jako signál, kvůli němuž je vyvolána reakce buňky. Steroidy kontrolují obsah sloučenin v krvi a buňkách, reprodukci, růst a další procesy. Příkladem je inzulin. Reguluje hladinu glukózy. Interakce buněk se provádí pomocí signálních proteinových sloučenin přenášených přes mezibuněčnou látku.
Přeprava prvků
Rozpustné proteiny podílející se na pohybu malých molekul mají vysokou afinitu k substrátu přítomnému ve zvýšených koncentracích. Mají také schopnost snadno uvolnit v oblastech s nízkým obsahem. Příkladem je transportní protein hemoglobin. Přesune kyslík z plic do jiných tkání a od nich - přenosy oxid uhličitý. Některé membránové proteiny se také podílejí na transportu malých molekul přes buněčné stěny a mění je. Cytoplazmatická lipidová vrstva je odolná vůči vodě. To zabraňuje difuzi nabitých nebo polárních molekul. Membránové dopravní spojení lze rozdělit na nosiče a kanály.
Redundantní připojení
Tyto proteiny tvoří tzv. Rezervy. Kumulují se například v semenech rostlin, vejcích zvířat. Tyto proteiny fungují jako záložní zdroj hmoty a energie. Některé sloučeniny jsou tělem používány jako zásobník aminokyselin. Na druhé straně jsou prekurzory účinných látek, které se podílejí na regulaci metabolismu.
Buněčné receptory
Takové proteiny mohou být umístěny buď přímo v cytoplazmě nebo uloženy ve stěně. Jedna část připojení přijímá signál. Obvykle se jedná obvykle o chemickou látku a v některých případech o mechanické působení (např. Protahování), o světlo a jiné podněty. Při procesu vystavení signálu určitému fragmentu molekuly - receptoru polypeptidu - začíná jeho konformační změny. Vyvolávají změnu konformace zbytku, která přenáší podnět k ostatním složkám buňky. Odesílání signálu lze provádět různými způsoby. Některé receptory jsou schopné katalyzovat chemickou reakci, zatímco druhé působí jako uzavření nebo otevření iontových kanálů pod vlivem podnětu. Některé sloučeniny se specificky vážou zprostředkováním molekul v buňce.
Motorové polypeptidy
Existuje celá řada proteinů, které zajišťují pohyb těla. Motorické proteiny se podílejí na svalové kontrakci, pohybu buněk, aktivitě flagelly a řas. Díky tomu je také prováděn směrový a aktivní transport. Kinesiny a dyneiny přenášejí molekuly podél mikrotubulů za použití ATP jako zdroje energie hydrolýzy. Druhá skupina pohybuje organoidy a další prvky směrem k centrosomu z míst periferních buněk. Kinesiny se pohybují v opačném směru. Dyneiny jsou navíc zodpovědné za činnost flagelly a řas.