Arenas: chemické vlastnosti a způsoby výroby
Aromatické chemické sloučeniny nebo arény jsou velká skupina karbocyklických sloučenin, jejichž molekuly obsahují stabilní cyklus šesti atomů uhlíku. Je nazýván "benzenovým kruhem" a způsobuje zvláštní fyzické a chemické vlastnosti arény.
Benzen a jeho různé homology a deriváty jsou primárně příbuzné aromatickým uhlovodíkům.
Molekuly arény mohou obsahovat několik benzenových kruhů. Takové sloučeniny se nazývají vícejádrové aromatické sloučeniny. Například naftalen je dobře známé léčivo pro ochranu produktů z vlny z můry.
Benzen
Tento nejjednodušší zástupce arenes se skládá pouze z benzenového kruhu. Jeho molekulární vzorec je C6H6. Strukturní vzorec benzenové molekuly je nejčastěji reprezentován cyklickou formou navrhovanou A. Kekulem v roce 1865.
Ad
Výhoda tohoto vzorce je správný odraz složení a ekvivalence všech atomů C a H v kruhu. Nemohla však vysvětlit mnoho chemických vlastností arén, proto je výrok o přítomnosti tří konjugovaných dvojných vazeb C = C chybný. To se stalo známou pouze příchodem moderní teorie komunikace.
Mezitím je dnes také psáno vzorec benzenu způsobem, který navrhuje Kekule. Za prvé, je vhodné psát rovnice s jeho pomocí. chemické reakce. Za druhé, moderní chemici v ní vidí jen symbol, ne skutečnou strukturu. Struktura benzenové molekuly je dnes přenášena různými typy strukturních vzorců.
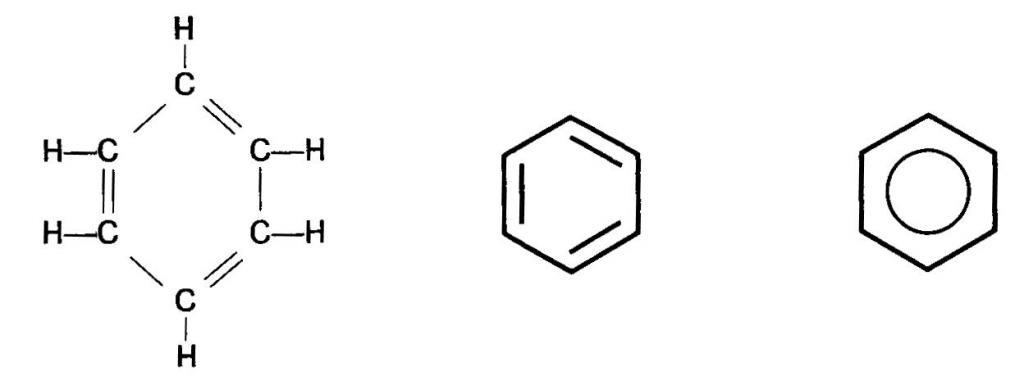
Struktura benzenového kruhu
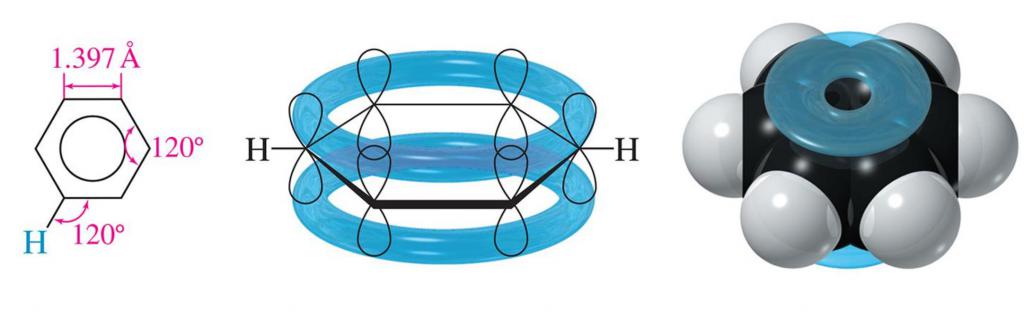
Hlavním rysem benzenového jádra je nepřítomnost jednoduchých a dvojných vazeb v něm v tradičním smyslu. Podle moderních konceptů se zdá, že benzenová molekula je plochý šestiúhelník s délkou strany rovnou 0,140 nm. Ukazuje se, že délka vazby C-C v benzenu je mezilehlá hodnota mezi jednotlivým (jeho délka je 0,154 nm) a dvojnásobnou hodnotou (0,134 nm). Ve stejné rovině ležely vazby C-H, tvořící úhel 120 ° s okraji šestiúhelníku.
Každý atom C v struktuře benzenu je ve sp2-hybridním stavu. Je propojen třemi hybridními orbitály se dvěma atomy C umístěnými v sousedství a jedním atomem N. To znamená, že tvoří tři s-vazby. Další, ale již nehybridizovaný 2p-orbitál se překrývá se stejnými orbitály sousedních atomů C (vpravo a vlevo). Jeho osa je kolmá k rovině prstence, a proto se překrývají orbitály nad a pod ním. V tomto případě se vytvoří společný uzavřený p-elektronový systém. Kvůli rovnocennému překryvu 2p orbitálů šesti atomů C dochází k "vyrovnání" vazeb C-C a C = C.
Ad
Výsledkem tohoto procesu je podobnost takových "jeden a půl" vazeb s dvojitými i jednoduchými vazbami. To vysvětluje skutečnost, že arény vykazují chemické vlastnosti charakteristické jak pro alkány, tak pro alkény.
Energie vazby uhlík-uhlík v benzenovém kruhu je 490 kJ / mol. Co je také průměr mezi energií jednoduchých a násobných dvojných vazeb.
Nomenklatura arény
Základem názvů aromatických uhlovodíků je benzen. Atomy v kruhu jsou očíslovány vyššími substituenty. Pokud jsou substituenty ekvivalentní, číslování se provádí nejkratší cestou.
Pro mnoho benzenových homologů se často používají triviální názvy: styren, toluen, xylen atd. Aby se odrážely relativní polohy substituentů, je běžné používat předpony orto, meta, para.
Ad
Pokud jsou v molekule funkční skupiny, například karbonylová skupina nebo karboxylová skupina, potom se molekula arény považuje za aromatický radikál, který je s ním spojen. Například -C6H5-fenyl, -C6H4-fenylen, C6H5-CH2-benzyl.
Fyzikální vlastnosti
První zástupci v homologní série Benzen je bezbarvá kapalina se specifickým zápachem. Jejich hmotnost je lehčí než voda, ve které se prakticky nerozpouští, ale ve většině organických rozpouštědel se dobře rozpouští.
Všechno aromatických uhlovodíků spálí s výskytem kouřového plamene, což je vysvětleno vysokým obsahem C v molekulách. Teploty tání a varu se zvyšují se zvyšujícími se hodnotami molekulových hmotností v homologní řadě benzenu.
Chemické vlastnosti benzenu
Z různých chemických vlastností arény by měly být substituční reakce uváděny zvlášť. Velmi významné jsou také některé adiční reakce, které se vyskytují za zvláštních podmínek a oxidačních procesů.
Substituční reakce
Zcela mobilní p-elektrony benzenového kruhu jsou schopny velmi aktivně reagovat s útočícími elektrofily. Benzenové jádro samotné v benzenu a uhlovodíkový řetězec s ním spojený ve svých homologech se účastní takové elektrofilní substituce. Mechanismus tohoto procesu je podrobněji studován organickou chemii. Chemické vlastnosti arén souvisejících s elektrofilním útokem se projevují třemi stadii.
Ad
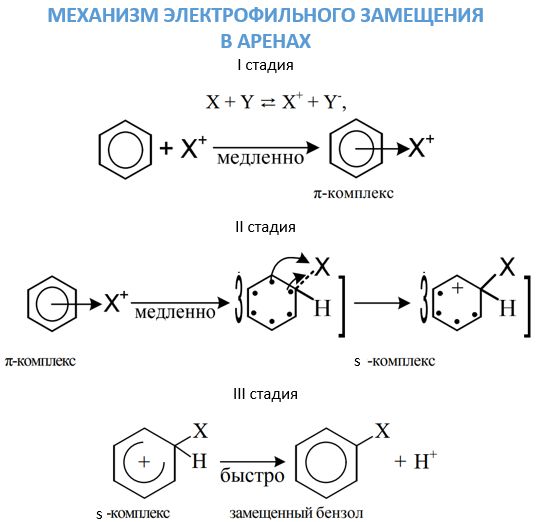
- První fáze. Vzhled komplexu π v důsledku vazby systému p-elektronů benzenového jádra na částic X + , který se váže na šest p-elektronů.
- Druhá fáze Přechod p-komplexu na s, kvůli uvolnění dvojice šesti p-elektronů dvojice za vzniku kovalentní vazby C-X. A další čtyři jsou redistribuovány mezi pěti atomy uhlíku v benzenovém kruhu.
- Třetí etapa. Doprovázeno rychlou eliminací protonu z komplexu s.
Bromace benzenu za přítomnosti bromidu železa nebo hliníku bez zahřívání vede k výrobě brombenzenu:
C 6 H 6 + Br 2 -> C 6 H 5 -Br + Br.
Nitrace se směsí kyseliny dusičné a kyseliny sírové vede k tvorbě sloučenin s nitroskupinou v kruhu:
C 6 H 6 + HONO 2 -> C 6 H 5 -NO 2 + 2 O.
Sulfonace se provádí bisulfidovým iontem, který je výsledkem reakce:
3 H 2 SO 4, SO 3 H + + H 3 O + + 2 HSO 4 - ,
nebo oxid sírový.
Odpovídá této chemické vlastnosti reakce arény:
C 6H 6 + SO 3H + -> C 6H 5- SO 3H + H + .
Reakce alkylové a acylové substituce nebo Friedel - Craftsova reakce se provádějí v přítomnosti bezvodého chloridu hlinitého.
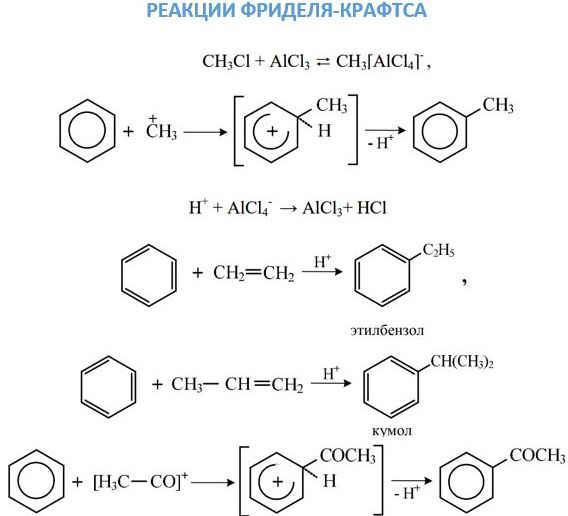
Tyto reakce jsou pro benzen pravděpodobně nepravděpodobné a postupují s obtížemi. Přidání halogenovodíků a vody do benzenu nedochází. Při velmi vysokých teplotách za přítomnosti platiny je však možná hydrogenační reakce:
C 6H 6 + 3H 2 -> C 6H 12 .
Při ultrafialovém ozařování se molekuly chloru mohou připojit k benzenové molekule:
C 6 H 6 + 3Cl 2 -> C 6 H 6 CI 6 .
Oxidační reakce
Benzen je vysoce odolný vůči oxidačním činidlům. Takže nezmění růžový roztok manganistanu draselného. V přítomnosti oxidu vanadia se však může oxidovat vzduchem kyslíkem na kyselinu maleinovou:
Ad
C 6H 6 + 4O -> COOH-CH = CH-COOH.
Ve vzduchu vznítí benzen s výskytem sazí:
2C 6H 6 + 3O 2 → 12C + 6H 2O.
Chemické vlastnosti arény
- Nahrazení
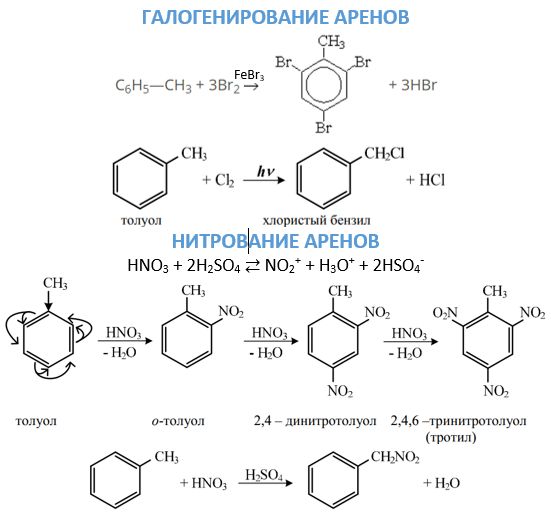
- Halogenace může probíhat různými způsoby v závislosti na reakčních podmínkách. V přítomnosti odpovídajícího halogenidu železa nebo hliníku, bude substituce probíhat v kruhu podle mechanismu popsaného výše. Za účelem zavedení atomu halogenu do postranního řetězce se reakce provádí zahříváním bez katalyzátoru nebo ve světle.
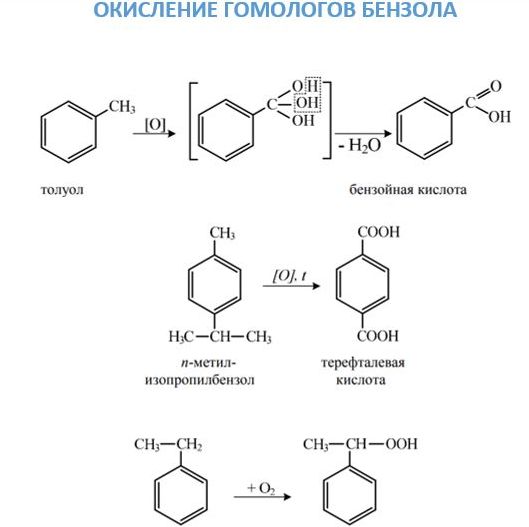
- Nitrování aromatických uhlovodíků s ionty nitronia, které vzniká smícháním kyseliny sírové a kyseliny dusičné, vede k připojení nitroskupiny k benzenovému jádru. Spojení nitroskupiny s postranním řetězcem je možné během Konovalovovy reakce. 2. Oxidace. Tuto chemickou vlastnost arenes lze vidět ze dvou hledisek. Na jedné straně jsou poměrně snadno oxidovány a postranní řetězec je vystaven působení pro vytvoření karboxylové skupiny. Pokud jsou dva substituenty připojeny k kruhu v molekule aromatického uhlovodíku, vznikne kyselina dvojsýtná. Na druhou stranu, stejně jako benzen, hoří s tvorbou sazí a vody.
Pravidla orientace
Která konkrétní pozice (o-, m- nebo p-) obsadit během interakce elektrofilního činidla s benzenovým kruhem je určena pravidly:
- pokud je v benzenovém jádru nějaký substituent, je to ten, který řídí přicházející skupinu do určité polohy;
- Všechny orientující substituenty jsou rozděleny do dvou skupin: Orientační skupiny prvního druhu směřují příchozí skupinu atomů k ortho a para poloze (-NH2, -OH, -CH3, -C2H5, halogeny); Orientanti druhého druhu směrují přicházející náhražky do polohy meta (-N02, -S03H, -CHO, -COOH).
Orientanti jsou zde uvedeny v pořadí klesající vodící síly.
Je třeba poznamenat, že toto oddělení substituentů skupiny je podmíněno skutečností, že ve většině reakcí je pozorována tvorba všech tří izomerů. Orientační činitelé pouze ovlivňují, které z izomerů budou získány ve větších množstvích.
Získání Arenas
Hlavními zdroji arény jsou suchá destilace uhelného a rafinace ropy. Uhelný dehet obsahuje obrovské množství všech druhů aromatických uhlovodíků. Některé druhy oleje obsahují až 60% arény, které lze snadno izolovat jednoduchou destilací, pyrolýzou nebo praskání.
Syntetické výrobní metody a chemické vlastnosti arenes jsou často vzájemně propojeny. Benzen, stejně jako jeho homology, se získá jedním z následujících způsobů.
1. Reforma ropných produktů. Dehydrogenace alkanů je nejdůležitější průmyslovou metodou syntézy benzenu a mnoha jeho homologů. Reakce se provádí průchodem plynů nad ohřátým katalyzátorem (Pt, Cr203, oxidy Mo a V) při t = 350-450 ° C:
C 6H 14 -> C 6H 6 + 4H 2 .
2. Reakce společnosti Würz-Fittig. Provede se ve stupni získávání organokovových sloučenin. V důsledku toho může reakce produkovat několik produktů.
3. Trimerace acetylenu. Samotný acetylen, stejně jako jeho homologové, jsou schopni při zahřívání s katalyzátorem vytvářet arény:
3C 2 H 2 -> C 6 H 6 .
4. Friedel-Craftsova reakce. Při chemických vlastnostech arény, způsobu výroby a transformace homologů benzenu se uvažuje výše.
5. Příprava odpovídajících solí. Benzen lze rozlišovat destilací solí. benzoové kyseliny s alkalickými látkami:
C 6H 5- COONa + NaOH -> C 6H 6 + Na 2CO 3 .
6 Obnova ketonu:
C 6 H 5- CO-CH 3 + Zn + 2 HCl -> C 6 5 -CH 2- CH 3 + 20 + ZnCl 2 ;
CH3-C6H5-CO-CH3 + NH2-NH2-> CH3-C6S-CH2-CH3 + 2O.
Použijte arény
Chemické vlastnosti a aplikace arény jsou přímo propojeny, protože většina aromatických sloučenin se používá pro další syntézu v chemické výrobě a není použita v hotové formě. Výjimkou jsou látky používané jako rozpouštědla.
Benzen C 6 H 6 se používá hlavně při syntéze ethylbenzenu, kumenu a cyklohexanu. Na svém základě přijímá meziprodukty pro výrobu různých polymerů: kaučuky, plasty, vlákna, barviva, povrchově aktivní látky, insekticidy, drogy.

Toluen C 6 H 5 -CH 3 se používá při výrobě barviv, drog a výbušnin.
Xyleny C 6 H 4 (CH 3 ) 2 ve smíšené formě (technický xylén) se používají jako rozpouštědlo nebo jako počáteční přípravek pro syntézu organických látek.
Isopropylbenzen (nebo kumen) C6H4-CH (CH3) 2 je počáteční reakční činidlo pro syntézu fenolu a acetonu.
Vinylbenzen (styren) C 6 H 5 -CH = CH 2 je surovina pro výrobu nejdůležitějšího polymerního materiálu - polystyrenu.