Chemické vlastnosti vodíku: vlastnosti a použití
Zvažte, co představuje vodík. V průběhu kurzu jsou studovány chemické vlastnosti a příprava tohoto nekovu. anorganická chemie ve škole. Tento prvek je veden periodickou tabulkou Mendeleeva, a proto si zaslouží podrobný popis.

Podrobnosti o otevření položky
Před zvážením fyzikálních a chemických vlastností vodíku zjistíme, jak byl tento důležitý prvek nalezen.
Lékárníci, kteří pracovali v šestnáctém a sedmnáctém století, opakovaně uváděli ve svých spisech o hořlavém plynu, který je uvolňován při vystavení účinkům kyselých kovů. Ve druhé polovině osmnáctého století byl G. Cavendish schopen shromáždit a analyzovat tento plyn a dát mu název "hořlavý plyn".
Fyzikální a chemické vlastnosti vodíku v té době nebyly studovány. Teprve koncem osmnáctého století dokázal A. Lavoisier analýzou dokázat, že bylo možné získat tento plyn analýzou vody. O něco později začal volat nový prvek hydrogen, což znamená "zrodit vodu". Vodík vděčí za své současné ruské jméno M.F. Solovo'ev.
Být v přírodě
Chemické vlastnosti vodíku lze analyzovat pouze na základě jeho výskytu v přírodě. Tento prvek je přítomen v hydro - a litosféře a je také součástí nerostů: přírodní a související plyn, rašelina, ropa, uhlí, hořlavé břidlice. Je obtížné si představit dospělé, který by nevěděl, že vodík je nedílnou součástí vody.
Kromě toho se tento nekovový materiál nachází u zvířat ve formě nukleových kyselin, bílkovin, sacharidů, tuků. Na naší planetě se tento prvek nachází ve volné formě poměrně vzácně, možná jen v přírodním a vulkanickém plynu.
Ve formě plazmy představuje vodík zhruba polovinu hmotnosti hvězd a slunce, navíc je součástí mezihvězdného plynu. Například ve volné formě, stejně jako ve formě methanu, čpavku, je tento nekov kov přítomen v složení komet a dokonce i v některých planetách.
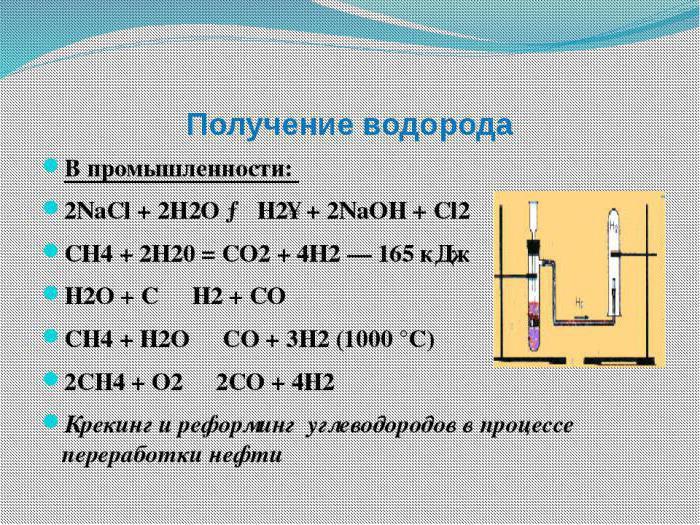
Fyzikální vlastnosti
Před zvážením chemických vlastností vodíku je třeba poznamenat, že za normálních podmínek je plynná látka lehčí než vzduch, která má několik izotopových forem. Je téměř nerozpustný ve vodě, má vysokou tepelnou vodivost. Protium s hmotnostním číslem 1 se považuje za jeho nejsilnější formu. Tritium, které má radioaktivní vlastnosti, je vytvořeno v přírodě z atmosférického dusíku při vystavení neuronům UV záření.
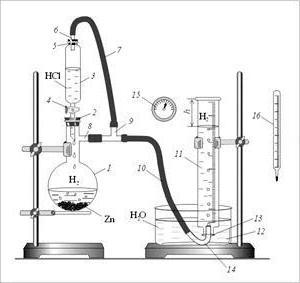
Vlastnosti struktury molekuly
Aby bylo možno zvážit chemické vlastnosti vodíku, reakce, které jsou charakteristické pro něj, se budou zabývat zvláštnostmi jeho struktury. V této diatomové molekule je kovalentní nepolární chemická vazba. Tvorba atomového vodíku je možná interakcí aktivních kovů s kyselými roztoky. Ale v této podobě je tento nekovový schopen existovat pouze v nezanedbatelném časovém období, téměř okamžitě se rekombinuje do molekulární formy.

Chemické vlastnosti
Zvažte chemické vlastnosti vodíku. Ve většině sloučenin, které tento chemický prvek tvoří, vykazuje oxidační stav +1, který činí podobný jako aktivní (alkalických) kovů. Hlavní chemické vlastnosti vodíku, charakterizující ho jako kov:
- interakce s kyslíkem za vzniku vody;
- reakce s halogeny, doprovázená tvorbou halogenovodíku;
- získání sirovodíku v kombinaci se sírou.
Níže je rovnice reakcí charakterizující chemické vlastnosti vodíku. Upozorňujeme na skutečnost, že jako nekovová (s oxidačním stavem -1) působí pouze při reakci s aktivními kovy a tvoří s sebou odpovídající hydridy.
Vodík při normální teplotě neaktivně interaguje s jinými látkami, takže většina reakcí se provádí pouze po předehřevu.
Podívejme se podrobněji na některé chemické interakce elementu, který vede periodickou tabulku chemických prvků Mendelejeva.
Reakce tvorby vody je doprovázena uvolněním 285,937 kJ energie. Při vyšších teplotách (více než 550 stupňů Celsia) je tento proces doprovázen silnou explozí.
Mezi těmito chemickými vlastnostmi plynného vodíku, které nalezly významné využití v průmyslu, je zajímavé jeho vzájemné působení s oxidy kovů. Katalytickou hydrogenací v moderním průmyslu se zpracovávají oxidy kovů, například čistý kov se extrahuje z oxidu železitého (směsný oxid železa). Tato metoda umožňuje efektivní zpracování šrotu.
Syntéza amoniaku, která zahrnuje interakci vodíku s vzdušným dusíkem, je také poptávka v moderním chemickém průmyslu. Mezi podmínkami výskytu této chemické interakce zaznamenáváme tlak a teplotu.

Závěr
Jedná se o vodík, který je za normálních podmínek chemicky nízkým obsahem. S rostoucí teplotou se jeho aktivita výrazně zvyšuje. Tato látka je požadována v organické syntéze. Například hydrogenací mohou být ketony redukovány na sekundární alkoholy a aldehydy mohou být převedeny na primární alkoholy. Kromě toho je možno pomocí hydrogenace transformovat nenasycené uhlovodíky třídy ethylenu a acetylenu na limitní sloučeniny z metanové řady. Vodík je správně považován za jednoduchou látku v poptávce v moderní chemické výrobě.