Chemie. Oxidy: jejich klasifikace a vlastnosti
Mezi různými třídami anorganických látek se rozlišuje komplex binárních sloučenin tvořených třemi skupinami. Jedná se o kyselé, zásadité a amfoterní oxidy. Jejich klasifikace a vlastnosti závisí na atomech, jejichž chemický prvek je kombinován s kyslíkem. V našem článku se seznámíme s typickými chemickými reakcemi charakteristickými pro oxidy a také zjišťujeme jejich genetickou souvislost s ostatními třídami anorganických sloučenin: zásadami, kyselinami a solemi.
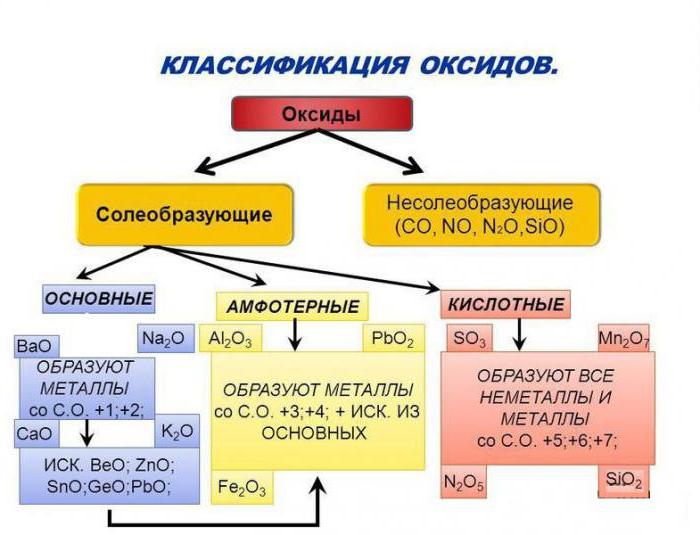
Vlastnosti základních oxidů
Zvažte sloučeniny, které obsahují atomy typických kovů. Například: CuO, FeO, MgO obsahují elektricky neutrální částice mědi, železa a hořčíku, což znamená, že jde o základní oxidy. Jejich klasifikace a vlastnosti závisí na povaze kovového prvku. Pokud složení látky obsahuje atomy alkalických kovů nebo kovů alkalických zemin, pak jsou její molekuly schopné interagovat s vodou.
Ad
Reakčním produktem s uvolněním velkého množství tepla budou alkálie, například žíravina nebo hydroxid vápenatý. Některé oxidy, jako např oxid mědi nebo železo nereaguje přímo s vodou, proto se jejich báze získávají nepřímo: z odpovídajících solí, které interagují s alkalickými látkami. Hlavní věc je jejich vlastnost - reagovat s kyselinami, vytvářet sůl a vodu.
Jaké oxidy se nazývají kyselé?
Klasifikace a vlastnosti kyselin, zásad, oxidů a solí jsou určeny především jejich schopností vzájemné interakce. Navíc z látek jedné třídy je možné získat sloučeniny jiné skupiny. Tak se kyseliny v kyselých oxidů v reakci s vodou. Výrobkem hydratace anhydridu kyseliny sírové je například kyselina sírová a procházením oxidem uhličitým CO 2 vodou získáme roztok slabý kyseliny uhličité. Oxidy kyselin, jejich klasifikace a vlastnosti proto závisí na povaze interakce s vodou a tvorbě kyseliny. Dodáváme také, že v molekule binární sloučeniny atomy nekovových prvků jsou navázány na atomy kyslíku. Jejich nejdůležitější vlastností bude schopnost reagovat s alkalickými látkami, produkty budou sůl a voda.
Ad

Proč oxid hlinitý reaguje s kyselinami a zásadami?
Jak jste si všimli, základní oxidy reagují s kyselinami, oxidy kyselin reagují s alkalickými látkami. Sloučeniny jako Al2O3 nebo ZnO jsou amfoterní oxidy. Jejich klasifikace a vlastnosti jsou založeny na schopnosti těchto látek souběžně reagovat s kyselinami a aktivními bázemi. Při interakci s oxidem hlinitým, například kyselinou sírovou, získáme její síran. Při reakci stejné sloučeniny s taveninou hydroxidu sodného vzniká sůl - metaaluminát sodný.
Jak je vidět, amfoterní prvky mohou tvořit oxidy, které si zachovávají schopnost reagovat jak s alkalickými, tak s kyselinami. Přicházejí s tvorbou soli. Vzhledem k oxidům, jejich klasifikaci a vlastnostem není možné říci o jiné skupině těchto binárních sloučenin. Pokud látka, jako je CO - oxid uhelnatý nebo oxid dusičitý, nemůže reagovat ani s kyselinami ani zásadami, pak sloučenina není schopna tvořit soli. Takové oxidy se nazývají lhostejné nebo lhostejné. Jak si pamatujeme, oxidy jsou binární sloučeniny, které nutně obsahují kyslík.
Ad

Získání oxidů
Pokračujeme v klasifikaci, vlastnostech, získávání oxidů. Existují tři způsoby, jak je v laboratoři těžba sloučenin. Nejběžnější z nich je oxidace jednoduchých látek. Spalování komplexních sloučenin, jako je zemní plyn nebo olej, je dalším způsobem, jak vyrábět plynný uhlík a oxidy vodíku. K třetímu způsobu přiřazujeme tepelný rozklad určitých solí kyselin uhličitých a dusičnanů, stejně jako zahřívání vodou nerozpustných bází, jako je například měď nebo hydroxid železa. To vytváří oxidy kovů a vodu.
Interakce oxidů mezi sebou
Při zkoumání oxidů, jejich klasifikaci a chemických vlastnostech se obracíme k reakcím mezi látkami kyselých a základních skupin. Výsledkem jsou sloučeniny, které patří do skupiny solí. Pokud se například oxidem uhličitým prochází roztokem oxidu vápenatého (vápenná voda), stává se zakalený v důsledku tvorby nerozpustných částic uhličitanu vápenatého CaCO 3 . V průmyslu jsou široce používané reakce interakce několika látek: sodík, vápník a křemík. Zahříváme jejich směs spolu s technickou sodou, získáme sklo.
Oxid vodíku - voda má zvláštní vlastnosti, budeme o nich hovořit dále. H 2 O je nejběžnější a nezbytná směs na Zemi. Schopnost molekul vytvářet vodíkové vazby poskytuje hlavní vlastnosti vody jako univerzální rozpouštědlo se specifickými vlastnostmi: vysokou tepelnou kapacitou a tepelnou vodivostí. Jsou velmi důležité pro metabolické procesy v živých organizmech.
Ad
Voda, jako oxid, reaguje s různými kyselinami a zásaditými oxidy. V prvním případě se získávají kyseliny, ve druhých - zásadách. Specifickou reakcí vodíku je provádět reakce hydrolytického rozkladu (hydrolýza). Jsou mezi nimi velmi časté organické látky původu. Jedná se o hydrolýzu bílkovin, sacharidů a tuků, které probíhají v gastrointestinálním traktu, štěpení celulózy mikroorganismy - saprotrofů apod.
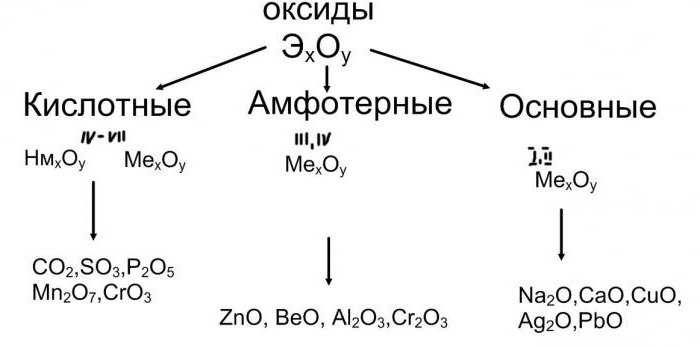
Oxidy, zásady, soli: klasifikace, vlastnosti
Mezi hlavní třídy anorganické látky existuje genetická vazba, která dokazuje možnost jejich vzájemné transformace. Takže od základního oxidu aktivního kovu lze získat bázi a z ní - sůl. Příkladem takového řetězce transformací je následující schéma: oxid sodný - hydroxid sodný - uhličitan sodný. Oxidy kyselin slouží jako výchozí sloučeniny při reakcích s vodou. Produkt, který je v tomto případě získán, je kyselý. Například: oxid uhličitý - kyselina uhličitá - uhličitan sodný.
Reakce kyseliny s hydroxidy, která se nazývá neutralizace, povede k vzhledu solí. V obou případech bude konečným článkem v genetickém řetězci sloučenina této třídy, která spojuje transformace nekovových a kovových chemických prvků. Existuje tedy reverzní mechanismus: ze soli na báze, kyseliny nebo na jednoduchou látku.

V tomto článku jsme studovali klasifikaci a chemické vlastnosti hlavních tříd anorganických látek.