Peptidová vazba je základem primární struktury proteinu. Charakterizace a tvorba peptidové vazby
Peptidová vazba je silné spojení mezi fragmenty dvou aminokyselin, které jsou základem tvorby lineárních proteinové struktury a peptidy. V takových molekulách se každá aminokyselina (s výjimkou terminálních) kombinuje s předchozí a další.
V závislosti na počtu vazeb mohou peptidové vazby vytvářet dipeptidy (sestávají ze dvou aminokyselin), tripeptidy (tři), tetrapeptidy, pentapeptidy atd. Krátké řetězce (od 10 do 50 monomerů) se nazývají oligopeptidy a dlouhé - polypeptidy a proteiny hmotnost více než 10 tisíc.
Charakteristika peptidové vazby
Peptidová vazba je kovalentní chemická sloučenina mezi prvním atomem uhlíku jedné aminokyseliny a atomem dusíku druhého, která je výsledkem interakce alfa-karboxylové skupiny (COOH) s alfa-aminoskupinou (NH2). Pokud k tomu dojde, nukleofilní substituce OH-hydroxylové skupiny na aminoskupině, ze které je vodík oddělen. Výsledkem je vytvoření jediné vazby CN a molekuly vody.
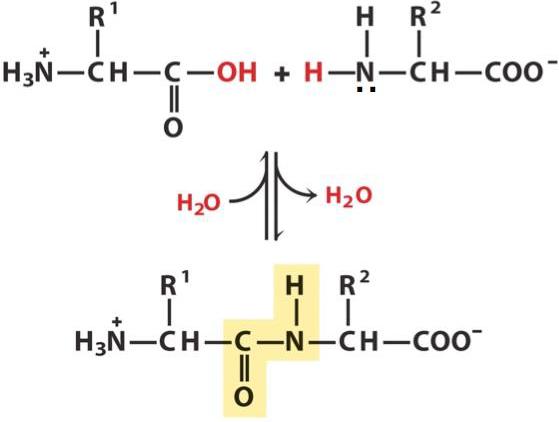
Vzhledem k tomu, že během reakce jsou některé složky (OH skupiny a atom vodíku) ztraceny, peptidové jednotky již nejsou nazývány aminokyselinami, ale aminokyselinovými zbytky. Vzhledem k tomu, že tyto obsahují vždy 2 atomy uhlíku, dochází v řetězci peptidu ke střídání C-C a CN vazeb, které tvoří páteř peptidu. Na jeho stranách jsou aminokyselinové radikály. Vzdálenost mezi atomy uhlíku a dusíku se pohybuje od 0,132 do 0,127 nm, což znamená neurčitou vazbu.
Peptidová vazba je velmi silná forma chemické interakce. Při standardních biochemických podmínkách, které odpovídají buněčnému prostředí, nepodléhá samodestrukci.
Peptidová vazba proteinů a peptidů je charakterizována vlastností koplanarity, protože všechny atomy podílející se na jeho tvorbě (C, N, O a H) jsou umístěny ve stejné rovině. Tento jev se vysvětluje tuhost (tj. Nemožnost otáčení prvků kolem vazby) vyplývající z rezonanční stabilizace. Mezi aminokyselinovým řetězcem mezi rovinami peptidových skupin jsou atomy uhlíku spojené s radikály.
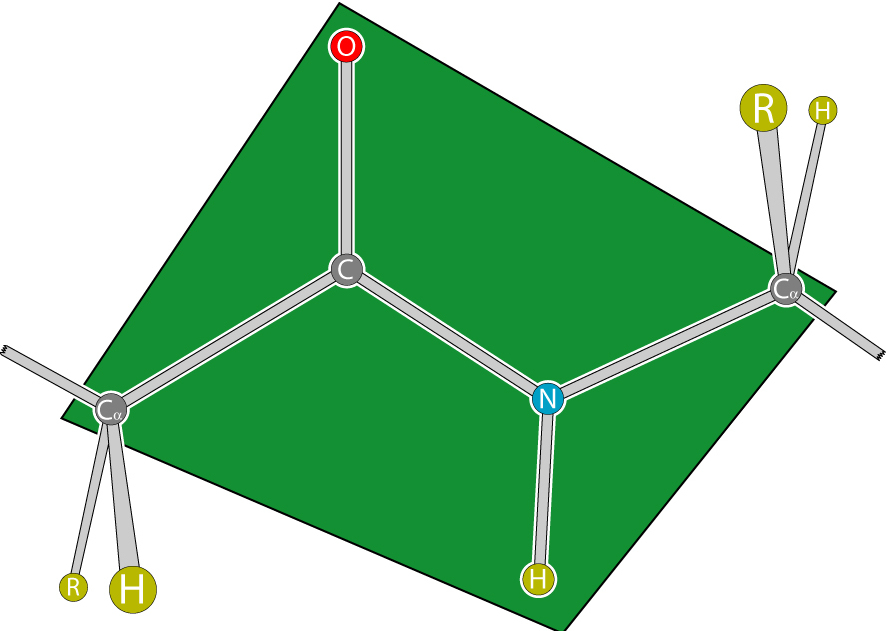
Typy konfigurace
V závislosti na poloze alfa-uhlíkových atomů vzhledem k peptidové vazbě mohou mít tyto dvě konfigurace:
- "cis" (umístěný na jedné straně);
- "trance" (jsou z různých stran).
Transforma je odolnější. Někdy konfigurace jsou charakterizovány umístěním radikálů, které nemění podstatu, protože jsou spojeny s alfa-uhlíkovými atomy.
Rezonanční jev
Zvláštnost peptidové vazby spočívá v tom, že je 40% duální a může být ve třech formách:
- Ketol (0,132 nm) - vazba CN je stabilizována a zcela jednotlivá.
- Přechodná nebo mezomerická - meziproduktová forma je částečně neurčitá.
- Enol (0,127 nm) - peptidová vazba se úplně zdvojnásobí a sloučenina C-O je zcela jednotná. V tomto případě získává kyslík částečně negativní náboj a atom vodíku - částečně pozitivní.
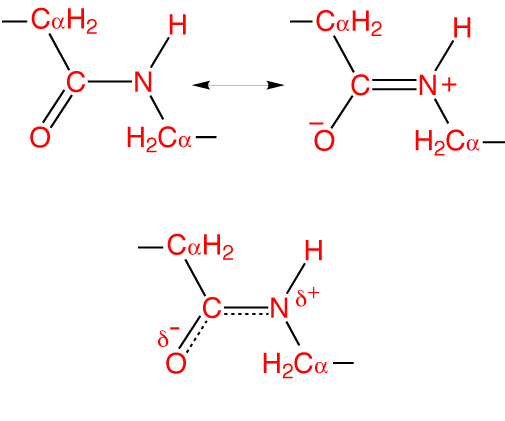
Tato vlastnost se nazývá rezonanční účinek a vysvětluje delokalizací kovalentní vazby mezi atomy uhlíku a dusíku. V tomto případě hybridní sp 2 orbitaly vytvářejí elektrický oblak šířící se na atom kyslíku.
Vytváření peptidové vazby
Tvorba peptidové vazby je typická polykondenzační reakce, která je termodynamicky nepříznivá. Při přirozených podmínkách se rovnováha posune k volným aminokyselinám, a proto k provedení syntézy je nutný katalyzátor, který aktivuje nebo modifikuje karboxylovou skupinu pro snadnější udržování hydroxylu.
V živé buňce vzniká peptidová vazba v centru syntézy proteinů, kde specifické enzymy pracující s energií makroergických vazeb působí jako katalyzátor.