Vlastnosti solí: fyzikální a chemické
Každý den jsme konfrontováni s solemi a ani nemyslíme na roli, kterou hrají v našem životě. Ale bez nich by voda nebyla tak chutná a jídlo by nemělo radost a rostliny by neprostřely a život na zemi by nemohl existovat, kdyby v našem světě nebyla žádná sůl. Takže jaké jsou tyto látky a jaké vlastnosti solí je činí nepostradatelnými?
Co je sůl
Ve složení je to nejpočetnější třída, která se vyznačuje různorodostí. это продукт реакции между кислотой и основанием, при которой водородный атом заменяется металлическим. Již v 19. století chemik J. Vercelius definoval sůl - to je produkt reakce mezi kyselinou a bází, ve které je atom vodíku nahrazen kovovým. Ve vodě jsou soli obvykle disociovány na kov nebo amonium (kation) a kyselý zbytek (anion).

Sůl můžete získat následujícími způsoby:
- interakcí kovu a nekovu, v tomto případě bude bez kyslíku;
- když kov reaguje s kyselinou, získá se sůl a uvolní se vodík;
- kov může z roztoku vyloučit jiný kov;
- кислотного и основного (еще их называют оксидом неметалла и оксидом металла соответственно); ve vzájemném působení dvou oxidů , kyselých a zásaditých (také se nazývají nekovový oxid a oxid kovu);
- reakce oxidu kovu a kyseliny produkuje sůl a vodu;
- reakce mezi bází a nekovovým oxidem také dává sůl a vodu;
- při použití iontové výměnné reakce mohou reagovat různé vodorozpustné látky (báze, kyseliny, soli), ale reakce bude probíhat, pokud se ve vodě vytvoří plyn, voda nebo slabě rozpustné (nerozpustné) soli.
Vlastnosti solí závisejí pouze na chemickém složení. Ale nejprve se podívejme na jejich třídy.
Klasifikace
V závislosti na složení se rozlišují následující třídy solí:
- na obsah kyslíku (obsahující kyslík a bez kyslíku);
- na interakci s vodou (rozpustný, slabě rozpustný a nerozpustný).
Taková klasifikace plně neodráží rozmanitost látek. Moderní a nejkompletnější klasifikace, která odráží nejen složení, ale také vlastnosti solí, je uvedena v následující tabulce.
| Sůl | |||||
|---|---|---|---|---|---|
| Normální | Surové | Hlavní | Dvakrát | Smíšené | Komplexní |
| Vodík je zcela nahrazen | Atomové atomy jsou nahrazeny kovem zcela ne zcela | Základní skupiny jsou nahrazeny kyselými zbytky, které nejsou plně | Skládá se ze dvou kovů a jednoho kyselého zbytku | Skládá se z jednoho kovu a dvou kyselých zbytků | Komplexní látky složené z komplexního kationtu a aniontu nebo kationtu a komplexního aniontu |
| NaCl | KHSO 4 | FeOHSO 3 | KNaSO 4 | CaClBr | [Cu (NH3) 4 ] S04 |
Fyzikální vlastnosti
Jakkoli může být široká skupina těchto látek, je možné vyjasnit obecné fyzikální vlastnosti solí. Jsou to látky nemulové struktury s iontovou krystalovou mřížkou.
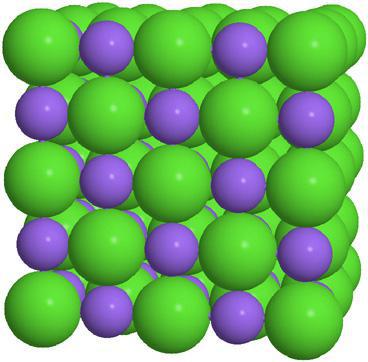
Velmi vysoké teploty tání a varu. Za normálních podmínek všechny soli nevedou k elektřině, ale většina z nich je dokonale vodivá v roztoku.
Barva může být velmi odlišná, záleží na iontu kovu, který je jeho součástí. Síran železnatý (FeSO 4 ) je zelený, chlorid železitý (FeCl3) je tmavě červený a chromitan draselný (K 2 CrO 4 ) je krásně jasně žlutá barva. Ale většina solí je stále bezbarvá nebo bílá.
Ad

Rozpustnost ve vodě se také liší a závisí na složení iontů. V podstatě mají všechny vlastnosti fyzikálních vlastností solí. Závisí na tom, který iont kovu a který zbytek kyseliny je v kompozici obsažen. Pokračujeme ve zvažování soli.
Chemické vlastnosti solí
I zde je důležitá vlastnost. Stejně jako fyzikální, chemické vlastnosti solí závisí na jejich složení. A také na které třídě patří.

Ale obecné vlastnosti solí lze ještě rozlišit:
- mnoho z nich se při zahřátí rozkládá na dva oxidy: kyselé a zásadité, bez kyslíku - kovy a nekovy;
- soli interagují s jinými kyselinami, ale reakce probíhá pouze v případě, že sůl obsahuje kyselý zbytek slabé nebo těkavé kyseliny nebo výsledkem je nerozpustná sůl;
- interakce s alkálií je možná, pokud kation tvoří nerozpustnou bázi;
- reakce je možná mezi dvěma různými solemi, ale pouze pokud se jedna z nově vytvořených solí nerozpustí ve vodě;
- může dojít k reakci s kovem, ale je to možné pouze tehdy, pokud kov, který se nachází vpravo od napětí, od kovu obsaženého ve slané vodě.
Chemické vlastnosti normálních solí jsou diskutovány výše, zatímco jiné třídy reagují s látkami poněkud jiným způsobem. Rozdíl je ovšem pouze na produktech v zásuvce. V podstatě se zachovávají všechny chemické vlastnosti solí, stejně jako požadavky na reakce.