Relativní atomová hmotnost prvku v chemii a historie jeho definice
V procesu vývoje vědy se chemie potýkala s problémem výpočtu množství látky pro provádění reakcí a látek získaných v jejich průběhu.
Dnes pro takové výpočty chemické reakce mezi látkami a směsmi se používá hodnota relativní atomové hmotnosti uvedené v periodické tabulce chemických prvků DI Mendeleev.
Chemické procesy a vliv podílu prvku na látkách na průběh reakce
Moderní věda pod definicí "relativní atomové hmotnosti chemického prvku" znamená, kolikrát hmotnost atomu daného chemického prvku je více než jedna dvanáctina atomu uhlíku.
S narozením doby chemie se zvýšila potřeba přesných definic průběhu chemické reakce a jejích výsledků. 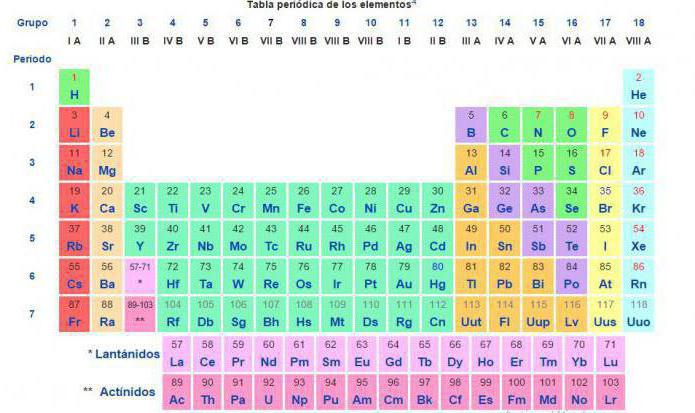 Proto se chemici neustále snažili vyřešit problém přesných hmotností interakčních prvků v látce. Jedno z nejlepších rozhodnutí v té době bylo závazné pro nejlehčí prvek. A hmotnost jeho atomu byla považována za jednotku.
Proto se chemici neustále snažili vyřešit problém přesných hmotností interakčních prvků v látce. Jedno z nejlepších rozhodnutí v té době bylo závazné pro nejlehčí prvek. A hmotnost jeho atomu byla považována za jednotku.
Historický průběh počítání látek
Zpočátku byl použit vodík, pak kyslík. Tato metoda výpočtu však byla nepřesná. Důvodem byla přítomnost izotopů s hmotností 17 a 18 v kyslíku.
 Proto má směs izotopů technicky přijatá jiná čísla než šestnáct. V současné době se relativní atomová hmotnost prvku vypočítá na základě hmotnosti atomu uhlíku, který je základem, v poměru 1/12.
Proto má směs izotopů technicky přijatá jiná čísla než šestnáct. V současné době se relativní atomová hmotnost prvku vypočítá na základě hmotnosti atomu uhlíku, který je základem, v poměru 1/12.
Dalton položil základy relativní atomové hmotnosti prvku
Teprve později v devatenáctém století dalton navrhl výpočet nejlehčího chemického prvku, vodíku. Na přednáškách svým studentům ukázal na postavách vyřezaných ze dřeva, jak jsou spojeny atomy. U ostatních prvků použil data dříve získaná jinými vědci.
Ad
Podle experimentů Lavoisiera voda obsahuje pětinu procent vodíku a osmdesát pět procent kyslíku. S těmito údaji Dalton vypočítal, že relativní atomová hmotnost prvku, který je součástí vody, v tomto případě kyslíku, je 5,67. Omylem jeho výpočtů je skutečnost, že se domníval, že se jedná o nesprávný počet atomů vodíku v molekule vody.
Podle jeho názoru byl na atom kyslíku jeden atom vodíku. Při použití údajů chemiků Austin, že 20 procent vodíku a 80 procent dusíku je v amoniaku, vypočítá, jaká je relativní atomová hmotnost dusíku. S tímto výsledkem dospěl k zajímavému závěru. Ukázalo se, že relativní atomová hmotnost (vzorec amoniaku byl chybně přijat s jednou molekulou vodíku a dusíku) je čtyři. Ve svých výpočtech se vědec spoléhal na periodickou tabulku Mendelejeva. Podle analýzy vypočítal, že relativní atomová hmotnost uhlíku je 4,4, místo dříve přijatých dvanácti.
Ad
 Navzdory vážným selháním byl Dalton nejprve vytvořen stůl některých prvků. Během života vědce prošla opakovanými změnami.
Navzdory vážným selháním byl Dalton nejprve vytvořen stůl některých prvků. Během života vědce prošla opakovanými změnami.
Izotopová složka látky ovlivňuje přesnost relativní atomové hmotnosti
Při zvažování atomových hmotností prvků lze poznamenat, že přesnost každého prvku je odlišná. Například u lithia se jedná o čtyřmístnou číslici a u fluoru osmimístné. 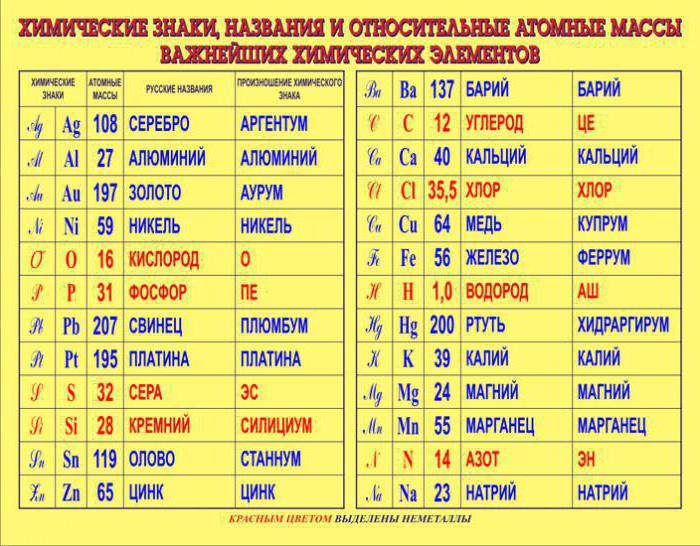 Problém spočívá v tom, že izotopová složka každého prvku je vlastní a není trvalá. Například u obyčejné vody existují tři typy izotopů vodíku. Tito, kromě obvyklého vodíku, zahrnují deuterium a tritium.
Problém spočívá v tom, že izotopová složka každého prvku je vlastní a není trvalá. Například u obyčejné vody existují tři typy izotopů vodíku. Tito, kromě obvyklého vodíku, zahrnují deuterium a tritium.
Relativní atomová hmotnost izotopů vodíku je dva a tři. "Těžká" voda (tvořená deuterem a tritiem) se zhoršuje. Proto ve stavu výparů jsou vodní izotopy menší než v kapalném stavu.
Ad
Selektivita živých organismů na různé izotopy
Živé organismy mají selektivní vlastnost vůči uhlíku. Pro výrobu organických molekul se používá uhlík s relativní atomovou hmotností dvanácti. Proto látky organického původu, stejně jako množství minerálů, jako je uhlí a olej, obsahují méně izotopové složky než anorganické materiály.
Mikroorganismy, které zpracovávají a hromadí síru, opouštějí izotopy síry 32. V oblastech, kde se bakterie netvoří, je podíl izotopu síry 34, což je mnohem vyšší. Právě na základě poměru síry v horninách půdy dospějí geologové k závěru o povaze původu vrstvy - ať už má magmatickou povahu nebo sedimentární.
Ze všech chemických prvků nemá jediný žádný izotop - fluor. Proto je jeho relativní atomová hmotnost přesnější než ostatní prvky.
Existence povahy nestabilních látek
Některé prvky mají relativní hmotnost v hranatých závorkách. Jak vidíte, jsou to prvky umístěné po uranu. Faktem je, že nemají stabilní izotopy a rozpadu s uvolněním radioaktivního záření. Nejstabilnější izotop je proto uveden v závorkách. 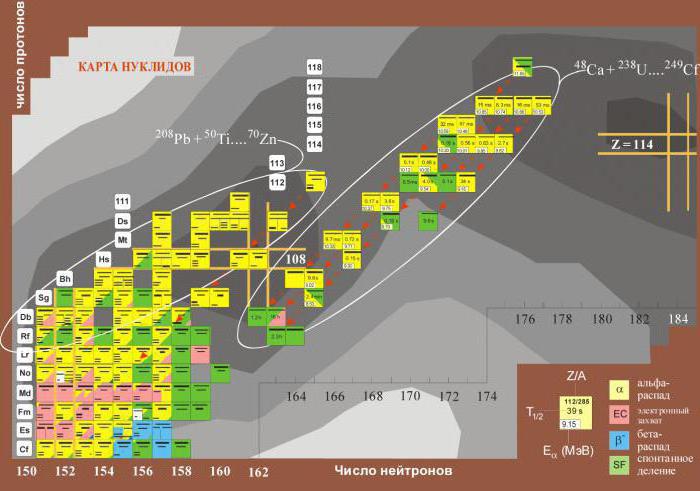 Časem se ukázalo, že někteří z nich mohou mít za umělých podmínek stabilní izotop. V periodické tabulce Mendelejev bylo nutné změnit atomové hmotnosti některých transuranických prvků.
Časem se ukázalo, že někteří z nich mohou mít za umělých podmínek stabilní izotop. V periodické tabulce Mendelejev bylo nutné změnit atomové hmotnosti některých transuranických prvků.
V procesu syntézy nových izotopů a měření jejich délky života bylo někdy možné detekovat nuklidy s poločasem života milionů krát delším.
Věda nehybně stojí, objevují se nové prvky, zákony, vzájemné vztahy různých procesů v chemii a přírodě. Proto v jaké formě se chemie a periodický systém Mendeleevových chemických prvků objeví v budoucnosti, za sto let, je nejasný a nejistý. Ale chci věřit tomu, že práce chemiků nahromaděných v minulých stoletích budou sloužit novém dokonalým znalostem našich potomků.