Radioaktivní chemický prvek. Umělý radioaktivní prvek
Až do konce 19. století se všechny chemické prvky zdály trvalé a nedělitelné. Neexistovala otázka, jak převést neměnné prvky. Zjišťování radioaktivity však obrátilo svět, o kterém jsme se dozvěděli, a vydláždila cestu k objevování nových látek.
Objevování radioaktivity
Čest objevu přeměny prvků má francouzský fyzik Antoine Becquerel. Pro jednoho chemické zkušenosti potřeboval krystaly uranyl-síran draselný. Omotal látku v černém papíru a sáček položil v blízkosti fotografické desky. Po vývoji filmu vědec viděl obrysy uranylových krystalů na obraze. Přes tlustou vrstvu papíru byly jasně odlišitelné. Becquerel několikrát opakoval tento experiment, ale výsledek byl stejný: obrysy krystalů obsahujících uran byly na fotografických deskách jasně viditelné.
Ad
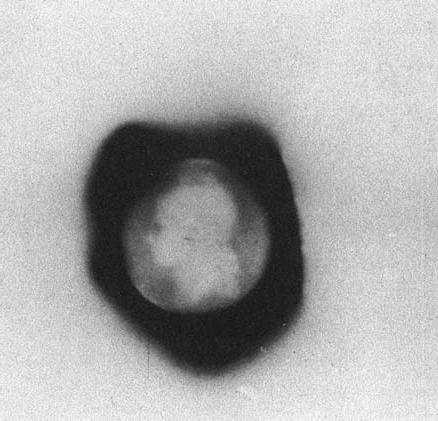
Výsledky zjištění Becquerel oznámil na příští schůzi, kterou uspořádala Pařížská akademie věd. Jeho zpráva začala slovy "neviditelné záření". Takže popsal výsledky svých experimentů. Poté pojem záření začal používat fyzici.
Curie experimenty
Výsledky pozorování Becquerela zaujaly francouzští vědci Marie a Paul Curie. Správně usoudili, že nejen uran může mít radioaktivní vlastnosti. Vědci si všimli, že zbytky rudy, ze kterých je tato látka extrahována, jsou stále vysoce radioaktivní. Vyhledání prvků, které se liší od původních, vedlo k objevení látky s vlastnostmi podobnými uranu. Nový radioaktivní prvek získal jméno polonium. Takové jméno Marie Curie dali látku na počest své vlasti - Polsko. Následně bylo objeveno rádio. Radioaktivní prvek byl produktem rozpadu čistého uranu. Poté se v chemii začala nová éra, která se dříve nestala v přírodě. chemikálie.
Ad
Položky
Většina současně známých jader chemických prvků je nestabilní. Časem se takové sloučeniny spontánně rozpadají na další prvky a různé drobné částice. Vyšší rodičovský prvek v komunitě fyziků se nazývá zdrojový materiál. Výrobky vzniklé během rozkladu látky se označují jako děti nebo rozkladné produkty. Samotný proces je doprovázen uvolňováním různých radioaktivních částic.
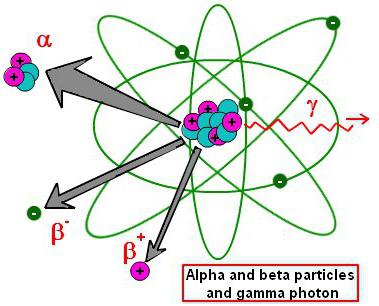
Izotopy
Nestabilita chemických prvků lze vysvětlit existencí různých izotopů stejné látky. Izotopy jsou variace některých prvků periodického systému se stejnými vlastnostmi, ale s různým počtem neutronů v jádře. Mnoho běžných chemických látek má alespoň jeden izotop. Skutečnost, že tyto prvky jsou široce distribuovány a dobře studovány, potvrzuje, že jsou ve stabilním stavu po delší dobu. Ale každý z těchto "dlouhých" prvků obsahuje izotopy. Jejich vědci produkují jádra během laboratorních reakcí. Umělé radioaktivní elementy vyrobené syntetickým způsobem nemohou dlouhodobě existovat ve stabilním stavu a časem se rozpadají. Tento proces může probíhat třemi způsoby. Názvem elementárních částic, které jsou vedlejšími produkty termonukleární reakce, se dostaly jména všech tří typů rozkladu.
Ad
Alfa rozpad
Radioaktivní chemický prvek se může přeměnit podle prvního režimu rozpadu. V tomto případě je alfa částic, jehož energie dosáhne 6 milionů eV, vysunutá z jádra. Podrobná studie výsledků reakce ukázala, že tato částice je atom helia. Z jádra se odebírají dva protony, takže výsledný radioaktivní prvek bude mít v periodickém systému atomové číslo ve dvou polohách nižší než v mateřské látce.
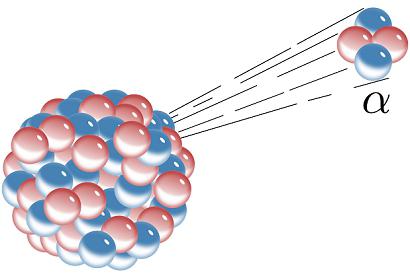
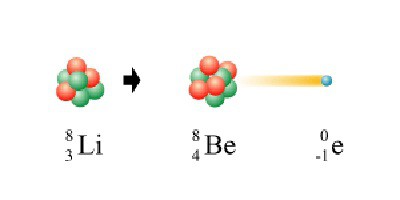
Beta rozpad
Reakce beta rozkladu je doprovázena emisí jednoho elektronu z jádra. Vzhled této částice v atomu je spojen s rozpadem neuronu na elektron, proton a neutrino. Jak elektron opouští jádro, radioaktivní chemický prvek zvyšuje jeho atomové číslo o jednu jednotku a stává se těžší než jeho mateřský.
Gamma rozpad
Při rozpadu gama jádro vysílá fotonový paprsek s různými energiemi. Tyto paprsky se nazývají gama záření. V tomto procesu není radioaktivní prvek upraven. Jen ztrácí energii.
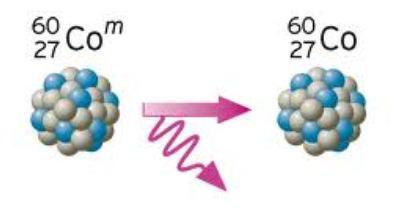
Samo o sobě nestabilita, kterou má radioaktivní prvek, vůbec neznamená, že s určitým množstvím izotopů najednou zmizí naše substance a uvolní obrovskou energii. Ve skutečnosti rozpad jádra připomíná vaření popcornů - chaotický pohyb kukuřičných jader v pánvi a je zcela neznámé, které z nich budou odhaleny jako první. Zákon radioaktivní rozpadové reakce může zaručit pouze to, že po určitou dobu bude počet částic, úměrný počtu nukleonů zbývajících v jádru, vyletět z jádra. V jazyce matematiky lze tento proces popsat následujícím způsobem:
Ad
dN = λNdt.
Zde na obličeji je poměrná závislost počtu nukleonů dN opouštějících jádro v období dt, na počtu všech nukleonů přítomných v jádru N. Koeficient λ je konstanta radioaktivity rozkládající se látky.
Počet nukleonů zbývajících v jádru v čase t je popsán vzorcem:
N = N0e-ml ,
kde N 0 je počet nukleonů v jádru na začátku pozorování.
Například radioaktivní element halogen s atomovým číslem 85 byl objeven teprve v roce 1940. Jeho poločas je poměrně dlouhý - 7,2 hodiny. Obsah radioaktivního halogenu (astatinu) na celé planetě nepřesahuje jeden gram čisté látky. Takže za 3,1 hodiny by jeho teoretické množství mělo být teoreticky sníženo na polovinu. Avšak konstantní procesy rozkladu uranu a thoria způsobují vznik nových a nových atomů astatinu, i když ve velmi malých dávkách. Proto jeho množství v přírodě zůstává stabilní.
Poločas
Konstanta radioaktivity slouží k určení, jak rychle se rozpadne studovaný prvek. Pro praktické problémy ale fyzikové často používají množství, které se nazývá poločas rozpadu. Tento indikátor udává, jak dlouho substance ztratí přesně polovinu nukleonů. U různých izotopů se toto období liší od drobných frakcí sekundy až po miliardy let.
Ad
Je důležité si uvědomit, že čas v této rovnici se nezvyšuje, ale násobí. Například, pokud během nějaké doby, kdy látka ztratila polovinu nukleonů, pak v průběhu 2t ztratí další polovinu zbytku - tedy čtvrtinu původního počtu nukleonů.
Vznik radioaktivních prvků
Radioaktivní látky se samozřejmě vytvářejí v horní atmosféře Země, v ionosféře. Při působení kosmického záření se plyn ve vysoké nadmořské výšce podrobuje různým změnám, které přeměňují stabilní látku na radioaktivní prvek. Nejvíce obyčejný plyn v naší atmosféře je N 2 , například ze stabilního izotopu, dusík-14 je přeměněn na radioaktivní izotop uhlík-14.
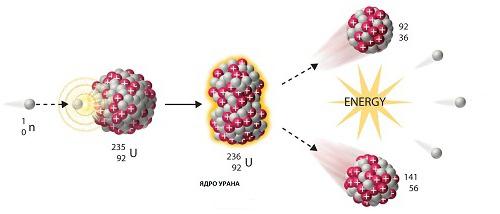
V dnešní době vzniká mnohem častěji radioaktivní prvek v řetězci člověkem vyvolaných reakcí atomového štěpení. Toto je název procesu, v němž se jádro mateřské látky rozdělí na dvě dceřiné společnosti a poté na čtyři radioaktivní vnoučata. Klasickým příkladem je izotop uranu 238. Jeho poločas je 4,5 miliardy let. Téměř tolik naší planety existuje. Po deseti stádiích rozkladu se radioaktivní uran přeměňuje na stabilní olovo 206. Uměle získaný radioaktivní prvek se ve svých vlastnostech neliší od jeho přirozeného protějšku.
Praktický význam radioaktivity
Po katastrofě v Černobylu mnozí mluvili vážně o potlačení rozvojových programů. jaderné elektrárny. Z hlediska domácí, radioaktivita přináší lidstvu obrovské výhody. Studium možností jeho praktického využití se zabývá vědou radiografie. Například radioaktivní fosfor se pacientovi podává, aby získal úplný obraz zlomenin kostí. Jaderná energie také slouží k výrobě tepla a elektřiny. Možná v budoucnosti čekáme na nové objevy v této úžasné oblasti vědy.