Kyselina sírová a její chemické vlastnosti
Kyseliny jsou chemické sloučeniny sestávající z atomů vodíku a zbytků kyselin, například SO4, SO3, PO4 atd. Jsou to anorganické a organické. První zahrnují kyselinu chlorovodíkovou, fosforečnou, sulfidovou, dusičnou a kyselinu sírovou. K druhému - octovému, palmitovému, formickému, stearovému, atd.
Co je kyselina sírová?
Tato kyselina se skládá ze dvou atomů vodíku a zbytku kyseliny S04. Má vzorec H2SO4. 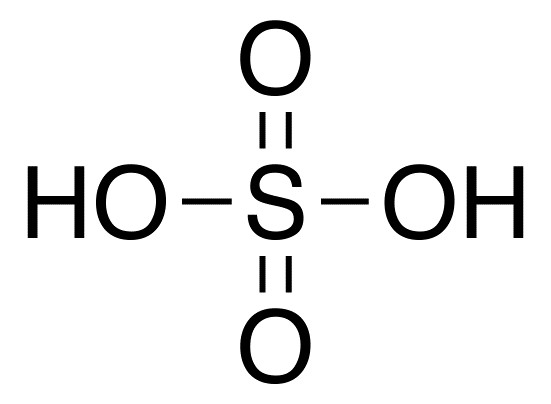 Kyselina sírová nebo, jak se také nazývá sulfát, označuje anorganické kyslíkaté dibázické kyseliny. Tato látka je považována za jednu z nejagresivnějších a chemicky aktivních látek. Ve většině chemických reakcí působí jako oxidační činidlo. Tato kyselina může být použita v koncentrované nebo zředěné formě, v těchto dvou případech má mírně odlišné chemické vlastnosti.
Kyselina sírová nebo, jak se také nazývá sulfát, označuje anorganické kyslíkaté dibázické kyseliny. Tato látka je považována za jednu z nejagresivnějších a chemicky aktivních látek. Ve většině chemických reakcí působí jako oxidační činidlo. Tato kyselina může být použita v koncentrované nebo zředěné formě, v těchto dvou případech má mírně odlišné chemické vlastnosti.
Fyzikální vlastnosti
Kyselina sírová v normálních podmínkách má kapalný stav, její teplota varu je asi 279,6 stupňů Celsia, bod zmrznutí, když se změní na tuhé krystaly, je asi -10 stupňů pro sto procent a asi -20 pro 95 procent.  Čistá sto procent síranové kyseliny je mastná, bez zápachu a bezbarvá kapalná látka, která má téměř dvakrát tolik hustoty než voda - 1840 kg / m3.
Čistá sto procent síranové kyseliny je mastná, bez zápachu a bezbarvá kapalná látka, která má téměř dvakrát tolik hustoty než voda - 1840 kg / m3.
Chemické vlastnosti kyseliny síranové
Kyselina sírová reaguje s kovy, jejich oxidy, hydroxidy a solemi. Zředěná vodou v různých poměrech, může se chovat jinak, proto se podrobněji zabýváme vlastnostmi koncentrovaného a slabého roztoku kyseliny sírové odděleně.
Koncentrovaný roztok kyseliny sírové
Koncentrovaný roztok je roztok obsahující 90% kyseliny sírové. Takové řešení kyseliny sírové je schopno reagovat i s nízkoaktivními kovy, stejně jako s nekovy, hydroxidy, oxidy, solemi. Vlastnosti takového roztoku kyseliny sírové jsou podobné jako koncentrovaná kyselina dusičná. 
Interakce s kovy
Při chemické reakci koncentrovaného roztoku kyseliny sírové s kovy umístěnými napravo od vodíku v elektrochemické řadě kovových napětí (tj. Nikoliv nejaktivnější) se vytvářejí tyto látky: síran kovu, se kterým dochází k interakci, voda a oxid siřičitý. Měď (měďnatý), rtuť, vizmut, stříbro (argentum), platina a zlato (aurum) jsou kovy, které jsou výsledkem interakcí, se kterými se vytvářejí uvedené látky.

Interakce s neaktivními kovy
S kovy, které jsou na levé straně vodíku v sérii napětí, koncentrovaná kyselina sírová se chová trochu jinak. V důsledku takové chemické reakce se vytvářejí následující látky: specifický sulfát kovu, sirovodík nebo čistá síra a voda. Železo (ferum), hořčík, mangan, beryllium, lithium, baryum, vápník a všechny ostatní v řadě napnutí nalevo od vodíku kromě hliníku, chromu, niklu a titanu - jsou také koncentrovány kovy; kyselina sírová nereaguje.
Interakce s nekovy
Tato látka je silným oxidačním činidlem, a proto je schopná podílet se na redoxních chemických reakcích s nekovy, jako je například uhlík (uhlík) a síra. V důsledku takových reakcí je nutně voda uvolněna. Přidání této látky k uhlíku také uvolňuje oxid uhličitý a oxid siřičitý. A pokud přidáte kyselinu k síře, dostaneme pouze oxid siřičitý a vodu. Při takové chemické reakci hraje síranová kyselina úlohu oxidačního činidla.
Interakce s organickými látkami
Mezi reakcemi kyseliny sírové a organické látky lze charging rozlišit. Takový proces nastává, když se daná látka srazí s papírem, cukrem, vlákny, dřevem atd. V každém případě se uvolňuje uhlík. Uhlík, který vznikl během reakce, může částečně interagovat s kyselinou sírovou, když je v přebytku. Na obrázku je reakce cukru s roztokem kyseliny sírové průměrné koncentrace.

Reakce se solemi
Koncentrovaný roztok H2SO4 také reaguje se suchými solemi. V tomto případě dochází k standardní výměnné reakci, při které se tvoří sulfát kovu, který je přítomen ve struktuře soli, a kyselinou se zbytkem, který byl ve složení soli. S roztoky solí však koncentrovaná kyselina sírová nereaguje.
Interakce s jinými látkami
Také tato látka může reagovat s oxidy kovů a jejich hydroxidy, v těchto případech dochází k výměnným reakcím, v prvním se uvolní síran kovu a voda, v druhém - stejný.
Chemické vlastnosti slabého roztoku kyseliny sírové
Zředěná kyselina sírová reaguje s mnoha látkami a má stejné vlastnosti jako všechny kyseliny. Na rozdíl od koncentrovaných látek interaguje pouze s aktivními kovy, tedy s těmi, které jsou vlevo od vodíku v řadě namáhání. V tomto případě dochází ke stejné substituční reakci jako v případě jakékoliv kyseliny. Toto uvolňuje vodík. Takový roztok kyseliny reaguje také se solnými roztoky, v důsledku čehož dochází k výměnné reakci, která již byla diskutována výše, s oxidy - a rovněž koncentrovanými, s hydroxidy - také stejným způsobem. Kromě běžných sulfátů existují také hydrosulfáty, které jsou výsledkem interakce hydroxidu a kyseliny sírové.

Jak znát, že roztok obsahuje kyselinu sírovou nebo sulfáty
Chcete-li zjistit, zda jsou tyto látky přítomné v roztoku, speciálně kvalitní odpověď na síranové ionty, což vám umožňuje vědět. Spočívá v přidání bária nebo jeho sloučenin do roztoku. V důsledku toho může vypadat bílá sraženina. (síran barnatý), což naznačuje přítomnost sulfátů nebo kyseliny sírové.
Jak extrahovat kyselinu sírovou
Nejběžnější metodou průmyslové výroby této látky je extrakce z pyritického železa. Tento proces se vyskytuje ve třech stádiích, u kterých probíhá specifická chemická reakce. Zvažte je. Nejprve se k pyritu přidá kyslík, což vede k tvorbě oxidu železitého a oxidu železitého oxid siřičitý, který se používá pro další reakce. Tato interakce nastává při vysokých teplotách. Následuje stupeň, ve kterém se oxid sírový získá přidáním kyslíku v přítomnosti katalyzátoru, kterým je oxid vanadia. Nyní se v posledním stupni přidá voda k získané látce a získají se sulfátové kyseliny. Jedná se o nejběžnější způsob komerční produkce kyseliny sulfátové, používá se nejčastěji proto, že pyrite je nejvíce snadno dostupný surovina vhodná pro syntézu látky popsané v tomto článku. Kyselina sírová získaná tímto způsobem se používá v různých průmyslových odvětvích, chemických i mnoha dalších, rafinace ropy obohacování rud, atd. Také je často používáno v technologii výroby sady syntetických vláken.