Druhý zákon termodynamiky. Interpretace, teoretické a praktické zdůvodnění
Ve fyzice, protože je to přesná věda, většina dogmů je empiricky prokázána. Tak byl odvozen druhý termodynamický zákon, který se v současné době zkoumá ve všech školách. Nevratné tepelné procesy - to je to, co říká. Je třeba poznamenat, že v počátečních fázích studie je takový výklad mnohem srozumitelnější.
Obecné pohledy
Fyzikální princip, který omezuje směr různých procesů termodynamické systémy je druhým zákonem termodynamiky. Definice tohoto termínu vznikla v 19. století, nejprve Rudolfem Clausisem a poté Williamem Thomsonem (lordem Kelvinem). Podle dvou postulátů na světě nemůže existovat jakýsi druh věčného pohybu druhého druhu. Neexistuje a nebude taková instalace, která by se ohřívala, vycházela ze všech věcí, živých bytostí a jevů, se proměnila v energii pro svou trvalou práci. Na základě toho bylo pravidlo odvozeno, že účinnost nemůže být stejná jako jedna. To lze porovnat s provozem chladničky, kde se teplota, například, rovná absolutní nula. Za takových podmínek je vyloučena kruhová výměna tepla. 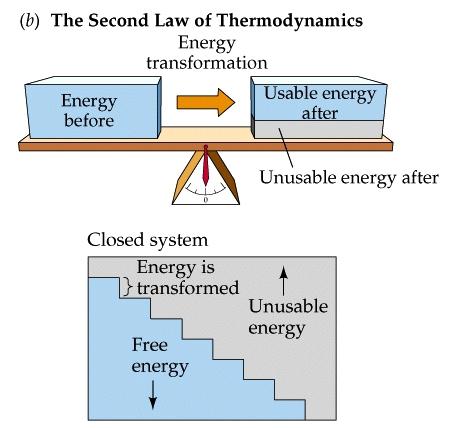
Formulace Rudolfa Clausise
První vyslovil druhou termodynamický zákon R. Clausis - německý fyzik a matematik. Podle něj je kruhový proces, při kterém je dosaženo výsledku přenosem tepla z méně ohřátého těla na ohřívanější. Jinými slovy, teplota v plném rozsahu nebo částečně se může volně pohybovat od teplejšího těla k chladnějšímu, ale tento proces nemůže nastat v opačném směru. To nám jasně ukazuje nepřítomnost cyklickosti, začarovaného kruhu. Takové pojmy jsou pro termodynamiku nepřijatelné. Teplo je prostě vyměňováno mezi těly a v důsledku těchto akcí se nevytváří žádná nadměrná energie. 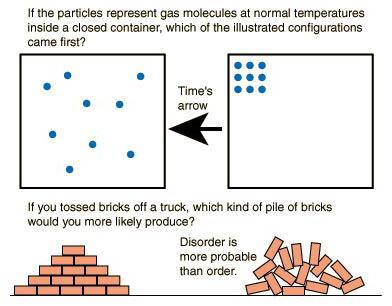
Postulát odvozený lordem Kelvinem
Podobná definice druhého zákona o termodynamice získaná ve spisech Thomsona - britského fyzika a mechaniky. Teoreticky to zní takto: "Cyklický proces, jehož jediným výsledkem může být práce získaná chlazením teplého těla nebo nádrže, je nemožné." Abychom pochopili tuto interpretaci jasněji, představme si určitý stroj (nemůže existovat podle termodynamického postulátu). Pravidelně chladí nádrž neustále horkou vodou, kterou získává z této tepelné energie. Díky této energii stroj zvedá různé zatížení jako stavební jeřáb. V tomto případě není žádný motor, elektrárny a jiné mechanické náplně. Z hlediska empirické fyziky to není možné. 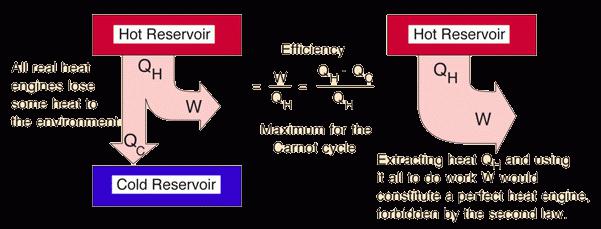
Co je běžné?
Nyní budeme zvažovat, jak jsou tyto dva interpretace kombinovány a na které se v zásadě zakládá druhý zákon termodynamiky. Entropie je měřítkem chaosu, který se zvyšuje v procesu výměny tepla. To je spojovací prvek pro popis Clausis a Kelvina. Ale trochu zpátky. Druhý termodynamický zákon říká, že při výměně tepla se energie snižuje (proto není možné získat práci), ale míra chaosu se zvyšuje. Tento proces je nevratný a často se nazývá spontánní. V termodynamice se entropie neustále rozmnožuje, ale její zničení je nemožné. To je důvod, proč ani 100 procent energie, která je v jakémkoli těle, nemůže být přeměněna na práci. 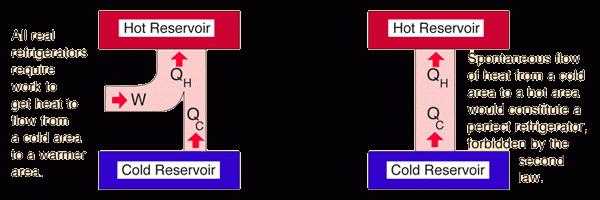
Jaká je míra chaosu?
Koncept entropie byl nejprve formulován ústy Clausis. Byl použit k určení míry nevratného procesu rozptýlení energie. Byla to určitá změna v odchylce skutečného procesu od ideálu. Entropie v uzavřených systémech, kde se všechny procesy vyskytují cyklicky, má konstantní hodnotu. Pokud je proces nevratný (což se týká termodynamiky), pak má entropie vždy pozitivní význam. Je také třeba poznamenat, že měřítko chaosu je generováno absolutně všemi procesy, které se vyskytují ve vesmíru. S konstantními ukazateli objemu a energie těla nebo nádrže se entropie neustále zvyšuje. Pokud se tyto číselné údaje mění periodicky, může být míra chaosu snížena kvůli práci, která se dělá, ale jeho úplné zničení není možné. Mělo by být poznamenáno, že entropie vesmíru neklesá. Zůstává buď normální, nebo trvale se zvyšuje.
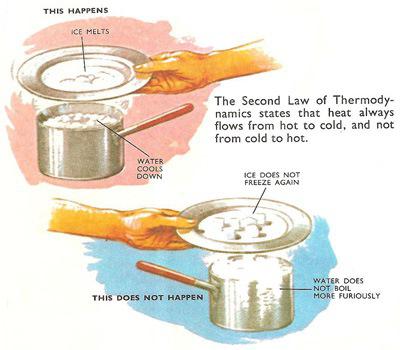
Ilustrativní příklad
Druhý termodynamický zákon lze vysvětlit standardním příkladem, který se často dává studentům. Máme dvě těla s různými teplotami. Čím víc zahřátá látka vydává teplo méně zahřáté, dokud se jejich hodnoty teploty nezmění. Během tohoto procesu se entropie prvního, teplejšího těla sníží o menší číslo, než se bude zvyšovat u druhého, chladnějšího těla. V důsledku toho takový spontánní proces vytvoří entropii systému, jehož index bude vyšší než celková hodnota entropie dvou těles v počáteční poloze. Jinými slovy, zvýšila se chaosová míra systému dvou látek, která vznikla v důsledku výměny tepla. 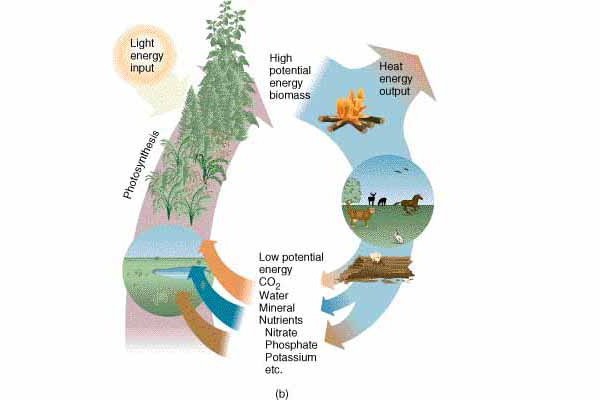
Termální smrt vesmíru
Když Clausis uskutečnil své vyšetřování, dospěl k závěru, že bez ohledu na to, jak otevřený prostor nám připadá (naše planeta, její samostatná území, vodní plochy apod.), To vše je ve vesmíru. Vesmír je naopak největším uzavřeným prostorem, ve kterém probíhají makroskopické procesy. Vzhledem k tomu, že v uzavřeném systému entropie neustále zvyšuje svůj index, náš svět se blíží skutečnosti, že brzy v něm míra chaosu dosáhne nekonečné hodnoty. To znamená, že všechny procesy se jednoduše zastaví kvůli tomu, že je energie vyčerpána. Takový kritický bod, kterému se v určité budoucnosti dostaneme, dostalo jméno termální smrti. Ukazuje se, že všechny naše akce (pohyby, chůze, běh), všechny jevy, které se na planetě vyskytují (příval větru, tsunami, pohyb litosférických desek) - to vše způsobuje nezvratné zvýšení entropie a vyčerpává energii.
Odmítnutí teorie
Člověk stále nemůže posuzovat celý vesmír. Vidíme jen část světa, ve kterém žijeme, a prozkoumáme tento koutek, prokazujeme určité zákony a na základě toho vytváříme vlastní myšlenky. Proto první vyvrácení možnosti tepelné smrti, založené na druhém termodynamickém zákonu, spočívá v tom, že vesmír nemusí být uzavřený systém. Je jisté, že 85 procent vesmíru tvoří antihmoty, jejichž vlastnosti nikdo nezná. Druhým vyvrácením je, že náš vesmír, i když je uzavřen, je nepřetržitý výkyv. Vzhledem k různým výkyvům a změnám ve velikosti, hmotnosti, energii a teplotě se entropie nezvyšuje (v celkové, univerzální hodnotě) a nesníží se. V důsledku toho jsme již ve stavu termodynamické rovnováhy nebo ve slovech Clausis ve stavu tepelné smrti.
Shrnutí
Druhý termodynamický zákon je neoddělitelně spojen s vývojem přesných věd. Bylo otevřeno na počátku vědeckého a technického pokroku a stalo se východiskem pro další práci vědců v oblasti matematiky, fyziky a astronomie. Je třeba poznamenat, že to všechno reprezentujeme zejména v suchozemských podmínkách. Je pravděpodobné, že v jiném prostředí, kde gravitační pole mají jinou sílu, funguje termodynamika podle zcela jiného schématu.