Karbid hliníku: používá
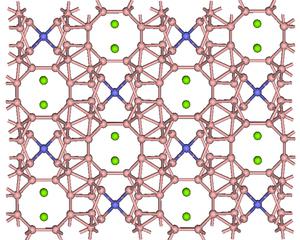
Chemická sloučenina vzorce Al4C3 se nazývá karbid hliníku. Jeho vzhled je reprezentován nažloutnou krystaloidní látkou. Sloučenina je velmi odolná vůči vnějšímu prostředí, teplota tání alumokarbidu je 1400 ° C a relativní hustota je 2,36 g / cm3. Mřížka Al4C3 je složitá a obsahuje atomy uhlíku. Vystupují tam jako anionty. Karbid hliníku, stejně jako jiné anorganické sloučeniny, má mnoho využití. Tato látka patří do první skupiny, jejíž rozdíl spočívá v nezměněné valence typické pro kov v normě.
Karbid hliníku: získání látky

Látka může být získána spojením kovu s uhlíkem, který musí být umístěn v obloukové peci. Složené karbid vápníku tam je také mírný obsah Al содержаниеC3. Při příjmu elektrolytů je sloučenina produktem koroze grafitu. Reakce oxidu hlinitého s uhlíkem vytváří Al4C3. Dalším způsobem získání této látky je současná kalcinace koksu a hliníku při teplotě 1800 ° C. Vyrábí se speciálně vyškolenými pyrotechnikami a chemikáliemi. Nemůžete se snažit získat karbid hliníku doma, stejně jako v laboratořích, které nejsou pro tento účel určeny.
Fyzikální a chemické vlastnosti
Hlavní vlastností látky je její schopnost interagovat s vodou, kyslíkem a hydroxid sodný. Kromě toho se karbid hliníku může tavit, lámat a rozpouštět. Má entalpii tvorby ΔH = -209 (S = 88,95), energie Gibbs = -196 t, molární tepelná kapacita = 116,8. Index lomu karbid hliníku = 2,7 na 20 stupňů. Al4C3 může přicházet do styku s mnoha chemickými prvky, vytvářejícími dobře známé sloučeniny potřebné v průmyslu. Příkladem je zemní plyn - metan. Může být dosaženo smícháním karbidu hliníku s vodou. V tomto případě působí H 2 O jako rozpouštědlo pro kov, v důsledku čeho se hlavní sloučenina rozkládá.
Aplikace karbidu hliníku
 Al4C3 se používá v různých odvětvích průmyslu. Při výrobě alumokarbidu s grafitovými částicemi se vytváří velmi silný materiál. Nástroje, které tvoří tuto sloučeninu, mají stejnou tvrdost jako topaz. Obvykle se alumokarbid přidává k řezání předmětů používaných na obráběcích strojích, lékařských zařízeních atd. Kromě toho je tato sloučenina nezbytným materiálem v pyrotechnice. Byl používán v této oblasti po dlouhou dobu a zatím nebyl nahrazen. Zde je k výrobě jisker nezbytný alumokarbid. Jeho přítomnost v pyrotechnických dílech závisí na tom, proč a v jakém množství se prášek používá. Další aplikací látky je chemický průmysl, kde je sloučenina nezbytná pro tvorbu různých produktů, zejména organických plynů.
Al4C3 se používá v různých odvětvích průmyslu. Při výrobě alumokarbidu s grafitovými částicemi se vytváří velmi silný materiál. Nástroje, které tvoří tuto sloučeninu, mají stejnou tvrdost jako topaz. Obvykle se alumokarbid přidává k řezání předmětů používaných na obráběcích strojích, lékařských zařízeních atd. Kromě toho je tato sloučenina nezbytným materiálem v pyrotechnice. Byl používán v této oblasti po dlouhou dobu a zatím nebyl nahrazen. Zde je k výrobě jisker nezbytný alumokarbid. Jeho přítomnost v pyrotechnických dílech závisí na tom, proč a v jakém množství se prášek používá. Další aplikací látky je chemický průmysl, kde je sloučenina nezbytná pro tvorbu různých produktů, zejména organických plynů.
Co je metan?
Tato sloučenina patří do skupiny organických, ve struktuře jde o jednoduchý uhlovodík a má vzorec CH4. Metan reaguje málo s vodou, je bez zápachu a bezbarvý. Plyn patří do skupiny alkanů, je dostatečně odolný vůči účinkům různých látek chemické reakce. To je věřil, že metan není nebezpečné pro lidské zdraví, nicméně, někteří vědci argumentují opakem. Lidé, kteří mají stálý kontakt s plynem, mají změny v centrálním nervovém systému. Metan je výbušný, proto je v průmyslové výrobě nutné pečlivě sledovat jeho koncentraci ve vzduchu. Vzhledem k tomu, že plyn je bez zápachu, je obtížné zaznamenat únik. Z tohoto důvodu jsou v podniku instalovány speciální snímače, které zaznamenávají svou úroveň.
Způsoby, jak získat metan
 Vzhledem k tomu, že plyn je přírodní sloučenina, není vždy vyrobena laboratoří. Metan se vyrábí za anaerobních podmínek, což je výsledkem fermentačních procesů v bažinách, ve střevech zvířat a příliš mokré zemi. Podle vědců jedna z nich Saturnovy měsíce obsahuje tekuté směsi obsahující tento plyn na svém povrchu. Také metan je jednou ze složek atmosféry velkých planet. Nejvyšší obsah metanu se pozoruje v přírodních, důlních a bažinových plynech. V průmyslových podmínkách se plyn vyrábí hydrogenací a koksováním uhlí.
Vzhledem k tomu, že plyn je přírodní sloučenina, není vždy vyrobena laboratoří. Metan se vyrábí za anaerobních podmínek, což je výsledkem fermentačních procesů v bažinách, ve střevech zvířat a příliš mokré zemi. Podle vědců jedna z nich Saturnovy měsíce obsahuje tekuté směsi obsahující tento plyn na svém povrchu. Také metan je jednou ze složek atmosféry velkých planet. Nejvyšší obsah metanu se pozoruje v přírodních, důlních a bažinových plynech. V průmyslových podmínkách se plyn vyrábí hydrogenací a koksováním uhlí.
Metan se vyrábí také v laboratořích. Jedním ze způsobů, jak ho získat, je zahřátí kyseliny octové a hydroxidu sodného (nebo vápna). Tato druhá látka je také spojena s acetátem v důsledku tavení, v důsledku čehož se také vytváří metan. Obě metody nevyžadují přítomnost vody. Třetím způsobem výroby plynu je hydrolýza, ke které je karbid hliníku vystaven. V tomto případě se methan vytváří rychleji. Způsob hydrolýzy je také levnější, protože nevyžaduje vystavení vysokým teplotám.
Aplikace karbidu hliníku v průmyslové chemii

Kromě hydrolýzy sloučeniny může být také použita jako činidlo. Takové použití karbidu hliníku je nezbytné k určení obsahu některých látek. Zejména je možné odhalit cenný plyn - trícium, které je přítomno ve vodě. Dále může být vyrobena kombinovaná sůl z karbidu hliníku. Získává se, jako metan, kombinací látky s vodou. Tato sůl se nazývá tetrahydrooxaluminát sodný. Tkaniny je nutné dodat barvě. Výroba a použití karbidu je pro různé průmyslové odvětví velmi důležité, takže náklady na jeho získání jsou poměrně velké. Finanční prostředky na nákup látek jsou přidělovány státem.