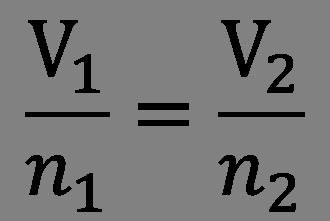Avogadroův zákon: popis a biografie vědce
Předvídat výsledky studie, předvídat vzorek, cítit společný původ - to všechno znamenalo práci velkého počtu experimentátorů a vědců. Nejčastěji se prognóza týká pouze oblasti zaměstnání výzkumného pracovníka. A málo má odvahu provádět dlouhodobé prognózy, což je výrazně předčasné. Italský Amedeo Avogadro měl dost odvahy. Z tohoto důvodu je tento vědec nyní znám po celém světě. A zákon Avogadro je stále používán všemi chemikami a fyziky na planetě. V tomto článku podrobně popíšeme o něm a jeho autora.
Dětství a studium
Amedeo Avogadro se narodil v Turíně v roce 1776. Jeho otec, Philippe, pracoval jako soudní pracovník. Celkově měla rodina osm dětí. Všichni předkové Amedeo sloužili jako právníci v katolické církvi. Mladík také neodcházel z tradice a začal se zabývat judikaturou. Ve věku dvacetiletého již získal doktorát.
Postupem času přestala právní praxe přitahovat Amedeo. Zájmy mladého muže ležely v jiné oblasti. Již v mládí chodil do školy experimentální fyziky a geometrie. Pak se v budoucnu probudil vědec lásky. Vzhledem k nedostatkům ve znalostech se společnost Avogadro zabývala sebevzděláváním. Ve věku 25 let Amedeo věnoval svůj volný čas studiu matematiky a fyziky.
Vědecké činnosti
V první fázi byla Amedeova vědecká práce věnována studiu elektrických jevů. Avogadrova zájem byl zvláště intenzivní poté, co Volt objevil zdroj elektrického proudu v 1800s. Neméně zajímavý byl i mladý vědec, diskuse o Volte a Galvani o povaze elektřiny. A obecně pak tato oblast pokročila ve vědě.
V letech 1803 a 1804 představil Avogadro a jeho bratr Felice dvě práce vědcům Turínské akademie, které odhalily teorie elektrochemických a elektrických jevů. V roce 1804 se Amedeo stal odpovídajícím členem této akademie.
V roce 1806 získal Avogadro práci v tureckém lycea. O tři roky později se vědec přestěhoval do lýcea v Vercelli, kde vyučoval matematiku a fyziku po dobu deseti let. V té době Amedeo četl hodně vědecké literatury a získal užitečné výňatky z knih. Vedl je až do konce života. K dispozici bylo až 75 svazků po 700 stranách. Obsah těchto knih hovoří o všestrannosti zájmů vědce a o kolosální práci, kterou udělal.
Osobní život
Amedeo uspořádal rodinný život poměrně pozdě, když už jeho věk prošel třetím desítkem. Ve společnosti Vercelli se setkal s Annou di Giuseppe, která byla mnohem mladší než vědec. V tomto manželství se narodilo osm dětí. Nikdo z nich nechodil po stopách svého otce.
Avogadrov zákon a jeho důsledky
V roce 1808 Gay-Lussac (ve spolupráci s Humboldtem) formuloval princip volumetrických vztahů. Tento zákon stanovil, že poměr mezi objemy reakčních plynů lze vyjádřit primární čísla. Například 1 objem chloru, spojený s 1 objemem vodíku, dává 2 objemy chlorovodíku, atd. Tento zákon nic neudělal, poněvadž nejprve neexistoval žádný konkrétní rozdíl mezi pojmem tělesa, molekula a atomem a za druhé, vědci měli různá stanoviska ohledně složení částic různých plynů.
V roce 1811 zahájila Amedeo důkladnou analýzu výsledků výzkumu Gay-Lussac. V důsledku toho si Avogadro uvědomil, že zákon o objemových vztazích umožňuje porozumět struktuře molekuly plynu. Hypotéza, kterou formuloval, zní: "Počet molekul každého plynu ve stejném objemu je vždy stejný."
Objevování zákona
Tři roky vědec pokračoval v experimentování. V důsledku toho se objevil zákon Avogadro, který zní takto: "Stejné objemy plynných látek při stejné teplotě a tlaku obsahují stejný počet molekul. Míra hmotnosti molekul může být určena hustotou různých plynů. " Například pokud 1 litr kyslíku obsahuje tolik molekul jako 1 litr vodíku, tak poměr hustoty těchto plynů se rovná hmotnostnímu poměru molekul. Vědec také poznamenal, že molekuly v plynech nejsou vždy složeny z jediných atomů. Přítomnost různých a stejných atomů je přijatelná.
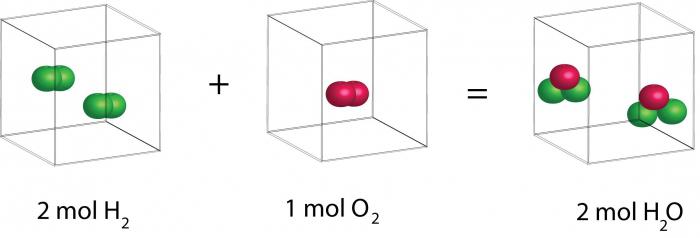
Bohužel, v době Avogadro, tento zákon nemohl být teoreticky prokázán. Ale umožnil v experimentech sestavit složení molekul plynu a určit jejich hmotnost. Sledujeme logiku takového uvažování. Během experimentu bylo zjištěno, že vodní pára z plynu, jakož i objemy vodíku a kyslíku korelují v poměru 2: 1: 2. Z této skutečnosti můžeme vyvodit různé závěry. První: molekula vody sestává ze tří atomů a molekuly vodíku a kyslíku dvě. Druhý závěr je také vhodný: molekuly vody a kyslíku jsou diatomické a vodík je monatomický.
Oponenti hypotézy
Avogadrovův zákon měl mnoho oponentů. To bylo částečně způsobeno skutečností, že v těchto dnech nebyl žádný jednoduchý a jasný záznam o rovnicích a vzorcích chemických reakcí. Hlavním nepřítelem byl Jens Berzelius, švédský chemik s nezpochybnitelnou autoritou. On věřil, že všechny atomy mají elektrické náboje a samotné molekuly jsou tvořeny atomy s protikladnými náboji, které se vzájemně přitahují. Takže atomy vodíku měly kladný náboj a atomy kyslíku měly negativní charakter. Z tohoto pohledu jednoduše neexistuje molekula kyslíku sestávající ze dvou stejně nabitých atomů. Ale jestliže jsou molekuly kyslíku stále monoatomické, pak při reakci dusíku s kyslíkem by poměr objemového poměru měl být 1: 1: 1. Toto tvrzení je v rozporu s pokusem, kdy bylo získáno 2 litry oxidu dusnatého z 1 litru kyslíku a 1 litru dusíku. Z tohoto důvodu Berzelius a další chemici odmítli zákon Avogadro. Koneckonců, není absolutně v souladu s experimentálními daty.
Obnova zákona
Před šedesátým devatenáctým stoletím se v chemii pozorovalo svévolnost. A rozšířila se jako hodnocení molekulové hmotnosti a na popis chemických reakcí. Tam bylo obecně mnoho mylných představ o atomovém složení komplexních látek. Někteří vědci dokonce plánovali opustit molekulární teorii. A až v roce 1858, chemik z Itálie nazvaný Cannizzaro nalezl v korespondenci mezi Berthollet a Ampere odkaz na Avogadrova zákon a její důsledky. To zjednodušilo složitý obraz chémie doby. O dva roky později Cannizzaro hovořil o zákonu Avogadro v Karlsruhe na Mezinárodním kongresu o chemii. Jeho zpráva zasáhla vědce nesmazatelný dojem. Jeden z nich řekl, že vypadá, že vidí jeho oči, všechny pochybnosti se odpařily a na oplátku se objevil pocit jistoty.
Po uznání zákona Avogadro vědci mohli nejen určit složení molekul plynu, ale také vypočítat atomovou a molekulovou hmotnost. Tato znalost pomohla při výpočtu hmotnostních poměrů činidel v různých chemických reakcích. A bylo to velmi pohodlné. Měřením hmotnosti v gramech by výzkumníci mohli pracovat s molekulami.

Závěr
Od objevování zákona Avogadro uplynula hodně času, ale nikdo nezapomněl na zakladatele molekulární teorie. Logika vědce byla bezchybná, což později potvrdily výpočty J. Maxwella založené na kinetické teorii plynů a pak experimentální studie (Brownian pohyb). Bylo také stanoveno, kolik částic je obsaženo v molu každého plynu. Tato konstanta - 6,022 • 1023 byla pojmenována Avogadrovo číslo trvalé jméno Amedeo.