Komplexní sloučeniny a jejich význam
Komplexní sloučeniny (CS) hrají důležitou roli v aktivitě živých organismů. Jsou také široce používány v průmyslu. Dnes zvažujeme jejich druhovou rozmanitost, aplikaci a historii studia.
Úvod do komplexních sloučenin
Komplexní sloučeniny jsou látky tvořené kombinací ligandu a komplexotvorného činidla. Hrát roli interagujících částic může atomy a ionty. A. Werner v roce 1893 představil teorii komplexních sloučenin světu, nazývaný také teorie koordinace.
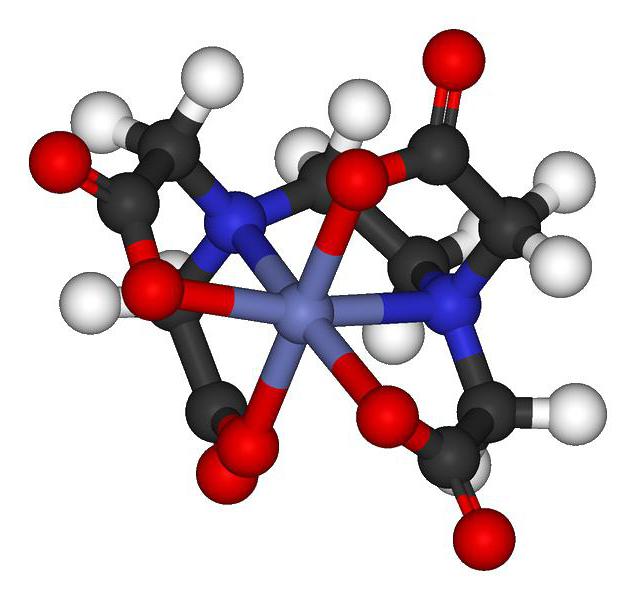
Přítomnost vnější koule a úplná disociace v roztoku vody do nízko disociačních kationtů a aniontů jsou charakteristické pro CS. Existují však některé druhy, které nemají vnější kouli, která jim neumožňuje rozpustit ve vodě. Tam je obrovské množství policajta.
Druhy sloučenin
Komplexní sloučeniny jsou rozděleny do tří hlavních typů:
- První typ, který se liší v komplexním náboji, zahrnuje kationtové komplexy, ve kterých jsou kolem neutronových molekul koordinovány pozitivní ionty. Druhý typ se nazývá aniontový komplex, ve kterém pozitivně oxidovaný atom působí jako komplexační činidlo a anionty jednoduchého nebo komplexního typu jsou ligandy. Třetí typ se nazývá neutrální komplex, byl vytvořen kvůli molekulární koordinaci kolem atomu, který má neutrální náboj.
- V závislosti na povaze ligandu se dělí na amonitany (amoniak - ligand), akvokomplexy (ligand - voda), hydroxokomplexy (ligandy - hydroxidové ionty), komplexy kyselin (ligandy - kyselé zbytky), karbonyly (ligandy - uhlíkové molekuly druhé valencie).
- V souladu s umístěním ligandů jsou monodentátové, bidentátové a polydentátové QS.
Historické informace
V roce 1893 se poprvé pokusil o vyčerpávající popis struktury ČS pomocí koordinační teorie Alfreda Wernera. Práce byla provedena předtím, než se objevila teorie elektronového valence a obvyklé chemické reakce přírody.

V jeho teorii Werner argumentoval, že sloučeniny anorganické povahy mají jádra složená z atomů tvořících komplex. Atomy obklopující komplexování se nazývají koordinace. Jsou uspořádány v souladu s tvarem jednoduchého polyhedronu. A. Werner předpokládal přítomnost koordinačního typu vazby ve společném elektronovém páru, který by atomům nebo molekulám dal dalšímu páru. Nicméně neexistence těchto sloučenin způsobila nedůvěru mezi chemickou komunitou. V důsledku toho se vědec v následujících dvou desetiletích snažil vytvořit potřebné látky, které by potvrdily jeho teorii.
Werner v roce 1911 syntetizoval přes čtyřicet molekul optického typu, který neobsahoval uhlíkové atomy, což nakonec změnilo názor chemických vědců na jeho teorii.
Alfred Werner získal v roce 1913 Nobelovu cenu za úspěchy v oblasti chemie.
Nomenklatura
Komplexní sloučeniny mají systém pro vytváření vlastních jmen, skládající se z pěti bodů:
- První je výrazný anion, pak kation.
- Složitá část začíná ligandem - anionem nacházejícím se ve vnitřní kouli a na konci je přidán "o".
- Monodentátní ligandy jsou označeny pomocí řečtiny: mono, di, tři, tetra, penta, hex (1, 2, 3, 4, 5, 6). Při práci s polydentátovými ligandy se používají tris, bis, tetrakis a další.
- Určete vnitřní kouli s jejími součástmi, jděte na vnější stranu.
- Komplexní činidlo částic s neutrálním komplexem je uvedeno v nominativním případě.
Informace o struktuře
Komplexní sloučeniny mají vnitřní sféru sestávající z řady iontů nebo molekul neutrální povahy, pevně spojených s komplexačním činidlem. Jsou nazývány ligandy. Vnitřní koule může mít tři typy náboje: "+", "-" nebo "0".
Vnější koordinační koule jsou ionty, které se nenacházejí v prostoru vnitřní koule.
Vazba mezi ligandem a centrálním iontem může být způsobena buď elektrostatickou přitažlivostí nebo donor-akceptorovým mechanismem.
Isomerismus v koordinačních sloučeninách je hlavní statistický aspekt. Pokud jde o izomerismus, znamenají různé vzájemné polohy v prostoru atomů nebo složek sloučeniny, což povede ke změně fyzikálních a chemických vlastností odpovídající sloučeniny - izomeru. CS isomerismus je strukturální, optický a prostorový.
Stereochemie
Komplexní sloučeniny spolu s organické látky Vysokými molekulárními sloučeninami syntetického nebo přírodního původu jsou hlavními předměty stereochemických studií. A. Werner je považován za jednoho z vědců, kteří rozvíjeli celou oblast výzkumu a oživili některé oblasti chemické činnosti. Stereochemie dodnes zůstává referenčním bodem pro koordinační chemický výzkum.
Některé vlastnosti a metody získání
Získání komplexních sloučenin má poměrně širokou škálu možností, ale tyto jsou častěji používané:
- Rozpuštění hydroxidů ve vodném amoniaku, které se nerozpouštějí ve vodě.
- Interakce amoniaku s kovovými solemi s komplexními vlastnostmi; častěji se jedná o kovy v sekundární podskupině.
- Interakce kyanidů nebo rhodanidů s kovy nebo solemi.
- Místnost je nerozpustná v H 2 O kovů amfoterního typu, a to jejich oxidy nebo hydroxidy v alkalickém roztoku.
- Komplexní kyseliny mohou být získány například reakcí zlata a vodního roztoku nebo hydroxidu draselného s kyselinou chlorovodíkovou.
Mnoho kvalitativních vlastností sloučenin závisí na jejich elektronických vlastnostech, takže barva CS může být určena komplexačním činidlem a ligandy. Energetické dělení na d-orbitálu umožňuje, aby se elektrony pohybovaly z dxz , dxy , d zy pod úrovní na podnášky s vyšším energetickým indexem d z 2 nebo d z 2 - y 2 . Tento jev je doprovázen absorpcí lehkých kvant. Velikost rozdílu mezi rozdělenými úrovněmi způsobuje absorpci světelných kvant s vlnovou délkou různých délek, která dává určitou barvu.
Komplexní sloučeniny mají také dva důležité magnetické vlastnosti, podle nichž jsou klasifikovány jako paramagnetické a diamagnetické. Paramagnetické komplexy mají své vlastní μ-momenty a z tohoto důvodu se do nich vkládají do vnějších elektromagnetických polí. Diamagnetický komplex nemá žádný magnetický moment, a proto magnetické pole spěchá, aby ho vytlačilo. Vlastnosti paramagnetické povahy jsou určeny přítomností elektronů, které ve své struktuře nemají dvojici.
Použití

Sloučeniny komplexního typu hrají jednu z nejdůležitějších rolí v jakémkoli organismu, například kyslík spárovaný s hemoglobinem v krvi se dodává O2 přes tělo do tkání a buněk; Chlorofyl uvnitř rostlin je také považován za komplex.
Použití komplexních sloučenin se v průmyslu široce používá. Pomocí chemických metod, které vyžadují tvorbu KS, jsou z rudy extrahovány kovy. Příklady zahrnují čisté železo, nikl a kobalt, které se získají tepelným rozkladem kovových karbonylů. Tyto složité látky, rozkládající se, emitují nezbytné kovy.

Analytická chemie může použít COP jako indikátory. Organická a anorganická syntéza může být kvůli nim zrychlena, protože vlastnosti katalyzátoru jsou vzhledem k jejich vysoké aktivitě neodmyslitelné. Elektroformování také nemůže bez složitých sloučenin, které je způsobeno nemožností získat takové spolehlivé povlaky z jednoduché soli, na rozdíl od kyanidových sloučenin.