Denaturace je proces změny struktury proteinu.
Denaturace je proces ztráty trojrozměrné konformace molekul proteinů. Takový jev může být dočasný nebo trvalý. V každé situaci je sekvence aminokyselinových zbytků v proteinové struktury zachovalé.
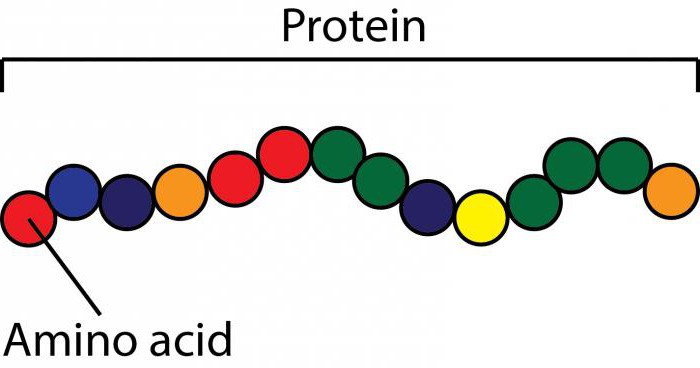
Zvláštní funkce
Denaturace proteinů je spojena se změnou teploty. V případě rozbití značného počtu vazeb, které stabilizují prostorovou strukturu molekuly proteinu, která je jedinečná, molekula zcela (nebo částečně) bude mít formu náhodné náhodné cívky.
Reverzibilní denaturace zahrnuje částečné změny, které nevedou k úplné změně primární aminokyselinové sekvence. V případě úplného zničení není možné obnovit strukturu proteinu.
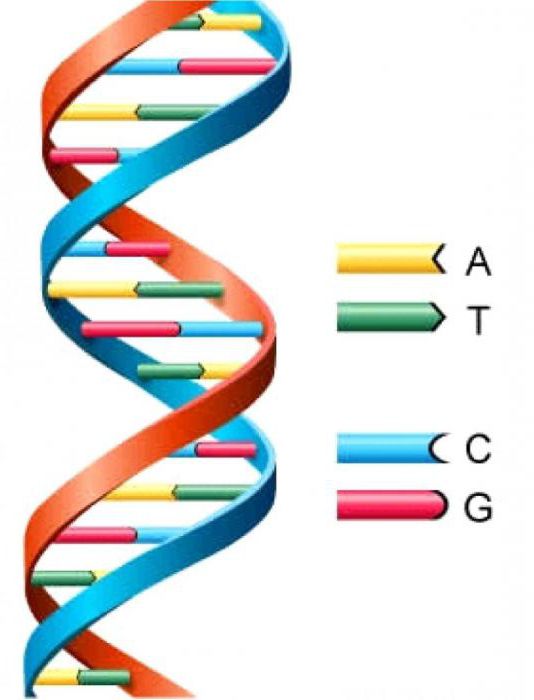
Charakteristický
Když se biopolymer zahřeje na 60-80 stupňů Celsia nebo se vystaví jiným činidlům, které mohou zničit nekovalentní (vodíkové, disulfidové) vazby v proteinech, dochází k denaturaci.
Tento jev je pozorován na rozhraní obou fází. V alkalickém nebo kyselém prostředí, stejně jako pod vlivem organických polárních rozpouštědel (fenolů, alkoholů), je struktura proteinu zničena.
Mechanismus
V některých případech používají k denaturaci močoviny nebo guanidinchloridu, které jsou schopné vytvářet vodíkové vazby s karbonylovými nebo aminoskupinami peptidových druhů, stejně jako s částí aminokyselinového radikálu.
Zároveň nahrazují intramolekulární vodíkové vazby existující v proteinové molekule, což vede ke změně sekundární a terciární struktury biopolymerů. Denaturace proteinů závisí na přítomnosti disulfidových vazeb v molekule.
Například disulfidové mosty jsou přítomny v inhibitoru trypsanu (pankreatický protein). Po obnovení se denaturace provádí bez použití dalších komponent denaturace. Když je protein následně umístěn za oxidačních podmínek, SH-skupiny cysteinu jsou oxidovány.
Výsledkem chemické interakce je obnovení počáteční konformace. Přítomnost jedné disulfidové vazby přispívá k významnému zvýšení stability celé prostorové struktury.
Denaturace je proces vedoucí ke snížení rozpustnosti molekuly proteinu. V důsledku jeho tvorby sediment "zkroucené" bílkoviny. Při vysoké koncentraci v roztoku biopolymeru je pozorováno úplné "srážení" hmotnosti roztoku.
Příkladem takového jevu mohou být transformace pozorované při vaření kuřecího vajíčka. Denaturace DNA zahrnuje úplnou ztrátu biologické aktivity proteinu. Tyto vlastnosti přispěly k použití roztoku jako antiseptické látky. karbolová kyselina.
Vysoká pravděpodobnost zničení struktury proteinových molekul vytváří obrovské množství potíží při jejich izolaci, studiu, praktickém použití pro průmyslové a lékařské účely.
Renaturace
Pokud je denaturací proces rozpadávání biopolymerů, pak je renaturace opakem. Obnova přirozené konformace molekuly proteinu je možná v případě pomalého ochlazování proteinu zničeného během zahřívání.
Podobný jev potvrzuje strukturu primární struktury proteinových molekul. Tvorba nativní konformace je spontánní proces zahrnující použití minimálního množství energie.
Prostorová struktura biopolymeru používá kódování umístění aminokyselinové sekvence v polypeptidu. To komplikuje postup renaturace proteinových molekul.

Závěr
Proteinové molekuly se stejnou nebo podobnou konformací mohou mít významné rozdíly v primární struktuře. Současně jsou různé aminokyseliny podobné v chemicko-fyzikálních vlastnostech postranních řetězců. Při procesu denaturace se molekula rozkládá, ztrácí schopnost plnit svůj biologický účel.
Pokud dojde k ultrafialovému nebo infračervenému záření kinetické energie biopolymer, což vede k vibracím jeho atomů. To způsobuje úplnou destrukci vodíkových vazeb, vyvolává koagulaci proteinové molekuly.