Princip Le Chatelier v chemii
V některých případech dochází k vzájemnému vzájemnému ovlivňování nebo rozpadu látek vzniklých reakcí a v systému se objevují současně dvě reakce: přímá (vznik reakčních produktů) a reverzní reakce (původní látky jsou nově syntetizovány). V případě shody náhodných a inverzních procesů v uvažovaném systému dochází k rovnováze, která se nazývá chemická. Jedná se o dynamickou rovnováhu, protože samotná reakce se nezastaví, ale vytváří se stejné množství látky a současně se rozkládá. S konstantní teplotou a tlakem může tato situace trvat dosti dlouhou dobu. V grafické podobě je uvedeno níže. Pod pojmem ekvivalentní rychlostí se rozumí určitá konstanta, která je současně rovna rychlosti přímých a zpětných reakcí.
Ad
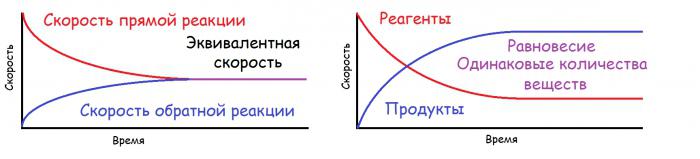
Princip biasu chemické rovnováhy
Zásada posunutí (posunu) rovnováhy byla objevena v roce 1884 Le Chatelier. Později ho shrnul Karl Ferdinand Brown (1887). Proto má v současné době dvojče - princip Le Chatelier-Brown. Tento zákon se používá jak v chemii, tak v termodynamice, elektrodynamice, ekologii a biochemii. Existuje mnoho formulací, ale podstatou každého z nich je následující: "Když je vliv na systém v rovnováze, chemická rovnováha se posune tak, aby kompenzovala tuto změnu (tj. Systém se pokusí obnovit rovnováhu) ". Popsaný princip může být jasně prokázán pomocí následujícího systému. Na pevnou oporu je připevněna pružina. V klidu je tento systém v rovnováze. Pokud je pružina napnutá, pak se rovnováha posune k vnějšímu vlivu. Systém však také zvyšuje opozici. A v určitém okamžiku se síly opozice a vnějšího vlivu stanou navzájem rovnými, v důsledku čeho nastane nový rovnovážný stav.
Ad
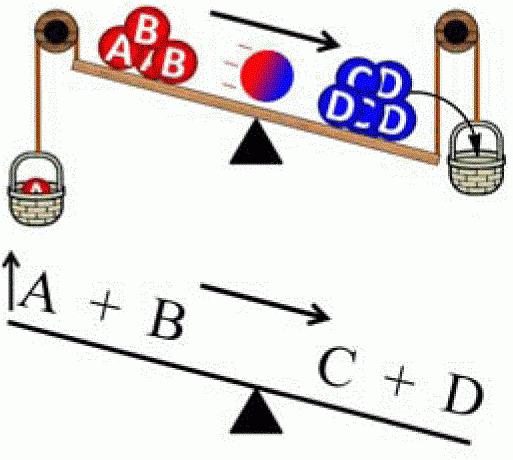
Princip Le Chatelier lze použít pouze pro systémy v rovnováze, jinak výsledky analýzy nebudou správné. Existují tři hlavní parametry, jejichž změna způsobuje posun v chemické rovnováze: tlak, teplota a koncentrace chemikálií.
Teplota
Změna teploty je nejčastější příčinou posunu chemické rovnováhy, což je pochopitelné, protože tento faktor je mnohem snazší ovlivnit, než například tlak. Zde je třeba uvést, že reakce jsou rozděleny do dvou typů tepelným účinkem. Mezi ně patří: exotermická (s teplem) a endotermická (s jeho absorpcí). Jak se v tomto případě posune chemická rovnováha? Princip Le Chatelier v tomto případě snižuje na následující: se zvyšující se teplotou se rovnováha posune směrem k reakci, k níž dochází při absorpci tepla, a když klesá, v opačném směru. Pokud tedy pro níže uvedenou reakci zvýšíte teplotu, váha se přesune na pravou stranu.
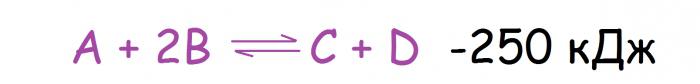
Nejvíce přímé reakce jsou exotermní a reverzní reakce jsou endotermní (to není pravidlo, ale spíše pozorování, z něhož lze nalézt mnoho výjimek).
Tlak
Jak se mění tlak, mění se další parametr systému - jeho objem (zvyšuje nebo snižuje), takže účinek tohoto parametru má obzvlášť silný vliv na systémy, ve kterých jsou přítomny plyny. V tomto případě platí princip chemická rovnováha je následující. Pokud se tlak v systému zvětší, pak se rovnováha posune ke snížení počtu molekul plynu a jak se tlak snižuje, rovnováha se pohybuje v opačném směru. Pokud se počet molekul plynu v průběhu reakce nemění, pak se rovnováha nezmění, jak se mění tlak, jako například v příští reakci.
Ad
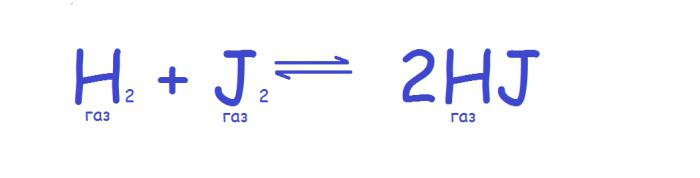
V praxi je však tento princip pravdivý pouze pro ideální plyny, protože všechny skutečné mají odlišnou stlačitelnost. Takže i když počet molekul plynu zůstává nezměněn, rovnováha může záviset na tlaku. V praxi to bude patrné, kdy vysoké tlaky. V případě kapalných a pevných látek změna tlaku ve skutečnosti neovlivňuje rovnováhu v důsledku malých objemů obsazených těmito látkami. Při zvažování smíšených systémů se berou v úvahu pouze molekuly plynu.
Rovnovážný posun v systému v důsledku změn v koncentraci jakékoli látky podílející se na reakci
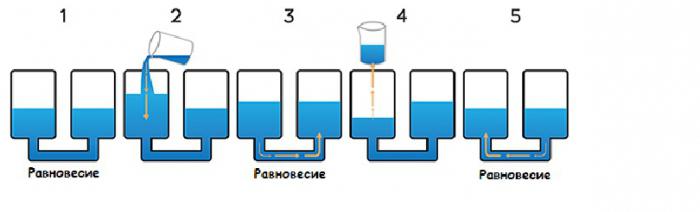
V průběhu změny koncentrace látky princip Le Chatelier funguje následovně. Při zvýšení koncentrace reakčních produktů se rovnováha posune směrem k obrácené reakci a se sníženým množstvím vytvořených látek se rovnováha pohybuje v opačném směru.
Ad
Co se stane, když přidáte inertní plyn
Můžete měnit hlasitost systému nejen jeho stlačením nebo oslabením tlaku, ale také přidáním inertního plynu, který nebude reagovat. Co se stane se systémem, když se do něj přidává helium? Ve skutečnosti se s největší pravděpodobností nic nestane, protože poměr látek obsažených v reakci se nezmění a proces nezáleží na celkovém tlaku systému, ale na části každého komponentu.
Efekt katalyzátoru
Množství katalyzátoru a jeho přítomnost obecně nemají žádný vliv na posun chemické rovnováhy. K tomu dochází s ohledem na skutečnost, že tento prvek rovnoměrně zrychluje jak přímou, tak i zpětnou reakci, udržuje rovnováhu v systému beze změny.
Způsob studování chemické rovnováhy
Podrobné zvážení chemické rovnováhy je velmi důležité pro úplné pochopení procesu. Jednou z nejčastěji používaných technik je tzv. Rovnovážná zmrazovací metoda. Takže tam je rychlý chlazení ve vyváženém stavu. Rovnováha prostě nemá čas na posun a při nízkých teplotách se většina procesů zpomaluje téměř na nulu. Z tohoto důvodu je možné úplně analyzovat složení směsi při jakékoliv teplotě (koncentrace látek zapojených do reakce, při nulových stupních, bude odpovídat počtu složek při teplotě, při níž začne redukce). Tato zkušenost se provádí několikrát s reakcemi probíhajícími v obou směrech.
Ad
Existuje úplná nezvratnost?
Není možné úplně posunout chemickou rovnováhu v jednom směru. Dokonce i se zdánlivým absolutním posunem bude vždy existovat malý počet molekul, které budou reagovat.

V praxi jsou prakticky všechny reakce reverzibilní a kolik bude tento efekt viditelný, často závisí na teplotě (často je rovnováha jednoduše silně posunutá v jednom směru, takže se stává viditelným až při změnách podmínek). Je to kvůli této prevalence reverzibilní chemické reakce studium rovnováhy je zvláště důležité.
Příklady syntéz, při nichž se během výroby mění chemická rovnováha
Při výrobě se chemická rovnováha obvykle posune směrem k přímému reakci, aby se získaly reakční produkty. Existuje mnoho příkladů takovýchto syntéz: získání amoniaku oxid síry (VI), oxid dusíku (II) atd.