Kovová vazba: elektrony ve veřejném vlastnictví
Speciální připojení
Nejde vždy o to, že elektrony jsou pevně vázány na atom a tvoří buď neutrální atomy nebo ionty. Existuje jiná forma existence elektronů - v kovové vazbě. Je velmi odlišný od jiných druhů, a proto má železo velmi specifické fyzikální vlastnosti. Jednou z vlastností, kterou poskytuje kovová chemická vazba, je schopnost dokonale provádět elektřinu. Pokud by lidé tuto kvalitu neuznali, technická civilizace prostě neexistovala.
Stejně jako v soli
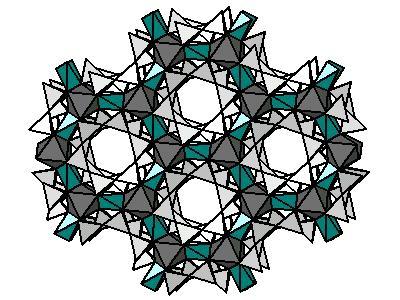
Kovové vazby jsou zvláštní stav atomů, ve kterých existují elektrostatické síly, vodivé elektrony tvoří určitý druh mraku a kladné ionty. V tomto případě jsou elektrony relativně volné a patří stejně jako všechny atomy kovové mřížky. Tato vlastnost je poněkud podobná vlastnostem roztavených solí, ale ne úplně, to je takové srovnání, i když má právo existovat, je spíše zjednodušující. Kvantově-mechanické zvážení tohoto problému naznačuje, že elektrony distribuují svou hustotu takovým způsobem, že atomy fyzicky zůstávají neutrální, ale zároveň malé negativní částice udržují relativní mobilitu.
Ad
Vysvětluje hodně

Kovové vazby jsou zodpovědné za takové kovové vlastnosti, jako je plasticita, pevnost, tvárnost, opacita, schopnost hladkého povrchu odrážet světlo. Ale nejdůležitější vlastností, která je pro lidi velmi důležitá, je velmi tepelná a elektricky vodivá. Elektrická vodivost je dosažena schopností elektronů být mobilní, zajišťující pohyb elektrického proudu.
Rozmanitost
Kovová vazba není jediná možná pro kovy. Například se tvoří čisté gálie kovalentních vazeb mezi atomy. A tyto páry jsou v uzlech krystalová mřížka a kolem - ano, vodivé elektrony, které také umožňují vytvářet kovový oblak. Obecně platí, že jediné číslo ve slově "vazba" není zcela správné, protože elektrony v oblaku jsou vlastnostmi spojů všech atomů. Ideální kolektivní ekonomika, kde se nikdo nepořádá.
Ad
Refraktérnost

Ve struktuře kovové mřížky jsou atomy vázány velmi velkými silami. To je důvod, proč je velmi obtížné tavit kov a tam jsou látky šampióny v teplotě tavení, například wolfram, který vyžaduje obrovskou teplotu ke změně stavu agregace. V tomto případě existuje jedna zvědavá výjimka - kovy skupiny zinku: samotný zinek, kadmium a rtuť. Tato vlastnost je dána tím, že jejich poslední skořápky jsou plné, jako u vzácných plynů, a jejich kovová vazba není zcela plná. Takže ve vakuu, vzhledem k těmto vlastnostem, nejsou používány.
Přesto ne ionty
Vlastnosti typických kovů jsou tedy zajištěny zvláštnostmi jejich existence ve formě mřížky s mobilními elektrony, které tvoří něco jako mrak, takže neutronové atomy nacházející se v mřížích. Ačkoli tradičně se uzly nazývají ionty, nejsou takové z hlediska přesnějšího kvantově-mechanického přístupu.