Výroba alkoholů, aplikace, vlastnosti. Způsoby výroby alkoholů
Alkoholy jsou v přírodě běžné. Většina lidí je obeznámená ethylalkoholu (ethanol) je aktivní složka v alkoholických nápojích, ale je to jen jedna z rodiny organických sloučenin známých jako alkoholy. Získat je, především ethyl (víno v důsledku enzymatické fermentace hroznového džusu, bylo jedním z prvních chemických procesů, které zvládlo lidstvo.
Názvosloví alkoholů
Alkoholy představují organických sloučenin hydroxylovou (OH) funkční skupinou s alifatickým atomem uhlíku. Vzhledem k tomu, že OH je členem molekul všech alkoholů, jsou často reprezentovány jako deriváty vody obecného vzorce ROH, kde R označuje alkylovou skupinu.
Výroba methanolických alkoholů (CH3OH) a ethanolu (CH3CH2OH), které jsou prvními dvěma členy jejich homologních řad, je důležitou úlohou chemického průmyslu v mnoha zemích. Obsahují-li od jednoho do čtyř atomů uhlíku, jsou často nazývány běžnými názvy, ve kterých je za názvem alkylové skupiny následováno slovo alkohol: 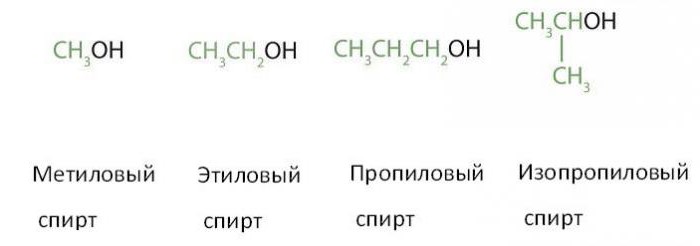
Je vidět, že všechny čtyři (poslední dva jsou izomery jedné látky) výše uvedené alkoholové molekuly obsahují jednu hydroxylovou skupinu. Na tomto základě všichni patří do třídy monohydric alkoholů (tam jsou také dva, tři, čtyři a polyatomic). Kromě toho jsou všechny deriváty nasycených uhlovodíků z množství alkanů: methanu, ethanu, propanu (názvy alkoholů se získají přidáním konce "-ol" na název alkénu). Proto se také nazývají okrajové monohydrické alkoholy.
Ad
Monohydricky alkoholy
Produkce, vlastnosti (fyzikální i chemické) těchto sloučenin závisí na počtu atomů uhlíku připojených k atomu, který je přímo spojen s OH skupinou. Proto mohou být monohydrické alkoholy na tomto základě rozděleny do tří tříd.
- Primární alkoholy mají molekulu, ve které je jeden atom uhlíku navázaný na OH skupinu připojen k jinému atomu C. Jejich obecný vzorec je RCH20H. Například ethanol je primární alkohol.
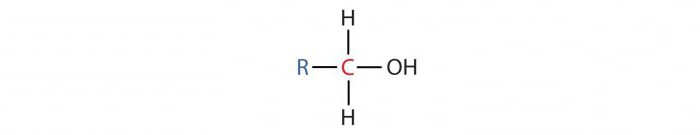
- Sekundární alkoholy mají v molekule jeden uhlíkový atom s OH skupinou připojenou ke dvěma dalším atomům C. Jejich obecný vzorec je R2CHOH. Patří sem propyl a isopropylalkoholy.
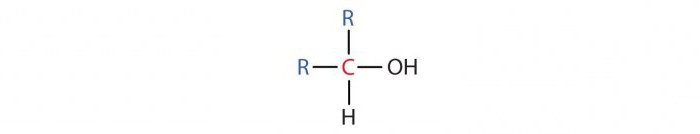
- Terciární alkoholy obsahují v molekule atom uhlíku s OH skupinou připojenou ke třem dalším atomům C. Jejich obecný vzorec je R3 COH.

Získání monohydricních alkoholů v průmyslu je možné několika způsoby, které budou popsány níže.
Metanol jako produkt zemního plynu
Metanol se získá smícháním plynného vodíku a oxidu uhelnatého při vysokých teplotách a tlacích (200 ° C, 350 ° C) v přítomnosti katalyzátoru sestávajícího z oxid zinečnatý (ZnO) a oxid chromu (Cr2O3) jako katalyzátoru: 2H2 + CO - CH3OH. 
V tomto případě je surovinou pro výrobu činidel zemní plyn a vodní pára, míchání, které produkuje syntézní plyn, což je směs CO a H2.
Metanol je důležité rozpouštědlo a používá se jako automobilové palivo, ať už jako čistá kapalina - v některých závodních automobilech, nebo jako vysoce oktanová přísada do benzínu. Výroba a používání alkoholů ve světě, zejména methanolu, se měří v milionech tun. Na konci roku 2013 bylo celosvětově spotřebováno 66 milionů tun metanolu, z toho 65% v Asii, 17% v Evropě a 11% v USA.
Ad
Získání konečných alkoholů z alkenů
Mnoho jednoduchých hmotnostních alkoholů průmyslově důležitých je produkováno hydratací (přidáním vody) alkenů (ethylen, propylen, buten). Při této reakci se získá ethanol, isopropanol, butanol (sekundární a terciární).
Známé přímé a nepřímé způsoby výroby alkoholů hydratací. Přímé umožňuje vyhnout se tvorbě stabilních meziproduktů, obvykle pomocí kyselých katalyzátorů.
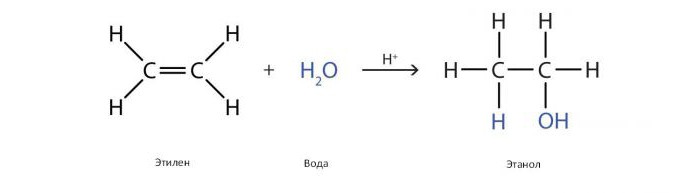
Katalyzátor je obvykle kyselina fosforečná, adsorbován na porézním nosiči, jako je silikagel nebo křemelina. Tento katalyzátor byl poprvé použit ve velkém měřítku výroby ethanolu ve Spojených státech společností Shell v roce 1947. Reakce se provádí za přítomnosti vysokotlaké páry při 300 ° C, přičemž mezi ethylenem a párou se udržuje poměr 1,0: 0,6.
Ad
Podobná reakce na výrobu isopropylalkoholu s katalyzátory ve formě kyselina sírová vypadá takto 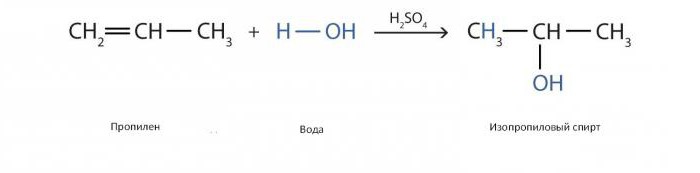
Nepřímá metoda hydrolýzy ethylenu
Nepřímým způsobem, v praxi poprvé aplikovaným v průmyslovém měřítku v roce 1930, který se dnes považuje za téměř úplně zastaralý, je reakce vedoucí k produkci alkoholů převedením alkénu na sulfátové estery, které se potom hydrolyzují. Tradičně se alken reaguje s kyselinou sírovou za vzniku alkylsulfátových esterů. V případě výroby ethanolu může být tento krok zapsán následovně: H 2 SO 4 + C 2 H 4 → C 2 H 5 -O-SO 3 H
Následně se tento sulfátový ester hydrolyzuje, dokud se kyselina sírová regeneruje a ethanolem se neuvolní: C2H5-O-S03H + H20 - H2S04 + C2H5OH.
Způsoby výroby alkoholů jsou extrémně různorodé, ale postup popsaný níže je pravděpodobně znám, alespoň každým čtenářem.
Alkoholová fermentace
Jedná se o biologický proces, při kterém molekuly, jako je glukóza, fruktóza a sacharóza, se přeměňují na buněčnou energii s paralelní produkcí ethanolu a oxidu uhličitého jako produktů metabolismu. Fermentace je katalyzována enzymy obsaženými v kvasinkách a probíhá prostřednictvím komplexního vícestupňového mechanismu, který obecně zahrnuje konverzi (v prvním stupni) škrobu obsaženého v rostlinných zrnech na glukózu a následnou produkcí ethanolu z ní. Protože kvasnice provádí tuto transformaci v nepřítomnosti kyslíku, alkoholová fermentace se považuje za anaerobní proces.
Ad
Reakce fermentace alkoholů mohou být znázorněny následovně: 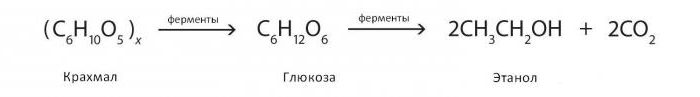
Způsoby, jak získat alkoholické nápoje
Veškerý ethanol obsažený v alkoholických nápojích se vyrábí fermentací způsobenou kvasinkami.
Víno se vyrábí fermentací přírodních cukrů přítomných v hroznech; Jablečné víno se získává obdobným kvašením přírodního cukru v jablkách a hruškách; a ostatní ovocná vína se vyrábějí fermentujícími sacharidy v jakémkoli jiném druhu ovoce. Brandy a brandy (například slivovice) jsou vyráběny destilací nápojů získaných fermentací ovocných cukrů.
Medové nápoje se vyrábějí fermentací z přírodních cukrů přítomných v medu. 
Pivo, whisky a vodka se vyrábějí fermentací škrobových zrn, které se převádějí na cukr účinkem enzymu amylázy, která je přítomna v obilných zrnech, které prošly klíčením sladu. K směsi mohou být přidány i další zdroje škrobu (například brambory a sladová zrna), protože amyláza bude působit také na jejich škrob.
Ad
Rýžová vína (včetně saké) se vyrábějí fermentací obilného škrobu, přeměněného na cukr Asugi Aspergillus ogugae.
Rum a některé další nápoje se získávají fermentací a destilací cukrové třtiny. Rum se obvykle vyrábí z cukrové třtiny - melasy.
Ve všech případech by měla probíhat fermentace v nádobě, která umožňuje únik oxidu uhličitého, ale zabraňuje vstupu vnějšího vzduchu. To je nezbytné, protože účinek kyslíku zabraňuje tvorbě etanolu a akumulace oxidu uhličitého vytváří riziko prasknutí nádoby. 
Nukleofilní substituční reakce
Alkoholy se vyrábějí v laboratořích metodami, které používají jako výchozí produkty pro reakci chemické látky širokého spektra tříd, od uhlovodíků po karbonylové sloučeniny. Existuje několik způsobů, jak se vracet k několika základním reakcím.
Primární halogenoalkany reagují s vodnými roztoky alkalického NaOH nebo KOH, čímž se vytváří primární alkoholy zejména při reakci nukleofilní alifatické substituce. Když například methylbromid reaguje s roztokem hydroxidu sodného, hydroxylové skupiny vytvořené během disociace alkalických látek nahrazují bromové ionty za vzniku methanolu. 
Několik reakcí, které umožňují výrobu alkoholů v laboratořích, je uvedeno níže.
Nucleophilic addition.
Grignardova reakční činidla (sloučeniny hořčíku s alkylhalogenidy - jodidy nebo bromidy) a organokovové sloučeniny mědi a lithia reagují s karbonylovými skupinami (C = O) aldehydů za vzniku primárních a sekundárních alkoholů v závislosti na přidávacím mechanismu Podobné reakce s ketony vedou k terciárním alkoholům . 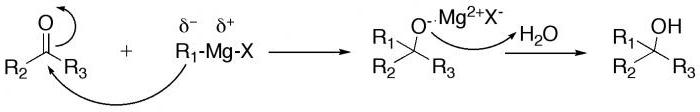
Barbierová reakce probíhá mezi halogenalkanem a karbonylovou skupinou jako elektrofilní substrát za přítomnosti hořčíku, hliníku, zinku, india, cínu nebo jeho solí. Reakčním produktem je primární, sekundární nebo terciární alkohol. Jeho mechanismus je podobný Grignardově reakci, s tím rozdílem, že Barbierova reakce je syntéza v jedné nádobě, zatímco Grignardovo činidlo je připraveno zvlášť před přidáním karbonylové sloučeniny. 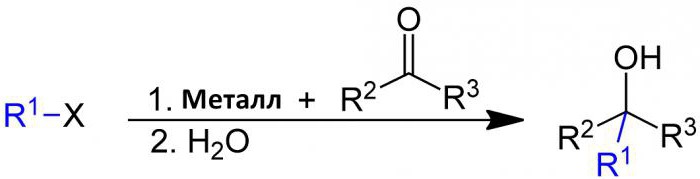 Jako nukleofilní adiční reakce se vyskytuje u relativně nenákladných a vodě odolných kovů nebo jejich sloučenin, na rozdíl od Grignardových činidel nebo organolithiových činidel. Z tohoto důvodu je v mnoha případech možné ji spustit ve vodě, což činí proces součástí zelené chemie. Barbierova reakce je pojmenována podle Philipa Barbiera, učitele Victora Grignarda.
Jako nukleofilní adiční reakce se vyskytuje u relativně nenákladných a vodě odolných kovů nebo jejich sloučenin, na rozdíl od Grignardových činidel nebo organolithiových činidel. Z tohoto důvodu je v mnoha případech možné ji spustit ve vodě, což činí proces součástí zelené chemie. Barbierova reakce je pojmenována podle Philipa Barbiera, učitele Victora Grignarda.
Reakce zotavení
Aldehydy nebo ketony se redukují na alkoholy borohydridem sodným (NaBH4) nebo (po kyselé úpravě) lithiumaluminiumhydridem (LiAlH).
Při reakci Meerwein-Pondorf-Wehrli (MPV) se výroba alkoholů redukcí z ketonů a aldehydů provádí za použití katalyzátoru na bázi alkoxidu hlinitého. Výhody MPV jsou jeho vysoká chemoselektivita a použití levného, ekologicky šetrného kovového katalyzátoru. Reakce objevily Meerwein a Schmidt a nezávisle Verli v roce 1925. Zjistili, že směs ethoxidu hliníku a ethanolu může snížit aldehydy na jejich alkoholy. Ponndorf aplikoval reakci na ketony a katalyzátor byl aktualizován na izopropylát hlinitý (Al (Oi-Pr) 3 , kde i-Pr je isopropylová skupina (CH (CH3) 2 ). za účelem získání isopropanolu.
Obecná rovnice pro získání alkoholu pomocí MPV redukce ketonů na alkoholy je následující:
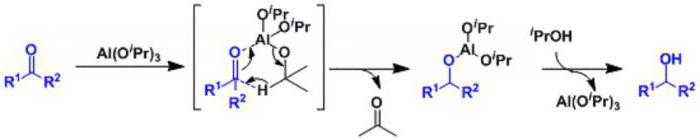
Samozřejmě to není všechno, co lze říci o alkoholech a jejich vlastnostech, ale doufáme, že jste se jim podařilo získat obecnou představu o nich.