První zákon termodynamiky je vysvětlením tohoto zákona a praktických příkladů.
Fyzické procesy, jako je teplo a práce, lze vysvětlit jednoduchým přenosem energie z jednoho těla do druhého. V případě práce je to asi mechanická energie Teplo přijímá tepelnou energii. Přenos energie probíhá podle zákonů termodynamiky. Hlavní body této části fyziky jsou známé jako "počátky".
První zákon termodynamiky reguluje a omezuje proces přenosu energie v jednom či druhém systému.
Typy energetických systémů
Ve fyzickém světě existují dva typy energetických systémů. Uzavřený nebo uzavřený systém má konstantní hmotnost. V otevřeném nebo otevřeném systému může hmotnost klesnout a zvýšit v závislosti na procesech, ke kterým dochází v tomto systému. Většina pozorovaných systémů je otevřená. 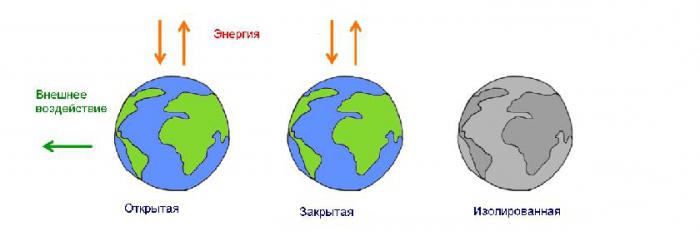 Výzkum v takových systémech je omezován množstvím náhodných faktorů ovlivňujících spolehlivost výsledků. Proto fyzikové studují jevy v uzavřených systémech, extrapolají výsledky na otevřené, berouce v úvahu nezbytné opravy.
Výzkum v takových systémech je omezován množstvím náhodných faktorů ovlivňujících spolehlivost výsledků. Proto fyzikové studují jevy v uzavřených systémech, extrapolají výsledky na otevřené, berouce v úvahu nezbytné opravy.
Izolovaná energie systému
Každá uzavřená soustava, ve které neexistuje žádná výměna energie s prostředím, je izolovaná. Rovnovážný stav takového systému je určen indikací takových veličin:
Ad
- P - systémový tlak;
- V je objem izolovaného systému
- T je teplota;
- n je počet molekul plynu v systému;
Jak je vidět, množství tepla a provedené práce nejsou zahrnuty v tomto seznamu. Uzavřený izolovaný systém neprovádí výměnu tepla a nevykonává práci. Její celková energie zůstává nezměněna.
Změna energie systému
Když se provede práce nebo dochází k výměně tepla, změní se stav systému a nebude považován za izolovaný.
Formulace prvního termodynamického zákona
Vnitřní energie Uzavřený systém se skládá ze součtu energií všech částic tohoto systému. Tato energie může být změněna pouze tím, že působí na systém zvenčí. Vnitřní energie takového uzavřeného systému se zvýší buď kvůli práci, která byla provedena v systému, nebo protože určité množství tepla je přeneseno do takového systému. Snížení celkové energie systému bude také záviset na dvou faktorech - ať už vydává teplo, nebo bude dělat nějakou práci.
Ad
Změna celkové energie může být vyjádřena vzorem, který vypadá takto: 
Pokud mluvíme o práci na systému, pak proměnná W bude záporné. Tento vzorec představuje první zákon termodynamiky.
Zákon o ochraně
Tento zákon je považován za jeden ze základních zákonů fyziky. Teplo a práce jsou hlavním prostředkem přenosu energie a změna vnitřní energie systému přímo závisí na těchto množstvích. Tím je upraven první zákon termodynamiky zákon o ochraně energie.
Za prvé byl pro izolované systémy odvozen první termodynamický zákon. Později se ukázalo, že zákon je univerzální a může být aplikován na otevřené systémy, pokud správně přihlédneme ke změně vnitřní energie, ke které dochází kvůli kolísání množství látky v systému. Pokud daný systém projde ze stavu A do stavu B, pak se práce prováděné systémem W a množství tepla Q liší. Různé procesy poskytují nerovnoměrné čtení těchto proměnných, i když systém nakonec přichází do původního stavu. Ale rozdíl je W - Q budou vždy stejné. Jinými slovy, jestliže se po jakémkoli nárazu systém vrátil do původního stavu, pak bez ohledu na typ procesů zapojených do transformace takového systému je dodržen pravidlo W - Q = const .
Ad
V některých případech je vhodnější použít diferenciální vzorec pro vyjádření prvního zákona. Vypadá to takto: dU = dW- dQ
zde dU - nekonečně malá změna vnitřní energie
dW - hodnota charakterizující nekonečně malý provoz systému
dQ - nekonečně malé množství tepla přeneseného do tohoto systému.
Enthalpy
Pro širší uplatnění prvního termodynamického zákona je představen koncept entalpie.
Toto je název celkového množství celkové energie látky a produktu objemu a tlaku. Fyzická exprese entalpie může být reprezentována následujícím vzorcem:
H = U + pV
Absolutní hodnota entalpie je součtem entalpií všech částí, které tvoří systém. 
Z kvantitativního hlediska nelze tuto hodnotu určit. Fyzici pracují pouze s rozdíly entalpií konečného a počátečního stavu systému. Koneckonců, u jakýchkoli výpočtů změní stav systému vybrat určitou úroveň, na které potenciální energie rovná se nula. Stejně tak dělají při výpočtu entalpie. Použijeme-li koncept entalpie, pak první zákon termodynamiky pro isoprocesses bude vypadat takto: dU = dW- dH
Enthalpie každého systému závisí na vnitřní struktuře látek tvořících tento systém. Tyto ukazatele závisí na struktuře látky, její teplotě, množství a tlaku. U komplexních látek je možné vypočítat standardní entalpii tvorby, která se rovná množství tepla, které je potřebné k vytvoření molu látky z jednoduchých složek. Standardní hodnota entalpie je zpravidla záporná, protože při syntéze komplexních látek se ve většině případů uvolňuje teplo.
Ad
První zákon termodynamiky v adiabatických procesech
Použití prvního termodynamického zákona pro isoprocesses může být zvažováno graficky. Zvažte například adiabatický proces, při kterém množství tepla zůstává konstantní po celou dobu, to znamená Q = const . Takový izoproces probíhá v tepelně izolovaných systémech nebo v tak krátké době, že systém nemá čas na provedení výměny tepla s vnějším prostředím. Pomalá expanze plynu v diagramu objemového tlaku je popsána v následující křivce:
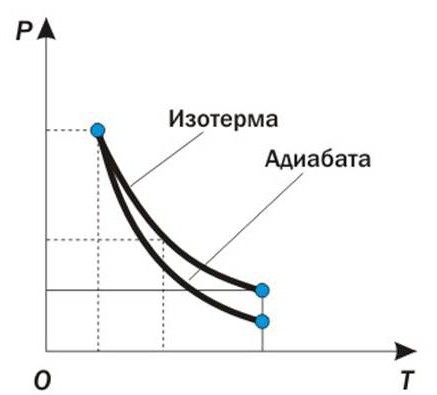
Podle harmonogramu je možné doložit uplatnění prvního zákona termodynamiky na isoprocesy. Vzhledem k tomu, že nedochází ke změně množství tepla v adiabatickém procesu, změna vnitřní energie se rovná množství vyrobené práce. dU = - dW
Z toho vyplývá, že vnitřní energie systému klesá a jeho teplota klesá.
Příklady adiabatických procesů
Konverzace je také pravdivá: pokles tlaku v nepřítomnosti výměny tepla prudce zvyšuje teplotu systému. Přibližně se plyn rozšiřuje ve spalovacích motorech. U vznětových motorů je hořlavý plyn stlačen 15krát. Krátkodobé zvýšení teploty umožňuje, aby se hořlavá směs samovolně vznítila. 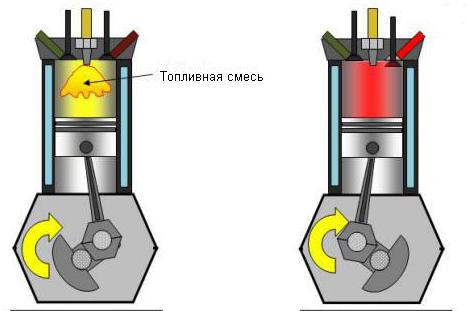
Jiný příklad adiabatického procesu může být zvážen - volná expanze plynů. Za tímto účelem zvažte instalaci, která se skládá ze dvou nádrží: 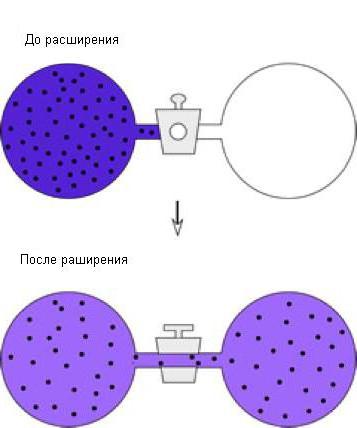
V první nádrži je plyn, v druhém je nepřítomen. Když otočíme kohoutek, zajistíme, že plyn naplní veškerý objem, který mu je přidělen. Při dostatečné izolaci systému zůstane teplota plynu nezměněna. Vzhledem k tomu, že plyn nedělal žádnou práci, proměnná dW = const . Ukázalo se, že při rovnovážných činnostech se teplota plynu během expanze snižuje. Rozptyl plynu je nerovnoměrný, proto tento proces nemůže být znázorněn na diagramu tlaku a objemu.
První termodynamický zákon je univerzální zákon, který platí pro všechny viditelné procesy vesmíru. Hluboké pochopení příčin určitých transformací energie nám umožňuje pochopit existující fyzikální jevy a objevit nové zákony.