Struktura plynných, kapalných a pevných těles je krátká
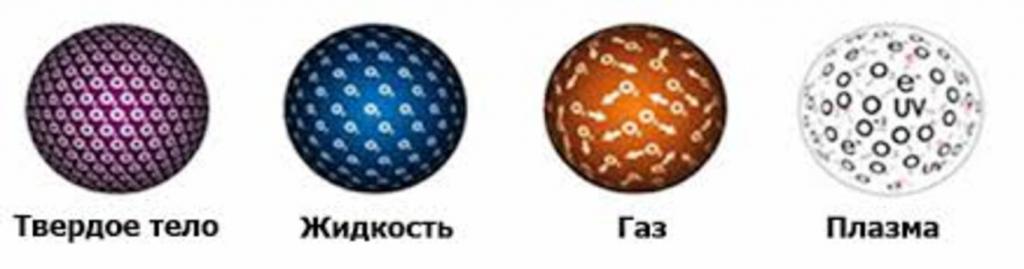
Za určitých podmínek je veškerá záležitost na planetě Zemi přítomna v jednom ze tří stavů: plynná, kapalná nebo pevná. Existuje také čtvrtý stav hmoty nazvaný plazma. Zvažte otázku struktury plynných, kapalných a pevných těles, stejně jako jejich přechod z jednoho stavu do druhého, když se změní vnější podmínky.
Pevný stav hmoty
Pevné látky jsou charakterizovány schopností odolávat vnějším silám, které je ovlivňují, aby mohly změnit svůj tvar a objem. Vzhledem k otázce struktury plynných, kapalných a pevných těles a jejich bydlení je nutno říci, že molekuly v nich jsou pevně spojeny. Proto má objekt zvláštní formu, kterou zachovává za stejných vnějších podmínek.
Molekuly v pevné látce mohou být v uspořádaném stavu, pak mluví o krystalické struktuře. Nebo mohou být v neuspořádaném stavu, pak mluvíme o amorfních pevných látkách. Výrazný příklad krystalová mřížka je struktura kovových systémů, která ve vesmíru tvoří ideální mřížku určitého typu, v jehož uzlech jsou ionty atomů. Příkladem pevného předmětu s amorfní strukturou je sklo.

Věda o pevných látkách
Solids studuje několik věd, které zahrnují následující:
- Fyzika kondenzovaných látek. Studie pevné a kapalné hmoty, jejichž rozměry přesahují 10 19 částic, za použití experimentálních a teoretických metod.
- Mechanika deformací. Tato věda studuje mechanické vlastnosti pevných látek jako jsou napětí v nich, elastické a plastické deformace, jakož i spojení těchto vlastností s termodynamickými vnějšími parametry. V této disciplíně není struktura nejtěžší substance důležitá.
- Věda o materiálech. Již studoval strukturu molekul pevných, kapalných a plynných těles, stejně jako fázové přechody mezi těmito stavy.
- Chemie pevných látek. Tato disciplína se specializuje na syntézu nových materiálů v pevném stavu.
Některé vlastnosti pevných látek
Při konstantním tlaku a relativně nízkých teplotách je látka v pevném stavu. Účinek malé vnější síly na pevný stav nevede k vnější viditelné deformaci tuhého tělesa.
Pokud zvýšíte sílu, začne se tělo elasticky deformovat. Při ještě větším zvýšení vnější expozice jsou možné dvě možnosti:
- Pokud je tělo kovem, začne se projevovat plastická deformace, tj. Ve tvaru se projeví významné změny, které zůstanou po zastavení vnějšího vlivu.
- Pokud má tělo amorfní strukturu nebo krystalickou strukturu, ale v místech mřížky budou ionty různých znaků, například krystalů soli NaCl, pak se tělo plasticky deformuje, ale prostě se zhroutí.
Každé pevné těleso je charakterizováno určitou hustotou. Nejlehčí látkou v této kategorii je aerogel, její hustota je 3 kg / m 3 . Ale nejhustší pevný materiál známý lidstvu je kov - osmium. Jeden metr krychlový osmium má hmotnost 22,600 kg.
Kovové materiály
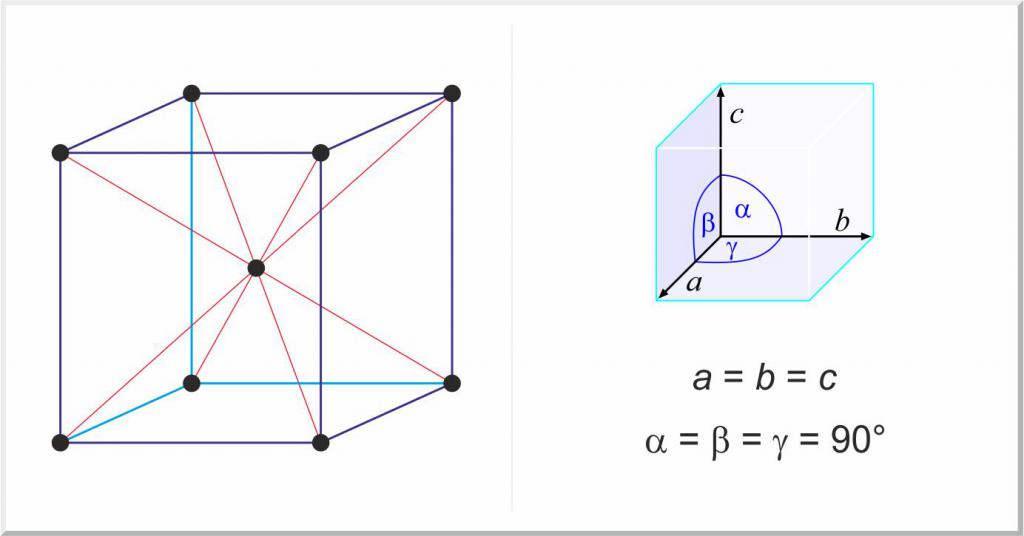
Zvláštní skupinou pevných látek jsou čisté kovy a jejich slitiny. V tomto případě rozdíl v struktuře pevných látek z plynných a kapalných stavů hmoty spočívá v existenci prostorové periodické mřížky, která se nazývá krystalová mřížka.

Kvůli své krystalické struktuře mají kovy řadu důležitých vlastností, například plasticitu a difrakci. Téměř všechny existují ve třech hlavních krystalických mřížkách:
- obličej centrovaný kubický, např. Au, Ag, Al, Cu;
- tělo-centrovaná kubická, například Nb, Mo, W, Fe;
- Hexagon těsně zabalený, například Ti, Zr.
Krystalografická věda byla vyvinuta ke studiu vlastností křišťálových mřížek.
Kondenzované látky - tekuté
Kapalný stav i pevný stav jsou nestlačitelné, to znamená, že si zachovává svůj objem v širokém rozsahu tlaků. Tekutina však nezachová svůj tvar, který ji odlišuje od pevné látky a přibližuje ji plynnému stavu hmoty.

Pokud molekula a atomová síla působí při tvorbě pevných látek, kapalina je tvořena molekulami, které jsou navzájem propojeny pouze molekulárně slabými silami. Nejběžnější na Zemi je voda, která jako plyn může mít podobu nádoby, do které je umístěna.
Pokud mluvíme o struktuře plynných, kapalných a pevných těles, je třeba uvést, že kapalina, na rozdíl od plynu, nezmění svou hustotu, když je umístěna v uzavřené nádobě.
Fluidní specifické funkce
Pro každou tekutinu v důsledku přítomnosti molekulárních sil v ní jsou takové vlastnosti, jako je povrchové napětí a kapilární účinek. Pokud se látka nachází v oblasti gravitace, například v naší Zemi, pak jakákoli těla, která je v ní umístěna, bude vytlačena z kapaliny podle slavného zákona Archimedes.

Pokud gravitační schopnost neovlivní kapalinu, bude vztlaková síla nulová. Kromě toho při absenci vnějších sil látek v takovém stavu má sklon získat nejmenší plochu povrchu, čímž se snižuje celková energie. Proto v podmínkách beztíže mají vodní kapičky sférický tvar, protože míč je číslem s nejmenší plochou pro tento objem kapaliny.
Kapilární vlastnosti jsou vysvětleny schopností molekul vstoupit do vzájemných vztahů nejen vzájemně, ale také s atomy a molekulami jiných těles. Tyto fyzikální charakteristiky kapaliny se nazývají soudržnost a adheze.
Stručně řečeno o struktuře plynných, kapalných a pevných těles bychom se měli zmínit o vlastnostech viskozity, která je vlastně v tekutém a plynném stavu. Viskozita je schopnost odolat jakémukoli posunu vrstvy látky vůči sobě navzájem v přítomnosti tlakového gradientu. U tekutin závisí tento indikátor na rychlosti posunutí těchto vrstev, teplotě a molekulové hmotnosti. Čím vyšší je rychlost těla v tekutině, tím větší je molekulová hmotnost částic tekutiny a čím nižší je teplota, tím větší je viskozita.
Struktura plynu
Plyn je stav hmoty, když jeho částice nejsou vzájemně propojeny, nebo tyto síly jsou velmi slabé. Takové látky volně mění objem a tvar, plní celou nádobu, do které jsou umístěny. Tento rozdíl v struktuře plynných těles z kapaliny a tuhé látky vede k tomu, že mají nižší hustotu. V případě plynné vody je běžné mluvit o páru.

Neexistuje absolutní porucha ve skutečných plynech. Molekuly v něm se však pohybují tak rychle, že prakticky vzájemně vzájemně nekomunikují. Proto plyn plní absolutně jakýkoliv objem a molekuly v něm budou odděleny poměrně velkými vzdálenostmi ve srovnání s velikostí samotných molekul. Vzhledem k velké vzdálenosti mezi molekulami se plyny snadno komprimují a zároveň zvyšují jejich hustotu a vnitřní tlak.
Perfektní plyn
Ve fyzice vytvářejí modely struktury pevných, kapalných a plynných těles určité rozumné zjednodušení reálných stavů hmoty, které umožňují použít jednodušší matematický přístroj pro studium těchto stavů. Jedním z takových modelů byla koncepce ideálního plynu.
Tento termín se vztahuje k plynovému stavu látky, ve které molekuly mají ve srovnání se vzdáleností mezi těmito body rozměry bodů a ve kterých vzájemně nereagují.
Za normálních podmínek, tj. Při atmosférickém tlaku a teplotě místnosti, lze považovat většinu reálných plynů za ideální. Například dusík, kyslík, vodík, vzácné plyny, oxid uhličitý a další.
Rovnice stavu pro ideální plyn je následující:
P * V = n * R * T, kde:
P, V, T a n - tlak, objem, teplota a množství plynné látky
R = 8,31 J / (mol * K) je univerzální konstanta.
Plazma je čtvrtý stav hmoty
Když uvažujeme o struktuře plynných, kapalných a pevných těles v 10. třídě, věnuje pozornost i jinému stavu hmoty - plazmě, která je plynem sestávajícím z kationtů a aniontů, to znamená kladně a záporně nabitých částic. Hlavním příkladem plazmy je látka, která tvoří naše slunce.
Pro řadu vlastností je plazma podobná plynu, jediný rozdíl spočívá v tom, že je schopen reagovat na magnetické pole a také provádět elektrický proud. Plazma může být získána zahříváním plynu na vysoké teploty, protože to způsobuje kolize mezi molekulami, což vede k jejich částečné nebo úplné ionizaci.
Změna stavu hmoty
Ve fyzice třídy 10 je zvažována struktura plynných, pevných a tekutých těles spolu s přechody mezi těmito stavy. Přechody mezi stavy látek jsou možné díky změnám tlaku a teploty. Změny se vyskytují pouze ve fyzické struktuře plynných, kapalných a pevných těles a jejich chemické složení zůstává konstantní.
Následující přechody mezi různými stavy hmoty jsou možné:
- Tavení Endotermický proces přechodu od pevného k tekutému.
- Krystalizace. Exotermický proces, při kterém se kapalina během chlazení stává pevnou.
- Vařte. Fyzikální endotermický proces, při kterém kapalina vstupuje do plynu.
- Kondenzace Exotermický přechod plynu na kapalinu.
- Sublimace nebo sublimace. Endotermický přechod z pevné látky na plyn, který obchází kapalný stav. Klasickým příkladem je sublimace suchého ledu.
Je třeba poznamenat, že všechny endotermické a exotermické procesy fázových přechodů probíhají s konstantní teplotou látky. Všechny tyto procesy, jejichž existence je způsobena zvláštnostmi struktury plynných, kapalných a pevných těles, jsou energetické, to znamená, že vyžadují buď dodávku nebo odstranění energie během jejich realizace.