Jak vypadá aminokyselinová vzorec?
Obecný vzorec aminokyselin potvrzuje přítomnost uhlíku, vodíku, kyslíku v molekule, stejně jako obsah dvou funkčních skupin: karboxylové a aminoskupiny. Právě oni vysvětlují amfiterový charakter těchto sloučenin, dualitu jejich struktury.
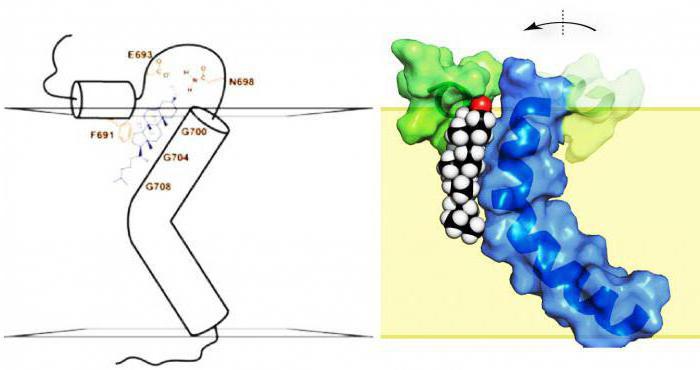
Význam sloučenin
Všechny procesy spojené s vitální aktivitou organismů se vyskytují na molekulární úrovni. Proto je tak důležité mít úplné pochopení vlastností všech organické látky jejich fyzikálních a chemických vlastností.
Zvažte některé aminokyseliny, jejichž vzorce a názvy jsou známy i moderním školákům.
Několik desetiletí došlo k rychlému vývoji biochemie. Díky inovativním výzkumným metodám bylo možné vysvětlit komplexní transformace spojené se syntézou proteinových molekul. Informace získané ve specializovaných vědeckých laboratořích se používají v lékařském a farmaceutickém průmyslu.
Ad

Biochemické funkce
Tato věda studuje chemické složení živých organismů, jejich strukturu, transformace. Díky biochémii je odvozeno obecné složení aminokyselin, sacharidů a tuků. Počínaje devátým stoletím se dnes biochemie stala spojencem při léčbě komplexních dědičných chorob.
Vlastnosti a struktura aminokyselin
Jakýkoli vzorec aminokyselin je derivát amoniaku a karboxylové kyseliny. V současné době existuje zhruba tři stovky zástupců této třídy, kteří se nacházejí v divočině. Jakýkoli vzorec aminokyselin, bez ohledu na charakteristiky uhlíkového řetězce, se skládá ze dvou funkčních skupin. Každý z nich opouští své obecné chemické vlastnosti těchto sloučenin. Obecný vzorec aminokyselin je NH2-CH (R) -COOH
Ad
Radikál, který je součástí molekuly, je derivátem omezujícího uhlovodíku.
Existují vyměnitelné a esenciální aminokyseliny, jejich vzorce jsou zvažovány v průběhu organické chemie.
Dvacet členů této třídy je součástí bílkovinných molekul, jsou považovány za jejich základní strukturní složku.
Mezi těmi látkami, které absolventi středních škol mají vědět, jsou: alanin, prolin, leucin, glycin, glutamin, valin, kyselina asparagová.
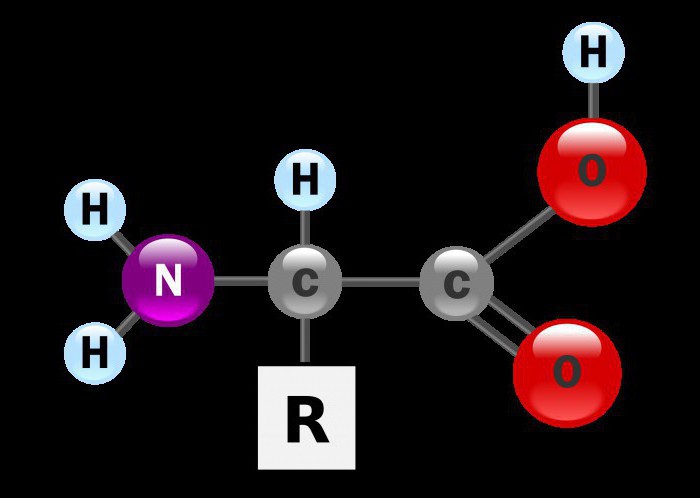
Amino klasifikace
V závislosti na typu aminokyselinového vzorce mohou existovat určité rozdíly v názvu. V naší době jsou izolované sloučeniny s nepolárními radikály. Mezi nimi vyberte alanin, prolin, valin, isoleucin, tryptofan, fenylalanin. Kromě toho existují aminokyseliny, které mají polární nenabité radikály: serin, cystein, glutamin, asparagin.
Standardní sloučeniny jsou integrální komponenty polypeptidových proteinových řetězců, které působí jako L-prostorové izomery. Téměř všechny obsahují asymetrický atom uhlíku ve struktuře, což vysvětluje volnou prostorovou rotaci aminokyselin.
Tyto sloučeniny jsou zahrnuty v mikrobiálních buňkách, které se vyskytují v složení antibiotik.
Proces vzájemné transformace stereoizomerů se nazývá racemizace. Vedle standardních zástupců této třídy jsou do proteinových molekul zahrnuty i nestandardní aminokyseliny.
V závislosti na zvláštnosti proteinové molekuly se na tvorbě podílejí pouze určité aminokyseliny. Například hydroxyprolin je přítomen v kompozici kolagenu.
Všechny aminokyseliny jsou slabé elektrolyty, proto ve vodném roztoku podléhají jen částečné disociaci. Schopnost sloučenin být ve formě polárních iontů se používá při analýze biologických objektů za účelem identifikace složení aminokyselin. Pro tento účel jsou vhodné metody jako je elektroforéza, iontoměničová chromatografie.
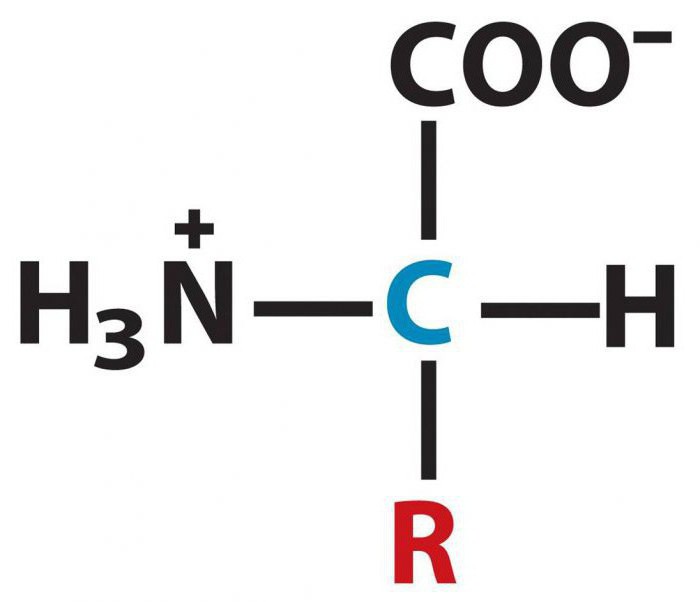
Jedná se o aminokyselinovou sekvenci, která určuje charakteristiky primární struktury proteinových molekul. Mezi hlavní oblasti použití této třídy organických látek lze poznamenat použití v organické syntéze farmaceutického průmyslu. Aminokyseliny se také používají jako krmivo pro skot.