Co je to reverzibilní reakce?
Co je to reverzibilní reakce? Jedná se o chemický proces, který se odehrává ve dvou vzájemně opačných směrech. Zvažte hlavní charakteristiky těchto transformací a jejich charakteristické parametry.
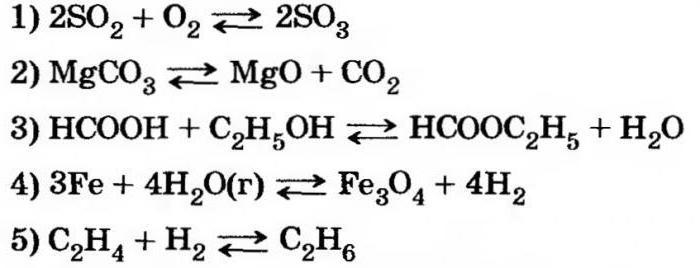
Jaká je podstata rovnováhy
Reverzibilní chemické reakce nevyrábějí určité produkty. Například během oxidace oxidu sírového (4), současně s produkcí oxidu sírového (6), se znovu vytvoří počáteční složky.
Nevratné procesy zahrnují úplnou transformaci interakčních látek doprovázené obdobnou reakcí, při které se získá jeden nebo více reakčních produktů.
Příklady nevratných interakcí jsou reakce rozkladu. Například při vytápění manganistan draselný kovový manganát, oxid manganitý (4) a plynný kyslík je také uvolněn.
Reverzibilní reakce neznamená tvorbu srážek, vývoj plynu. To je právě jeho hlavní rozdíl od nevratné interakce.
Chemická rovnováha je takový stav interagujícího systému, ve kterém se jedna nebo několik chemických reakcí může objevit reverzibilně za podmínky, že rychlost procesů je stejná.
Pokud je systém v dynamické rovnováze, nedochází ke změně teploty, koncentrace činidel a dalších parametrů v daném časovém období.

Podmínky rovnovážného posuvu
Reverzibilní reakční rovnováha lze vysvětlit pomocí pravidla Le Chatelier. Její podstatou spočívá ve skutečnosti, že když působí vnější vliv na systém, který je zpočátku v dynamické rovnováze, dochází ke změně reakce v opačném směru, než je účinek. Každá reverzibilní reakce s použitím tohoto principu může být posunuta správným směrem v případě změn teploty, tlaku, stejně jako koncentrace interakčních látek.
Princip Le Chatelier "pracuje" pouze pro plynná činidla, tuhé a kapalné látky nejsou brány v úvahu. Existuje reciproční vztah mezi tlakem a objemem definovaným Mendeleevovou - Clapeyronovou rovnicí. Je-li objem počátečních plynných složek větší než reakční produkty, pak je třeba změnit rovnováhu napravo, je důležité zvýšit tlak směsi.
Například při transformaci oxid uhelnatý (2) v oxid uhličitý 2 mol reaguje oxid uhelnatý a 1 mol kyslíku. To tvoří 2 moly oxidu uhelnatého (4).
Pokud by se v důsledku tohoto problému tato reverzibilní reakce posunula napravo, je nutné zvýšit tlak.
Koncentrace reakčních složek má také významný vliv na proces. Podle principu Le Chatelier, v případě zvýšení koncentrace počátečních složek, se rovnováha procesu posune směrem k výsledku jejich interakce.
V tomto případě přispívá snížení (odstranění z reakční směsi) výsledného produktu k toku přímého procesu.
Vedle tlaku, koncentrace, změna teploty má významný vliv na průběh zpětné nebo přímé reakce. Při zahřívání počáteční směsi se pozoruje rovnovážný posun směrem k endotermickému procesu.

Příklady reverzibilních reakcí
Zvažte v konkrétním procesu způsoby, jak posunout rovnováhu směrem k tvorbě reakčních produktů.
2CO + 02-2CO2
Tato reakce je homogenní proces, protože všechny látky jsou ve stejném (plynném) stavu.
V levé části rovnice jsou 3 objemy komponent, po interakci tento indikátor poklesne, tvoří se 2 objemy. Pro průtok přímého procesu je nutné zvýšit tlak reakční směsi.
Vzhledem k tomu, že reakce je exotermní, je teplota snížena, aby se vytvořil oxid uhličitý.
Zbytek procesu se posune směrem k tvorbě reakčního produktu se zvyšující se koncentrací jednoho z výchozích látek: kyslíku nebo oxidu uhelnatého.
Závěr
Reverzibilní a nevratné reakce hrají důležitou roli v lidském životě. Výměnné procesy, které se vyskytují v našem těle, jsou spojeny se systematickým posunem chemické rovnováhy. Při chemické výrobě se optimální podmínky používají k tomu, aby reakce směřovala správným směrem.