Alkenes hydratace: reakce a rovnice
Zjistěte, jaká je reakce hydratace alkénu. K tomu uvádíme stručný popis této skupiny uhlovodíků.
Obecný vzorec
Alkény jsou nenasycené organických sloučenin mající obecný vzorec SpN2n, v molekulách, u kterých existuje jedna dvojná vazba, a také přítomné jednoduché (jednoduché) vazby. Atomy uhlíku v něm jsou v sp2 hybridním stavu. Zástupci této třídy se nazývají ethylen, protože předkem této série je ethylen.

Vlastnosti nomenklatury
Abychom porozuměli mechanismu hydratace alkénu, je třeba rozlišit vlastnosti jejich jména. Podle systematické nomenklatury se při sestavování názvu alkénu používá určitý algoritmus akcí.
Ad
Nejprve musíte určit nejdelší uhlíkový řetězec, včetně dvojité vazby. Čísla označují umístění uhlovodíkových radikálů, počínaje nejmenší v ruské abecedě.
Pokud je v molekule několik identických radikálů, k názvu se přidávají di-, tri-, tetra-specifikující předpony.
Teprve poté se zavolá řetězec atomů uhlíku, přidá se přípona - na konci. Pro objasnění polohy nenasycené molekuly (dvojnásobné vazby) je označeno číslem. Například 2-methylpenten-2.

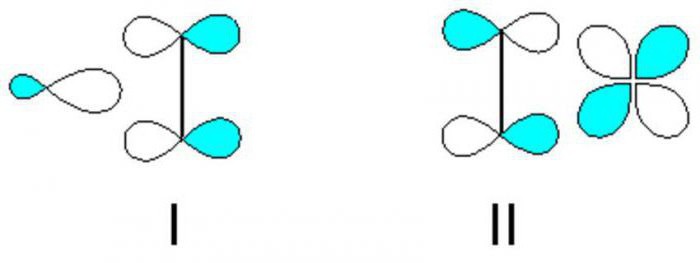
Hybridizace v alkénách
Abychom zvládli úkol následujícího typu: "Nastavit molekulární vzorec alkénu, jehož hydratace obdržela sekundární alkohol", je nutné zjistit strukturální vlastnosti zástupců této skupiny uhlovodíků. Přítomnost dvojné vazby vysvětluje schopnost ShNu vstoupit do reakce přidávání. Úhel mezi dvojitými vazbami je 120 stupňů. Pro nenasycenou vazbu není pozorována žádná rotace, proto je izomerie charakteristická pro zástupce této třídy. Jedná se o dvojnou vazbu, která působí jako hlavní místo reakce v molekulách alkenů.
Ad
Fyzikální vlastnosti
Jsou podobné nasyceným uhlovodíkům. Nejnižšími představiteli této skupiny organických uhlovodíků jsou plynné látky za normálních podmínek. Dále dochází k postupnému přechodu na kapaliny a pro alkény, jejichž molekuly obsahují více než sedmnáct atomů uhlíku, jsou charakterizovány pevným stavem. Všechny sloučeniny této třídy mají slabou rozpustnost ve vodě, zatímco jsou dokonale rozpustné v polárních organických rozpouštědlech.
Vlastnosti isomerismu
Přítomnost ethylenových sloučenin v molekulách vysvětluje rozmanitost jejich strukturních vzorců. Kromě izomerizace uhlíkového skeletu, charakteristického pro zástupce všech tříd organických sloučenin, mají izomery mezi třídami. Jedná se o cykloparafiny. Například pro propen je mezipříslovým izomerem cyklopropan.
Přítomnost dvojné vazby v této třídě molekul vysvětluje možnost geometrické cis a trans izomerie. Takové struktury jsou možné pouze v symetrických nenasycených uhlovodících, které mají ve svém složení dvojnou vazbu.
Existence této varianty isomerismu je dána nemožností volné rotace atomů uhlíku dvojitou vazbou.
Specifičnost chemických vlastností
Mechanismus hydratace alkénu má určité rysy. Tato reakce se týká elektrofilního přidávání.
Jak probíhá hydratační reakce alkénu? Chcete-li odpovědět na tuto otázku, zvažte pravidlo Markovnikov. Její podstatou spočívá ve skutečnosti, že hydratace alkenů asymetrické struktury se provádí určitým způsobem. Atom vodíku se připojí uhlík, který je více hydrogenovaný. Hydroxylová skupina je připojena k atomu uhlíku, který je menší než N. Hydratace alkenů vede k tvorbě sekundárních monohydrických alkoholů.
Ad
Aby reakce probíhala v plném rozsahu, používají se jako katalyzátory minerální kyseliny. Zaručují vstup požadovaného množství kationtů vodíku do reakční směsi.
Hydratací alkenů nelze získat primární monohydricní alkoholy, protože nebude dodržena Markovnikova pravidla. Tato vlastnost se používá při organické syntéze sekundárních alkoholů. Jakákoliv hydratace alkenů se provádí bez použití drsných podmínek, takže proces zjistil, že je prakticky používán.
Pokud je ethylen přijat jako počáteční zástupce třídy SpN2p, pravidlo Markovnikov nefunguje. Jaké alkoholy nelze získat hydratací alkenů? V důsledku tohoto chemického procesu není možné získat primární alkoholy z asymetrických alkenů. Jak se alkény hydratují? Získání alkoholů sekundární typ se provádí tímto způsobem. Pokud je jako uhlovodík vybrán zástupce acetylenové řady (alkiny), hydratace vede k výrobě ketonů a aldehydů. 
Podle Markovnikova pravidla jsou alkény hydratovány. Reakce má elektrofilní přidávací mechanismus, jehož podstata je dobře studována.
Ukažme některé konkrétní příklady takových změn. Co způsobuje hydrataci alkenů? Příklady nabízené v kurzu školní chemie ukazují, že propanol-2 může být získán z propenu interakcí s vodou a butanol-2 se získá z butenu-1.
Ad
V průmyslových objemech se používá hydratace alkenů. Tímto způsobem se získají alkoholy sekundární kompozice.

Halogenace
Kvalitativní reakce dvojná vazba je považována za interakci nenasycených uhlovodíků s halogenovými molekulami. Již jsme analyzovali, jak dochází k hydrataci alkenů. Mechanismus halogenace je podobný.
Halogenové molekuly mají kovalentní nepolární chemickou vazbu. Při manifestaci časových fluktuací v každé molekule dochází k elektrofilnosti. V důsledku toho se zvyšuje pravděpodobnost výskytu adice spolu s destrukcí dvojné vazby v molekulách nenasycených uhlovodíků. Po ukončení procesu je reakčním produktem dihalogenalkanový derivát. Bromace se považuje za kvalitativní reakci na nenasycené uhlovodíky, jelikož hnědá barva halogenu postupně zmizí.

Hydrohalogenace
Již jsme zkoumali vzorec pro hydrataci alkenů. Interakční reakce s bromovodíkem mají obdobnou variantu. V této anorganické sloučenině je tedy kovalentní polární chemická vazba, takže elektronová hustota je posunuta na více elektronativní atom bromu. Vodík získává částečný kladný náboj, daruje elektron na halogen, napadá molekulu alkenu.
Ad
Pokud nenasycený uhlovodík má asymetrickou strukturu, při interakci s halogenovodíkem se tvoří dva produkty. Proto se 1-brompropan a 2-brompropan získají z propenu během hydrohalogenace.
Pro předběžné vyhodnocení interakčních možností se bere v úvahu elektronegativita selektovatelného substituentu.
Oxidace
Dvojná vazba obsažená v molekulách nenasycených uhlovodíků je vystavena působení silných oxidačních činidel. Mají také elektrofilní charakter, používají se v chemickém průmyslu. Zvláštní význam má oxidace alkenů s vodným (nebo slabě alkalickým) roztokem. manganistan draselný. To se nazývá hydroxylační reakce v důsledku získání dvojmocných alkoholů.
Například ethylen-diol-1,2 (ethylenglykol) se získá oxidací molekul ethylenu vodným roztokem manganistanu draselného. Tato interakce je považována za kvalitativní reakci na dvojnou vazbu, protože během interakce je pozorována změna barvy roztoku manganistanu draselného.
V kyselém prostředí (v drsných podmínkách) se mezi reakčními produkty uvádí aldehyd.
Při interakci s atmosférickým kyslíkem je pozorována oxidace odpovídajícího alkenu na oxid uhličitý a vodní páru. Proces je doprovázen uvolněním tepelné energie, takže v průmyslu se používá k výrobě tepla.
Přítomnost dvojné vazby v molekule alkenu naznačuje možnost hydrogenačních reakcí v této třídě. Interakce SpN2p s molekulami vodíku nastává během tepelného použití jako katalyzátor platiny, niklu.
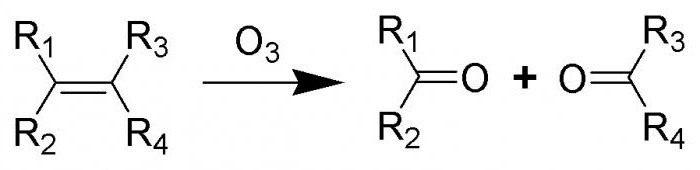
Mnozí zástupci třídy alkenů jsou náchylní k ozonaci. Při nízkých teplotách reagují zástupci této třídy s ozonem. Tento proces je doprovázen přerušením dvojité vazby, tvorbou cyklických peroxidových sloučenin nazývaných ozonidy. V jejich molekulách jsou přítomny vazby O-O, proto jsou látky výbušnými látkami. Ozonidy nejsou syntetizovány v čisté formě, rozkládají se procesem hydrolýzy a potom se redukují pomocí zinku. Výrobky této reakce jsou karbonylové sloučeniny izolovány a identifikovány výzkumnými pracovníky.
Polymerizace
Tato reakce zahrnuje postupnou integraci několika alkénových molekul (monomerů) do velké makromolekuly (polymeru). Z výchozího ethenu se získá polyethylen, který má průmyslové využití. Polymer je látka, která má vysokou molekulovou hmotnost.
Uvnitř makromolekuly je určitý počet opakujících se fragmentů, nazývaných strukturní jednotky. Pro polymeraci ethylenu se skupina -CH2-CH2- považuje za strukturní jednotku. Stupeň polymerace udává počet jednotek opakujících se v polymerní struktuře.
Stupeň polymerace určuje vlastnosti polymerních sloučenin. Například polyethylen s krátkým řetězcem je kapalina mající mazací vlastnosti. Pro makromolekuly s dlouhými řetězci je pevný stav zvláštní. Flexibilita a plasticita materiálu používaného při výrobě trubek, lahví, fólií. Polyethylen, jehož stupeň polymerace je pět až šest tisíc, má vysokou pevnost a proto se používá při výrobě odolných vláken, tuhých trubek, odlitků.
Z produktů získaných polymerací alkenů, které mají praktickou hodnotu, se volí polyvinylchlorid. Tato sloučenina se připraví polymerací vinylchloridu. Výsledný produkt má cenné výkonnostní charakteristiky. Je charakterizována zvýšenou odolností vůči agresivním chemikáliím, nehořlavou, snadno lakovanou. Co může být vyrobeno z polyvinylchloridu? Aktovky, pláštěnky, plátno, umělá kůže, kabely, izolace elektrických vodičů.
Teflon je produkt polymerace tetrafluorethylenu. Tato organická inertní sloučenina je odolná vůči náhlým změnám teploty.
Polystyren je elastická transparentní látka vytvořená polymerací původního styrenu. Je nepostradatelný při výrobě dielektrik v oblasti rozhlasu a elektrotechniky. Navíc se ve velkém množství používá polystyren pro výrobu kyselinovzdorných trubek, hraček, hřebenů, porézních plastů.
Vlastnosti získání alkenů
Zástupci této třídy jsou v moderním chemickém průmyslu poptáváni, proto byly vyvinuty různé metody pro jejich průmyslovou a laboratorní přípravu. V přírodě neexistuje ethylen a jeho homology.
Mnoho laboratorních možností pro získání zástupců této skupiny uhlovodíků je spojeno s inverzními adičními reakcemi, které se nazývají eliminaci (eliminace). Například při dehydrogenaci parafinů (nasycených uhlovodíků) se získají odpovídající alkény.
Při interakci halogenových derivátů alkanů s kovovým hořčíkem je také možné získat sloučeniny obecného vzorce SpH2n. Vyřazení se provádí podle pravidla Zaitseva, což je protiklad Markovnikova pravidla.
V průmyslových objemech se nenasycené uhlovodíky řady ethylenu získají krakováním ropy. Krakování plynů a pyrolýza ropy a plynu obsahuje deset až dvacet procent nenasycených uhlovodíků. Ve směsi reakčních produktů jsou parafiny a alkény, které jsou navzájem odděleny frakční destilací.
Některé aplikace
Alkenové jsou důležité třída organických sloučenin. Možnost jejich použití je způsobena vynikající reaktivitou, snadností výroby, přiměřenými náklady. Mezi mnoha průmyslovými odvětvími, která používají alkény, vyberte polymerní průmysl. Obrovské množství ethylenu, propylenu, jejich derivátů jde do výroby polymerních sloučenin.
Proto jsou otázky týkající se hledání nových způsobů výroby alkenových uhlovodíků tak důležité.
Polyvinylchlorid je považován za jeden z nejdůležitějších produktů pro použití odvozených od alkenů. Je charakterizována chemickou a tepelnou stabilitou, nízkou hořlavostí. Vzhledem k tomu, že tato látka není rozpustná v minerálech, ale je rozpustná v organických rozpouštědlech, může být použita v různých průmyslových odvětvích.
Jeho molekulová hmotnost je několik set tisíc. S rostoucí teplotou je látka schopná rozkladu a následně se uvolňuje chlorovodík.
Zvláštní význam mají dielektrické vlastnosti používané v moderní elektrotechnice. Mezi průmysly, ve kterých se používá polyvinylchlorid, lze vymezit výrobu umělé kůže. Výsledný materiál ve výkonu není v žádném případě nižší než přírodní materiál, zatímco má mnohem nižší náklady. Oděvy vyrobené z tohoto materiálu se stávají stále oblíbenější u módních návrhářů, kteří vytvářejí světlé a pestré kolekce oblečení pro mládež vyrobené z polyvinylchloridu v různých barvách.
Ve velkých množstvích se polyvinylchlorid používá jako těsnění v chladničkách. Díky své elasticitě, odolnosti je tato chemická sloučenina nezbytná při výrobě filmů a moderních strechových stropů. Omyvatelná tapeta je navíc pokryta tenkým PVC filmem. To jim umožňuje přidat mechanickou pevnost. Takové dokončovací materiály budou ideální volbou pro renovaci kancelářských prostor.
Kromě toho hydratace alkenů vede k tvorbě primárních a sekundárních jednosytných alkoholů, které jsou vynikajícími organickými rozpouštědly.