Chemické a fyzikální vlastnosti arény
Tam jsou organických sloučenin molekuly, které obsahují malý počet atomů vodíku, i když jejich uhlíkatý skelet je poměrně velký. Takové látky jsou považovány za vysoce nenasycené, nicméně nenastávají reakce charakteristické pro alkény nebo alkiny. Například, nezbarveny řešení. manganistan draselný nebo bromovou vodou. První chemici z této skupiny sloučenin byli látky s příjemným zápachem, takže se nazývaly aromatické. Existuje jiná jména - arény. Nomenklatura, izomerismus, získání a jejich fyzikální vlastnosti budou studovány v tomto článku.

Co je benzen
Nejjednodušší představitel arény je benzen. Molekulární vzorec látky - C6H6. Mezi ostatními aromatických uhlovodíků Má nejvíce praktický význam. Sloučenina objevila v roce 1825 anglický fyzik M. Faraday ve složení svítivého plynu. Je to bezbarvá kapalina, lehčí než voda (hustota 0,88 g / cm 3 ). Má charakteristický zápach, jedovatý. Bod varu - 80, zamrzne na 5,5. Fyzikální vlastnosti arény, stejně jako jiné organické látky, závisí nejen na kvalitativním a kvantitativním složení, ale také na struktuře jejich molekul.
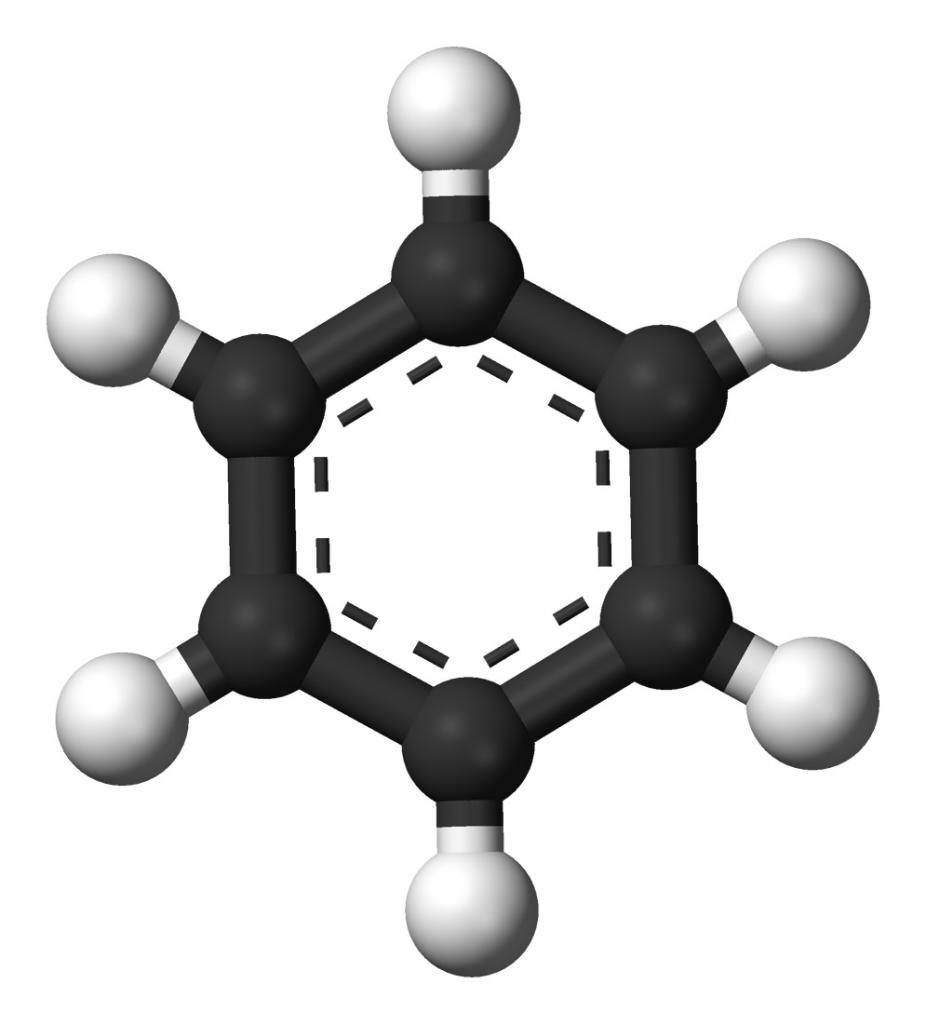
Riddle aromatického jádra
První strukturální vzorec této látky navrhl německý chemik Kekule. V něm atomy uhlíku leží ve stejné rovině a tvoří mezi sebou pravidelný šestiúhelník. Částice uhlíku v molekule jsou spojeny dvěma typy kovalentní vazby: Jeden a dvakrát, experimenty však nepotvrdily přítomnost p-vazeb v benzenu, protože látka nebyla oxidována roztoky bromové vody a manganistanu draselného. Vysvětlením tohoto rozporu je elektronická struktura hmoty. Ve své molekule existuje speciální typ chemické vazby, nazývané aromatické nebo jeden a půl. Je reprezentován společným elektronovým mrakem, který se skládá ze šesti vzájemně se překrývajících p-elektronů. Nachází se nad a pod rovinou molekuly, vazba má tvar prstence a nazývá se aromatickým jádrem. Jeden a půl vazba určuje fyzikální vlastnosti arény, stejně jako jejich schopnost substitučních a adičních reakcí.
Mechanismus procesu nahrazování
Systém aromatického jádra má zvýšenou elektronovou hustotu a může být vystaven účinkům elektrofilních částic s negativním nábojem. Výsledkem takového účinku bude nahrazení atomů vodíku jinými částicemi, například v benzenové molekule. Fyzikální vlastnosti arény a zvláštnosti chemických procesů jsou velmi odlišné od fyzikálních vlastností alkanů nebo alkenů. Navíc, na rozdíl od jiných tříd organických sloučenin, arény nemohou být popsány jedním obecným vzorcem. Takže pro naftalen bude vzorec následující: CnH2n-12 , pro benzen -CnH2n- 6 , pro difenyl- CnH2n -14.
Ad
Chlorace, bromace a nitrace aromatických uhlovodíků probíhají jediným mechanismem elektrofilní substituce, ve kterém chlor, brom nebo nitro skupiny hrají úlohu útočícího elektrofilního činidla.
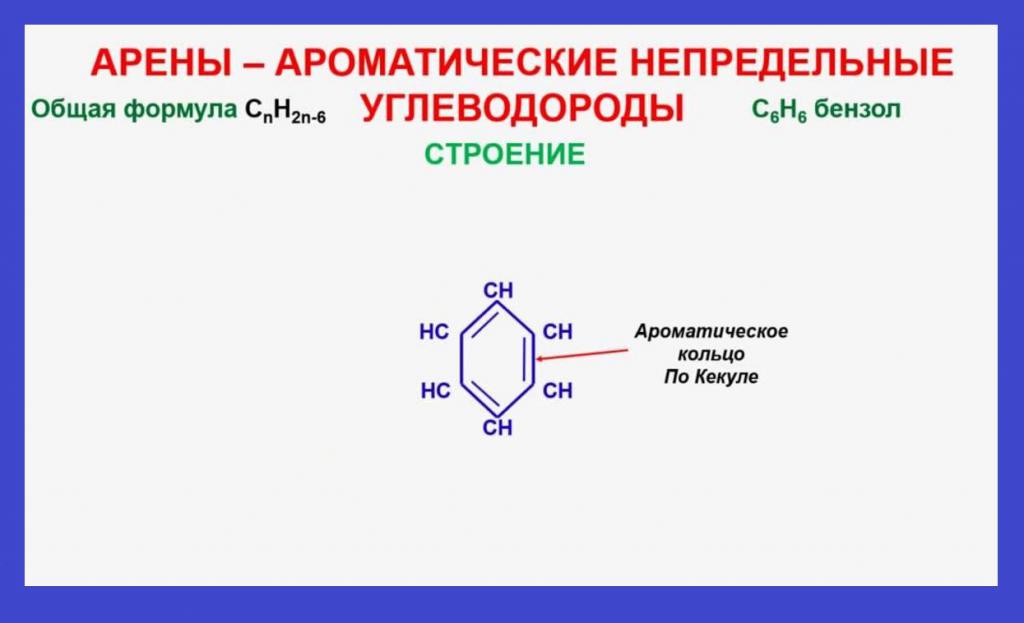
Proč přídavné reakce vyžadují drsné podmínky?
Hlavním rysem struktury molekul aromatických sloučenin je přítomnost benzenového kruhu v jejich molekulách, sestávající ze šesti překrývajících se p-elektronů. Hlavními chemickými charakteristikami a fyzikálními vlastnostmi arenes závisí. Pro rozbíjení jedné a půl komunikace je zapotřebí další významná část energie. Získává se pomocí následujících parametrů: ultrafialové záření, vysoká teplota a tlak v reakční směsi, stejně jako použití katalyzátorů. Například chlor se připojí k benzenu pouze při ozařování ultrafialovým světlem, čímž vznikne hexachlorcyklohexan (hexachloran). Používá se k oblékání dřeva při jeho dlouhodobém skladování, stejně jako v zemědělství jako prostředku k potírání hmyzích škůdců.

C6H6 + 3Cl2 --- lehký ---> C6H6Cl6 - přidání
Alkylbenzeny
Pokud jsou atomy vodíku v benzenové molekule nahrazeny uhlovodíkovými zbytky, například methyl-CH3 nebo ethyl-C2H5, pak výsledné aromatické uhlovodíky nebudou jednoduchým součtem vlastností alkanů a aren. Fyzikální vlastnosti a chemické reakce charakteristické pro tyto sloučeniny budou mít řadu rozdílů. Takto jsou toluen a ethylbenzen bezbarvé kapaliny se zvláštním zápachem, lehčí než voda a v nich nerozpustné. Ale látky jsou dobře rozpuštěny v organických rozpouštědlech, například v acetonu nebo dichlormethanu. Sami mohou být také použity jako rozpouštědla. Aromatické uhlovodíky mají také specifické vlastnosti. Povrchové napětí, difúzní koeficient, viskozita jsou fyzikální vlastnosti arény, stručně popisující jejich charakteristiky jako organická rozpouštědla.
Ad
Aromatická nitrace
Pod účinkem kyseliny dusičné a v přítomnosti kyseliny sírové jako katalyzátoru jsou arény nitrované. Reakce benzenu s dusíkovou směsí bude následující.
Nitrobenzen je světle žlutá olejovitá kapalina s charakteristickým mandlovým zápachem. Používá se jako rozpouštědlo a slouží jako surovina pro výrobu anilinu.
Při reakci kyseliny dusičné s toluenem vzniká výbušnina - trinitrotoluen nebo trotyl. Jako pyrogenní sloučeniny se používají a některé jiné. organické látky s benzenovými jádry obsahujícími několik vazeb v postranních řetězcích.
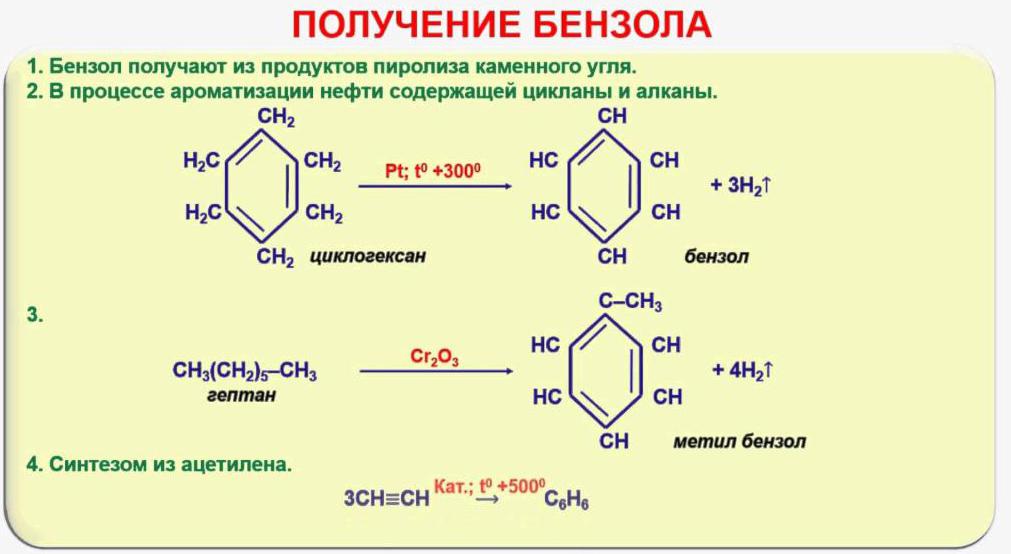
Získání a uplatňování arény
Fyzikální vlastnosti arenes: vysoká tepelná kapacita, hořlavost, schopnost rozpouštět jiné látky, jsou široce používány v různých hospodářských odvětvích. Benzen, toluen, naftalen, antracen a další aromatické uhlovodíky se získají z ropného nebo uhelného dehtu, který vzniká při koksování uhlí. Vzhledem k tomu, že průmyslová poptávka po arénách je obrovská, jsou těžit také metodou katalytické aromatizace uhlovodíků, které jsou součástí ropy a mají acyklickou strukturu. V tomto případě dochází k dehydrogenační reakci - eliminaci atomů vodíku, v důsledku čehož může být například benzen získán z hexanu. V chemii organické syntézy i nadále platí způsob výroby benzenu z acetylenu. Reakce se provádí zahříváním ethinu na 600 ° C a nazývá se trimerizace. Chemické a fyzikální vlastnosti arenes se používají v chemii při výrobě plastů, laků, barviv.

Benzen se používá jako přísada do paliva. V zemědělství slouží jako insekticidy sloučeniny - halogenové deriváty aromatických uhlovodíků - prostředky pro potírání hmyzích škůdců. Nitro sloučeniny, například trinitrotoluen, se používají ve vojenském průmyslu jako výbušniny. Mnohé arény jsou dobré rozpouštědla.
V našem článku jsme studovali chemické a fyzikální vlastnosti arény a určili oblasti použití těchto sloučenin v průmyslu.