Chemické a fyzikální vlastnosti alkynů
Alkyny jsou trojnásobné uhlovodíky. kovalentní vazbu mezi atomy uhlíku, které tvoří homologní série, vzorce CnH2n-2 . Částice samotné za takových podmínek jsou ve stavu sp-hybridizace. Toto je název procesu smíchání různých orbitálů (funkce jednovunových vln) s následným výskytem identických, ekvivalentních vlastností.
Fyzikální vlastnosti alkynů jsou jen málo, ale chemické vlastnosti jsou poměrně velké. Někteří i jiní si zaslouží pozornost.
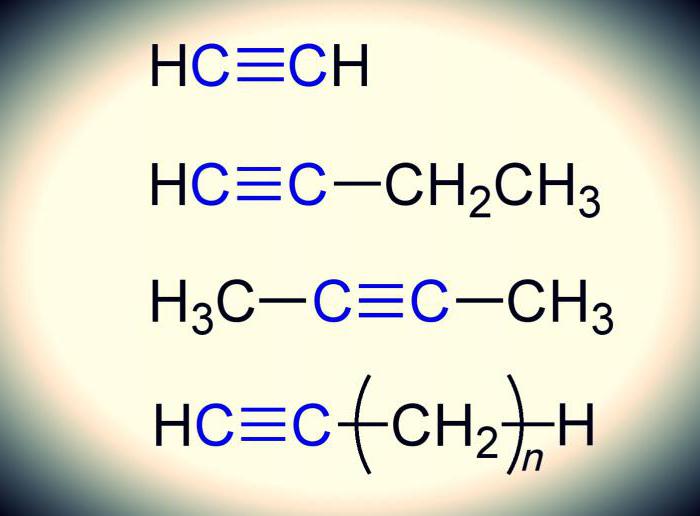
Podobnost s alkénami
Je to opravdu. Fyzikální vlastnosti alkynů jsou podobné těm, které jsou charakteristické pro alkény - acyklické nenasycené uhlovodíky s dvojnou vazbou. Vzorec je CnH2n .
Nižší alkiny jsou C2 - C4, jsou to plyny. Mají mírně vyšší teploty varu než podobné alkény.
Vzhledem k tomu, že tyto a další sloučeniny jsou uhlovodíky, rozpouštějí se špatně ve vodě. Jejich molekuly jsou hydrofobní. Organická rozpouštědla, jako je butanol, xylen, benzen, sulfid uhličitý a v mnoha dalších se rozpouštějí lépe.
Je třeba také poznamenat, že alkény a alkiny jsou méně husté než voda. Alkany, nasycené uhlovodíky s maximálním možným počtem atomů vodíku jsou také zahrnuty v tomto seznamu.
Chemické vlastnosti
Existuje mnoho z nich. A je také důležité si je všimnout s pozorností, protože mluvíme o fyzikálních a chemických vlastnostech alkynů. Stručně řečeno, tento seznam vypadá takto:
- Alkyny s koncovou trojnou vazbou jsou kyseliny C-H. Tvoří silné alkynidy se silnými bázemi.
- Pokud jsou spojeny s amoniovou monovalentní mědí nebo stříbrem, tvoří kvalitní odpověď s trojnásobnou vazbou terminálu.
- Přidáním kyanidu sodného do alkyndu stříbra lze získat alkyn.
- Alkinidy jsou silné nukleofily. Mohou vstupovat do různých nukleofilních substitučních reakcí. Který je mimochodem často použitelný pro syntézu acetylenových homologů - alkynu, jehož fyzikální vlastnosti budou projednány později.
- Chlorací acetylenu chloridem měďnatým se získá dichloracetylen. Pouze ve vodných roztocích CuCl.
- Pokud jednáte o monosubstituované acetylény s halogenem (energetickým oxidačním činidlem), budete schopni získat haloalkany.
Také tyto sloučeniny se mohou podílet na karbonylaci, ethynylaci, elektrofilním, radikálovém a nukleofilním přidávání, hydroboraci, oxidaci, izomeraci, oligomeraci, polymeraci, cykloformaci atd.

Etin
Fyzikální vlastnosti alkynů jsou nejlépe demonstrovány konkrétními příklady, které se týkají charakteristik zástupců této skupiny sloučenin.
Etin je bezbarvý plyn, nazývaný také acetylen. Vzorec - C 2 H 2 . Ve vodě, stejně jako jiný alkyn, nerozpustný. Lehčí než vzduch. Směří se při -83,8 ° C. Rozloženo kompresí s výbuchem. Etin se skladuje ve válcích naplněných buď aktivním uhlím impregnovaným acetonem nebo křemelinou (hornina sestávající z pozůstatků diatoms). Za takových podmínek se ethné rozpouští ve velkých množstvích pod tlakem.
Tento plyn nesmí být uvolňován do venkovního prostředí. Je to výbušná. Je zajímavé, že částice této sloučeniny byly nalezeny na Neptunu a Uranu.
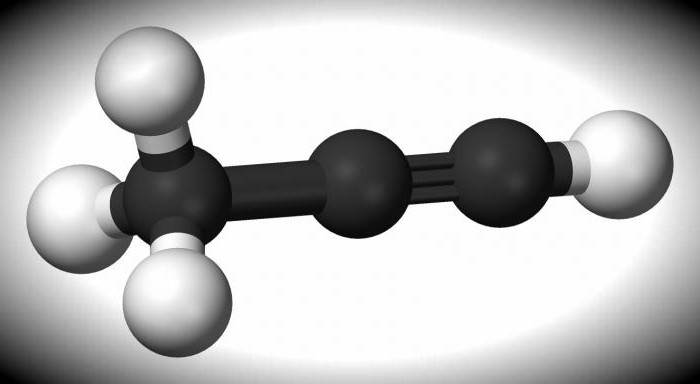
Propine
Vysoce hořlavý, bezbarvý plyn se vzorcem CH3-C≡CH. Má velmi nepříjemný a ostrý zápach. Chemické a fyzikální vlastnosti alkynu lze použít jako raketové palivo.
Tato látka se získá hydrolýzou karbidu hořečnatého. Také propylen je vedlejším produktem při výrobě acetylenu. Zde uvádíme některé fyzikální a tepelné vlastnosti této látky:
- Molární hmotnost - 40,06 k / mol.
- Hustota - 0,70 g / cm3.
- Bod tání je mínus 102,7 ° C.
- Bod varu - mínus 23,21 ° C.
- Entalpie vzdělání - 185,4 kJ / mol.
Když mluvíme o chemických vlastnostech, je třeba poznamenat, že propin může být izomerizován v přítomnosti silikátů nebo jiných katalyzátorů v allene - nejjednodušším zástupcem třídy homocumulenes, nenasycených organických sloučenin s kumulovanými uhlíkovými dvojnými vazbami.

Butin
Před uvedením fyzikálních vlastností alkinu známého pod tímto jménem je důležité poznamenat, že je charakterizován strukturní izomerismem. Má dva izomery:
- Butin-1. Bod tání je minus 125,9 ° C. Teplota varu při + 8,1 ° C Hustota - 0,678 g / cm³.
- Butin-2. Bod tání - mínus 32,3 ° C. Teplota varu je 27 ° C. Hustota - 0,694 g / cm³.
Jejich molární hmotnost je stejná - 54,09 g / mol. Ale existuje vlastnost butin-2, která není charakteristická pro jiný izomer. Vybuchne. A pro to potřebujeme teplotu -49. Za těchto podmínek vznikají výpary nad povrchem dané látky ve vzduchu pod vlivem zdroje zapálení. Neexistuje však žádné trvalé spalování.
Pentin
Tato sloučenina má také dva isomery:
- Pentin-1. Vzorec: CH = -C-CH2-CH2-CH3. Bod tání - mínus 90 ° C. Teplota varu je +39,3 ° C. Hustota je 0,695 d 20 4 .
- Pentin-2. Vzorec: CH3-C = C-CH2-CH3. Bod tání - mínus 101 ° C. Teplota varu při +55 ° C. Hustota je 0,714 d 20 4 .
Jinak jsou vlastnosti obou izomerů shodné se všemi, které byly uvedeny dříve. Nemají barvu a vůni, hoří, reagují na přídavek, mohou reagovat s vodíkem, lehčí než vzduch.
Mimochodem, protože mluvíme o fyzikálních vlastnostech alkenů a alkynů, je třeba poznamenat, že existuje ještě taková sloučenina - penten. Je to nenasycený uhlovodík se šesti izomery. Pentenes jsou nízkovroucí kapaliny, které se rozpouštějí pouze v organických rozpouštědlech. Jejich teplota tání činí -168,5 ° C až -137,56 ° C. Pro vaření je nutná teplota od + 20,06 ° C do + 38,57 ° C.

Alkanes
O těchto sloučeninách - konečně. S ohledem na fyzikální vlastnosti alkynů a alkény, alkany také nelze ignorovat. Jedná se o acyklické uhlovodíky s rozvětvenou nebo lineární strukturou s jednoduchými vazbami. Vzorec je CnH2n + 2 .
Nejjednodušším členem této třídy je metan. Bezbarvý plyn vzorce CH 4 , netoxický a bezpečný pro zdraví. Ale stane se explozivní, pokud se hromadí uvnitř. Zvláště pokud je koncentrace mezi 4,4% a 17%.
A co fyzické vlastnosti? Molární hmotnost - 16,05 g / mol. Hustota - 0,7168 kg / m³ v plynovém stavu. Taví se při -182,49 ° C a varu při -161,58 ° C. Může se samovolně vznítit, pokud teplota dosáhne 537,8 ° C.