Klasifikace termodynamických systémů
Zvažte vlastnosti termodynamických systémů. Pod nimi se běžně rozumí fyzikální makroskopické formy, sestávající z významného počtu částic, které nejsou určeny k popisu makroskopických parametrů každé jednotlivé částice.
Neexistují žádná omezení v povaze hmotných částic, které jsou nedílnou součástí takových systémů. Mohou být zastoupeny ve formě molekul, atomů, iontů, elektronů, fotonů.
Zvláštní funkce
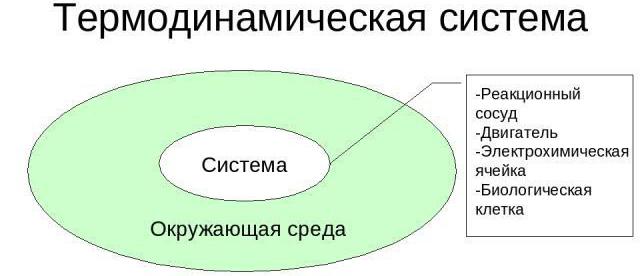
Analyzujme charakteristické vlastnosti termodynamických systémů. Jako příklad můžete vzít jakýkoli objekt, který lze pozorovat bez použití dalekohledu, mikroskopů. Pro úplný popis takového systému jsou vybrány makroskopické detaily, díky nimž lze určit objem, tlak, teplotu, elektrickou polarizaci, magnetickou indukci, chemické složení a hmotnost složek.
Pro všechny termodynamické systémy existují podmíněné nebo skutečné hranice, které je oddělují od životního prostředí. Místo toho často používají koncept termostatu, který je charakterizován tak vysokou hodnotou tepelné kapacity, že v případě výměny tepla s analyzovaným systémem zůstává teplotní index konstantní.
Systémová klasifikace
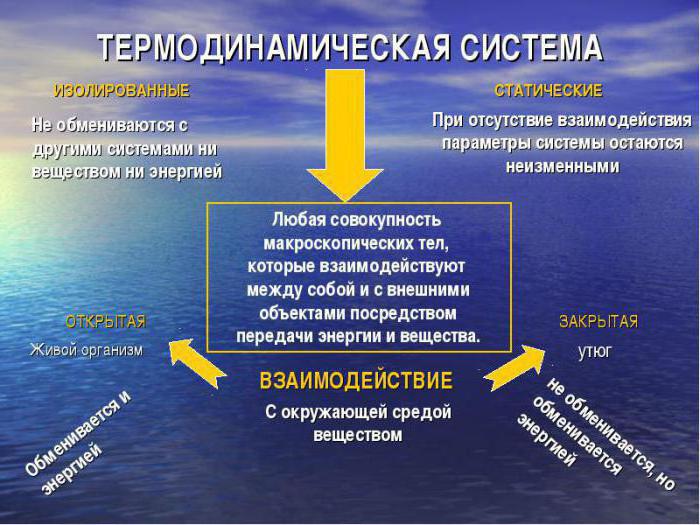
Zvažte, co představuje klasifikaci termodynamických systémů. V závislosti na povaze její interakce s prostředím je obvyklé vynechat:
- izolované druhy, které nevyměňují látku nebo energii s vnějším prostředím;
- adiabaticky izolované, nemění látku s vnějším prostředím, ale vstupuje do výměny práce nebo energie;
- uzavřené termodynamické systémy nemají žádnou výměnu látek, je povolena pouze změna energetické hodnoty;
- otevřené systémy se vyznačují úplným přenosem energie, hmoty;
- částečně otevřené mohou mít semipermeabilní oddíly, proto se plně neúčastní výměny materiálů.
V závislosti na popisu lze parametry termodynamického systému rozdělit na složité a jednoduché varianty.

Vlastnosti jednoduchých systémů
Jednoduché systémy se nazývají rovnovážné stavy, jejichž fyzikální stav lze určit specifickým objemem, teplotou, tlakem. Příklady termodynamických systémů tohoto typu jsou izotropní tělesa, která mají stejné charakteristiky v různých směrech a bodech. Takže kapaliny, plynné látky, pevné látky, které jsou ve stavu termodynamické rovnováhy, nejsou vystaveny elektromagnetickým a gravitačním silám, povrchovému napětí, chemickým přeměnám. Analýza jednoduchých těles je v termodynamice považována za důležitou a relevantní z praktického a teoretického hlediska.
Vnitřní energie termodynamický systém tohoto typu je spojen s okolním světem. Při popisu použití počtu částic je hmotnost látky každé jednotlivé složky.
Komplexní systémy
Komplex zahrnuje termodynamické systémy, které nespadají do jednoduchých forem. Jsou to například magnety, dielektrika, pevné elastické tělesa, supravodiče, povrchy rozhraní, tepelné záření, elektrochemické systémy. Jako parametry používané k jejich popisu je třeba poznamenat pružnost pružiny nebo tyče, povrch fázové části, tepelné záření.
Fyzikální systém se nazývá taková množina, ve které neexistuje žádná chemická interakce mezi látkami v mezích teploty, tlaku, vybraných pro studii. A chemické systémy volají ty možnosti, které zahrnují interakci mezi jednotlivými komponentami.
Vnitřní energie termodynamického systému závisí na přítomnosti jeho izolace vůči vnějšímu světu. Například jako varianta adiabatického pláště lze si představit Dewarská loď. Homogenní charakter se projevuje v systému, ve kterém všechny komponenty mají podobné vlastnosti. Příklady z nich jsou plynové, pevné, kapalné roztoky. Typickým příkladem plynné homogenní fáze je atmosféra Země.
Vlastnosti termodynamiky
Tato část vědy se zabývá studiem základních zákonů upravujících procesy spojené s uvolňováním, absorpcí energie. V chemické termodynamice je zamýšleno studovat vzájemné přeměny jednotlivých částí systému, stanovit zákony upravující přechod jednoho typu energie na jiný v daných podmínkách (tlak, teplota, objem).
Systém, který je předmětem termodynamického výzkumu, může být reprezentován jako jakýkoli objekt přírody, který zahrnuje velké množství molekul, které jsou odděleny rozhraním s jinými skutečnými objekty. Pod stavem systému vyplývá kombinace jeho vlastností, které umožňují jeho určení z hlediska termodynamiky.
Závěr
V každém systému dochází k přechodu jednoho druhu energie na druhou a nastává termodynamická rovnováha. Sekce fyziky kteří se zabývají podrobným studiem transformací, změnami, ochranou energie, mají zvláštní význam. Například v chemické kinetice je možné nejen popsat stav systému, ale také vypočítat podmínky vedoucí k jeho posunu správným směrem.
Hessův zákon, který se vztahuje k entalpii, entropii transformace, která je zvažována, umožňuje identifikovat možnost spontánní reakce, vypočítat množství uvolněného tepla (absorbovaného) termodynamickým systémem.
Termochemie založená na základech termodynamiky má praktický význam. Díky této části chemie se při výrobě provádí předběžné výpočty palivové účinnosti a proveditelnosti zavádění určitých technologií do reálné výroby. Informace získané z termodynamiky umožňují aplikovat jevy elasticity, termoelektrických vlastností, viskozity, magnetizace na průmyslovou výrobu různých materiálů.