Ionová vazba: příklady sloučenin
V důsledku vzájemné elektrostatické přitažlivosti mezi molekulami a atomy chemických prvků může dojít k iontové vazbě. Příklady takových sloučenin lze pozorovat při různých reakcích galvanických baterií, dokonce i jednoduchých sůl má sloučeninu tohoto typu. O tom, co je iontová vazba Jak se liší od kovalentní, popsané v tomto článku.
Jednoduché a komplexní ionty
Oba jednotlivé atomy a jejich různé sloučeniny se podílejí na iontové vazbě. Všichni účastníci takového spojení mají elektrický náboj a drženy spolu kvůli elektrostatickým silám. Existují jednoduché ionty, jako jsou Na + , K + , které jsou kationty; F - , Cl - - příbuzné s anionty. Také existují komplexní ionty sestávající ze dvou nebo více atomů. Příklady iontové chemické vazby založené na komplexních iontech jsou OH - , anionty, NO 3 - , kationtu NH 4+ . Jednoduché ionty s kladným nábojem jsou tvořeny atomy s nízkým ionizačním potenciálem - obvykle to jsou kovy hlavních podskupin skupin I - II. Jednoduché ionty s negativním nábojem jsou ve většině případů typické nekovy. 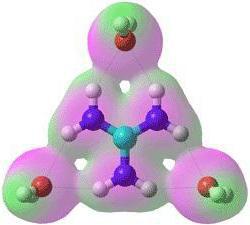
Kovalentní a iontová vazba
Příklady systémů vytvořených ze dvou částic s protilehlými elektrickými náboji ukazují, že v takovém případě vždy dochází k elektrickému poli. To znamená, že elektricky aktivní ionty mohou přitahovat i jiné ionty v různých směrech. Vzhledem k síle elektrického přitahování a iontové vazbě. Příklady takových sloučenin ukazují dva základní rozdíly mezi iontovými a kovalentními vazbami.
Ad
- Elektrické pole iontů se snižuje v závislosti na vzdálenosti v libovolném směru. Proto míra interakce mezi ionty nezávisí na tom, jak jsou tyto ionty umístěny v prostoru. Z těchto pozorování můžeme konstatovat, že iontová vazba je skalární, to znamená, že nemá směrovost.
- Dva ionty s různými náboji přitahují nejen sebe navzájem, ale i sousední nabité ionty - různý počet nabitých částic s opačným znaménkem se může připojit k určitému iontu. Jedná se o jiný rozdíl mezi kovalentními a iontovými vazbami: druhá nemá saturaci. Počet připojených iontů je určen lineárními rozměry nabitých částic, stejně jako princip, že přitažlivé síly iontů protilehlých nábojů by měly převládat nad odpuzujícími silami, které působí mezi rovnoměrně nabitými částicemi.
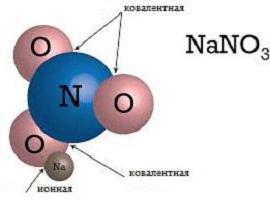
Sdružení
Vzhledem k tomu, že saturace a směrovost iontů chybí, mají sklon kombinovat se v různých kombinacích. Vědci této oblasti volali asociace. Při vysokých teplotách je asociace malá: kinetické energie molekuly a ionty jsou poměrně vysoké a v plynném stavu jsou látky s iontovým typem vazby ve formě jednotlivých molekul. Avšak střední a nízké teploty umožňují tvorbu různých strukturních sloučenin, jejichž tvorba je zodpovědná za iontový typ vazby. Příklady struktury látek v kapalném a tuhém stavu jsou uvedeny na obrázcích. 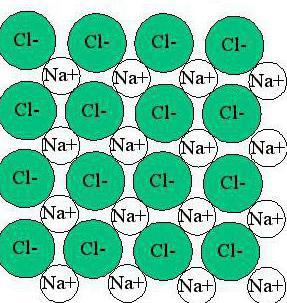
Jak vidíte, vytváří iontové pouto krystalová mřížka ve kterém každý prvek je obklopen ionty s opačným znaménkem náboje. Taková látka má navíc stejné vlastnosti v různých směrech.
Ad
Polarizace
Jak víte, když je elektron připojen k atomu nekovového, uvolní se určité množství energie. Připojení druhého elektronu však již vyžaduje energii, takže tvorba jednoduchých množstevně nabitých aniontů se stává energeticky nerentabilní. Prvky jako SO 4 2 , CO 3 2 však ukazují, že komplexní, vícenásobně nabité negativní ionty mohou být energeticky stabilní, protože elektrony v této sloučenině jsou distribuovány tak, že náboj každého atomu není větší než náboj samotného elektronu. Taková pravidla jsou diktována standardní iontovou vazbou.
Příklady typických prvků, ke kterým dochází v každém kroku (NaCl, CsF), nevykazují úplné oddělení pozitivních a záporných nábojů. Například v krystalu solí bude účinný záporný náboj jen asi 93% celkového náboje elektronu. Tento účinek je pozorován u jiných sloučenin. Toto neúplné oddělení náboje se nazývá polarizace. 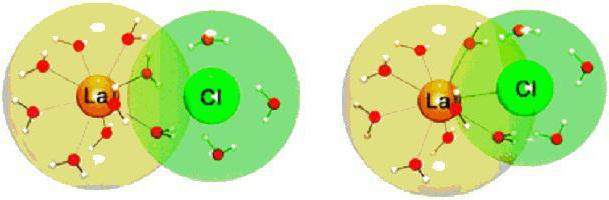
Příčiny polarizace
Příčinou polarizace je vždy elektrické pole. Vnější pole elektronů zažívá největší posun v průběhu polarizace. Mělo by se však poznamenat, že různé ionty mají odlišnou polarizovatelnost: čím je spojka vnějšího elektronu s jádrem slabší, tím jednodušší polarizace celého iontu a více deformace elektronového mraku.
Polarizace iontů má známý účinek na sloučeniny, které tvoří iontovou vazbu. Příklady chemických reakcí ukazují, že vodíkový iont H + má největší polarizační účinek, protože má nejmenší velikost a úplnou nepřítomnost elektronového mraku.