Koncept, vlastnosti a náboj elektronu
Elektron je elementární částice, která je jednou z hlavních jednotek ve struktuře látky. Elektronový náboj je negativní. Nejpřesnější měření bylo provedeno na počátku dvacátého století Millikenem a Ioffem.
Elektronový náboj je mínus 1,602176487 (40) * 10-19 Cl.
Přes tuto hodnotu se měří elektrický náboj další drobné částice.

Obecný pojem elektronu
Ve fyzice elementárních částic se říká, že elektron je nedělitelný a nestrukturovaný. Je zapojen do elektromagnetických a gravitačních procesů, patří do leptonové skupiny, stejně jako protipartikul - pozitron. Mezi ostatními leptony má nejlehčí hmotnost. Pokud se elektrony a pozitrony srazí, vede to k jejich zničení. Takový pár může vzniknout z částic gama-kvantum.
Ad
Než byly neutriny měřeny, byl to elektron, který byl považován za nejlehčí částice. V kvantové mechaniky se to označuje jako fermiony. Také elektron má magnetický moment. Je-li pozitron také odkazoval se na to, pak pozitron je rozdělen jako pozitivně nabitá částice, a elektron se nazývá negatron, jako částice s negativním nábojem.
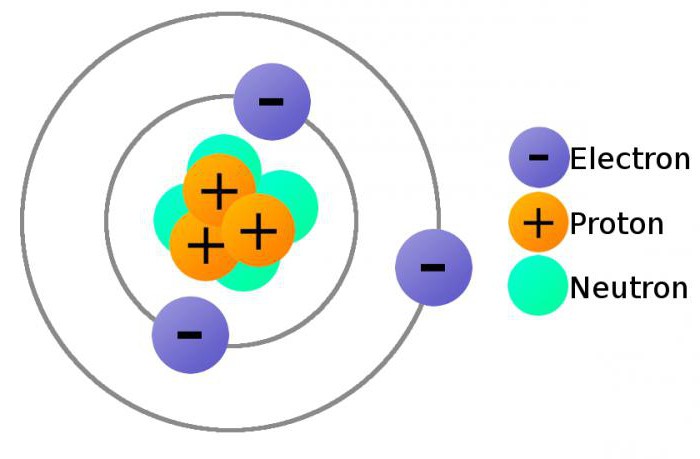
Oddělené vlastnosti elektronů
Elektrony patří k první generaci leptonů s vlastnostmi částic a vln. Každá z nich je vybavena kvantovým stavem, který je určen měřením energie, orientace točivého momentu a dalších parametrů. Působení na fermiony v něm je odhaleno skrze nemožnost být ve stejném kvantovém stavu současně s dvěma elektrony (podle principu Pauli).
Studie se provádí stejným způsobem jako kvazi-částice s periodickým krystalickým potenciálem, ve kterém se účinná hmota může výrazně lišit od hmotnosti v klidu.
Přes pohyb elektronů dochází elektrického proudu magnetismus a termo emf. Nabíjení elektronu v pohybu tvoří magnetické pole. Vnější magnetické pole však odvádí částici z přímého směru. Během zrychlení elektron získal schopnost absorbovat nebo emitovat energii jako foton. Jeho sada se skládá z elektronických atomových skořepin, jejichž počet a poloha určují chemické vlastnosti.
Ad
Atomová hmotnost se skládá hlavně z jaderných protonů a neutronů, zatímco elektronová hmota To je řádově 0,06% celkové atomové hmotnosti. Coulombova elektrická síla je jednou z hlavních sil schopných držet elektron v blízkosti jádra. Ale když molekuly jsou vytvořeny z atomů a vznikají chemické vazby elektrony jsou v nově vytvořeném prostoru redistribuovány.
Vzhled elektronů zahrnoval nukleony a hadrony. Izotopy s radioaktivními vlastnostmi mohou vysílat elektrony. V laboratorních podmínkách mohou být tyto částice studovány ve zvláštních zařízeních, například dalekohledy mohou detekovat záření z nich v plazmových mracích.
Discovery
Elektron byl objeven německými fyziky v devatenáctém století, kdy studovali vlastnosti katody v paprscích. Poté ho začali další vědci podrobněji studovat, čímž se dostali do hodnosti jediné částice. Byly studovány záření a další příbuzné fyzikální jevy.
Například skupina vedená Thomsonem odhadla elektronový náboj a hmotnost katodových paprsků, jejichž vztah, jak zjistil, nezávisí na zdroji materiálu.
Becquerel zjistil, že minerály emitují samotné záření a jejich beta paprsky se mohou odchylovat skrze působení elektrického pole a hmotnost a náboj udržují stejný poměr jako katodové záření.
Ad
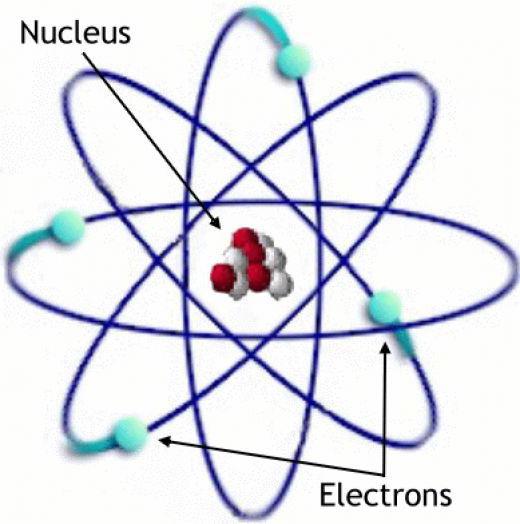
Atomová teorie
Podle této teorie se atom skládá z jádra a elektronů kolem něj, které se nacházejí v jako mrak. Jsou v jistých kvantovaných stavech energie, jejichž změna je doprovázena procesem absorpce nebo emisemi fotonů.
Kvantová mechanika
Na počátku dvacátého století byla formulována hypotéza, podle níž hmotové částice mají vlastnosti jak samotných částic, tak vln. Světlo se také může projevit ve formě vlny (nazývá se de Broglieova vlna) a částic (fotony).
V důsledku toho byla formulována slavná Schrödingerova rovnice, kde bylo popsáno šíření elektronových vln. Tento přístup se nazývá kvantová mechanika. Při jeho použití byly vypočítány elektronické stavy energie v atomu vodíku.
Základní a kvantové vlastnosti elektronu
Částice vykazují základní a kvantové vlastnosti.
Mezi základní patří hmotnost (9.109 * 10 - 31 kg), základní elektrický náboj (tj. Minimální část náboje). Podle dosud provedených měření nejsou v elektronu nalezeny žádné prvky, které by mohly odhalit jeho spodní strukturu. Někteří vědci se však domnívají, že jde o bodově nabitou částicu. Jak je uvedeno na začátku článku, elektronický elektrický náboj je -1,602 * 10 -19 Cl.
Ad
 Jako částice může být elektron současně vlnou. Experiment s dvěma štěrbinami potvrzuje možnost jeho současného průchodu oběma. To je v rozporu s vlastnostmi částice, kdy je vždy možné projít pouze jednou štěrbinou.
Jako částice může být elektron současně vlnou. Experiment s dvěma štěrbinami potvrzuje možnost jeho současného průchodu oběma. To je v rozporu s vlastnostmi částice, kdy je vždy možné projít pouze jednou štěrbinou.
Předpokládá se, že elektrony mají stejné fyzikální vlastnosti. Proto jejich permutace z hlediska kvantové mechaniky nevede ke změně stavu systému. Vlnová funkce elektronů je antisymetrická. Proto jeho řešení zmizí, když stejné elektrony spadají do stejného kvantového stavu (Pauliho princip).