Voda a její fyzikální a chemické vlastnosti. Struktura vody
Nejdůležitější podstatou naší planety, jedinečné svým vlastnostem a složením, je samozřejmě voda. Koneckonců, díky ní existuje život na Zemi, zatímco to není na jiných objektech dnešní známé sluneční soustavy. Tuhá, tekutá, ve formě páry - je to nezbytné a důležité. Voda a její vlastnosti jsou předmětem studia celé vědecké disciplíny - hydrologie.
Množství vody na planetě
Pokud vezmeme v úvahu indikátor množství tohoto oxidu ve všech agregačních stavech, pak to je asi 75% celkové hmotnosti na planetě. To by mělo brát v úvahu vázanou vodu v organických sloučenin živé bytosti, minerály a další prvky.

Pokud vezmete v úvahu pouze tekutý a pevný stav vody, rychlost klesne na 70,8%. Zvažte, jak jsou tyto procentní podíly rozděleny a které obsahují danou látku.
- Slaná voda v oceánech a mořích, slané jezero na Zemi 360 milionů km 2 .
- Čerstvá voda je rozložena nerovnoměrně: v ledovcích Grónska, Arktidy a Antarktidě je obklopena ledem o velikosti 16,3 milionu km2.
- V čerstvých řekách, bažinách a jezerech je koncentrováno 5,3 milionu km2 vodíku.
- Podzemní voda je 100 milionů m 3 .
To je důvod, proč astronauti ze vzdáleného vesmíru vidí Zemi ve formě modré koule s příležitostnými patami země. Voda a její vlastnosti, znalost vlastností struktury jsou důležitými prvky vědy. Navíc v posledních dobách začíná lidstvo pociťovat jasný nedostatek čerstvé vody. Snad takové znalosti pomohou při řešení tohoto problému.
Ad
Složení vody a struktura molekuly
Pokud uvažujeme o těchto ukazatelích, okamžitě se objeví vlastnosti, které tato úžasná látka projeví. Proto se molekula vody skládá ze dvou atomů vodíku a jednoho atomu kyslíku, proto má empirický vzorec H 2 O. Kromě toho elektrony obou prvků hrají důležitou roli při konstrukci samotné molekuly. Podívejme se, jaká je struktura vody a její vlastnosti.
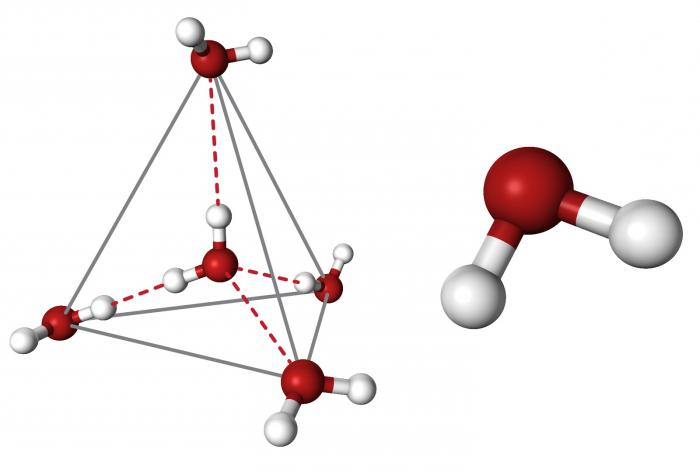
Je zřejmé, že každá molekula je orientována kolem druhé a společně tvoří společnou krystalovou mřížku. Zajímavé je, že oxid je vytvořen ve tvaru čtyřstěnu - atom kyslíku ve středu a dva páry jeho elektronů a dva vodíkové atomy kolem jsou asymetricky. Pokud nakreslíte čáru jádra atomů atomů atomů a spojíte je, získáte přesně geometrický geometrický tvar.
Ad
Úhel mezi středem atomu kyslíku a jádry vodíků je 104,5 ° C. Vazba je 0 - H = 0,0957 nm. Přítomnost elektronových párů kyslíku, stejně jako jejich větší elektronová afinita ve srovnání s vodíkem, zajišťuje tvorbu záporně nabitého pole v molekule. Naproti tomu jádra vodíků tvoří kladně nabitou část sloučeniny. Tak se ukazuje, že molekula vody je dipól. To určuje, jaká voda může být a její fyzikální vlastnosti závisí také na struktuře molekuly. Pro živé věci hrají tyto funkce zásadní roli.
Základní fyzikální vlastnosti
Ty se obvykle připisují krystalové mřížce, bodu varu a bodu tání, zvláštních individuálních vlastností. Všichni a zvážit.
- Struktura krystalové mřížky oxidu vodíku závisí na stavu agregace. Může se jednat o suchý led, kapalinu - hlavní vodu za normálních podmínek, plynnou páru, když teplota vody stoupne nad 100 ° C. Led tvoří krásné vzorované krystaly. Gril je obecně volný, ale kloub je velmi silný, hustota je nízká. Vidíte to na příkladu sněhových vloček nebo mrazivých vzorků na skle. V obyčejné vodě nemá mřížka trvalou podobu, mění se a přechází z jednoho státu do druhého.
- Molekula vody ve vesmíru má správný tvar koule. Při působení gravitace Země je ale zkreslená av kapalném stavu má tvar nádoby.
- Skutečnost, že struktura vodíkového oxidu je dipól, určuje následující vlastnosti: vysokou tepelnou vodivost a tepelnou kapacitu, které lze vysledovat při rychlém zahřátí a dlouhém ochlazení látky, schopnost orientovat se kolem sebe i iontů a jednotlivých elektronů, sloučenin. Toto činí vodu univerzální rozpouštědlo (polární i neutrální).
- Složení vody a struktura molekuly vysvětlují schopnost této sloučeniny tvořit více vodíkových vazeb, včetně jiných sloučenin, které mají osamocené elektronové páry (amoniak, alkohol a další).
- Teplota varu kapalné vody je 100 ° C, dochází k krystalizaci při + 4 ° C. Led je pod tímto indikátorem. Pokud zvýšíte tlak, pak bod varu vody dramaticky vzrůst. Takže ve vysokých atmosférách může být olovo taveno, ale současně ani neváří (nad 300 ° C).
- Vlastnosti vody jsou velmi důležité pro živé bytosti. Například jedním z nejdůležitějších je povrchové napětí. Jedná se o vytvoření nejtenčího ochranného filmu na povrchu oxidu vodíku. Jedná se o vodu v kapalném stavu. Je velmi obtížné tuto fólii zlomit mechanickým působením. Vědci zjistili, že je zapotřebí síla rovnající se 100 tunám. Jak si ji všimnout? Film je zřejmý, když voda pomalu proudí z kohoutku. Je vidět, že je to jako v nějakém druhu skořápky, který se rozprostírá na určitou hranici a váhu a vystupuje ve formě kulatých kapiček lehce deformovaných gravitací. Díky povrchovému napětí může být na povrchu vody mnoho předmětů. Hmyz se speciálními zařízeními se na ni může volně pohybovat.
- Voda a její vlastnosti jsou abnormální a jedinečné. Organoleptickými vlastnostmi této sloučeniny je bezbarvá kapalina bez chuti a zápachu. To, co říkáme chuť vody, jsou nerozpustné minerály a další složky.
- Vodivost oxidu vodíku v kapalném stavu závisí na tom, kolik a jaké soli se v něm rozpouštějí. Destilovaná voda neobsahující žádné nečistoty elektrického proudu neudržuje.
Led je zvláštní stav vody. Ve struktuře tohoto stavu jsou jeho molekuly navzájem propojeny vodíkovými vazbami a tvoří krásnou krystalickou mřížku. Ale je poměrně nestabilní a může snadno prasknout, roztavit, to znamená, deformovat se. Mezi molekulami se zachovává mnoho dutin, jejichž rozměry přesahují velikost samotných částic. Díky tomu je hustota ledu nižší než hustota kapalného vodíkového oxidu.
Ad

To má velký význam pro řeky, jezera a další sladkovodní útvary. Ve skutečnosti v zimním období voda v nich nezmrazuje úplně, ale pouze pokrývá hustá kůra lehčího ledu, který se vznáší. Pokud by tato vlastnost nebyla charakteristická pro tuhý stav oxidu vodíku, rezervoáry by zmrazily. Život ve vodě by byl nemožný.
Kromě toho je pevný stav vody velmi důležitý jako zdroj obrovského množství čerstvé pitné vody. Jedná se o ledovce.
Zvláštní vlastnost vody může být nazývána fenoménem trojitého bodu. Toto je podmínka, ve které mohou existovat současně led, pára a tekutina. To vyžaduje podmínky, jako jsou:
- vysoký tlak - 610 Pa;
- teplota 0,01 ° C
Index průhlednosti vody se mění v závislosti na nečistotách. Kapalina může být zcela průhledná, opalektivní, zakalená. Vlny žluté a červené barvy jsou absorbovány, fialové paprsky pronikají hluboko.

Chemické vlastnosti
Voda a její vlastnosti jsou důležitým nástrojem pro pochopení mnoha životních procesů. Proto jsou studovány velmi dobře. Takže hydrochemie má zájem o vodu a její chemické vlastnosti. Mezi ně patří:
Ad
- Tuhost Toto je vlastnost, která se vysvětluje přítomností vápenatých a hořečnatých solí a jejich iontů v roztoku. Rozdělí se na konstantu (soli jmenovaných kovů: chloridy, sírany, sulfity, dusičnany), dočasné (bikarbonáty), které jsou eliminovány vařením. V Rusku se voda chemicky upravuje, aby se zlepšila kvalita.
- Mineralizace. Vlastnost založená na dipólovém momentu oxidu vodíku. Díky své přítomnosti jsou molekuly schopné přilnout k sobě mnoho dalších látek, iontů a udržet je. Takto se vytvářejí kolegové, klatráti a další sdružení.
- Redox vlastnosti. Jako univerzální rozpouštědlo, katalyzátor, asociát, voda je schopna interagovat s mnoha jednoduchými a komplexními sloučeninami. S některými působí jako oxidační činidlo, s ostatními - naopak. Jak redukční činidlo reaguje s halogeny, solemi, některými méně aktivními kovy, s mnoha organické látky. Nejnovějšími transformacemi je studium organické chemie. Voda a její vlastnosti, zejména chemické, ukazují, jak je univerzální a jedinečná. Jako oxidační činidlo reaguje s aktivními kovy, některými binárními solemi, mnoha organickými sloučeninami, uhlíkem, metanem. Chemické reakce týkající se této látky obecně vyžadují výběr určitých podmínek. Od nich je závislost výsledku reakce.
- Biochemické vlastnosti. Voda je nedílnou součástí všech biochemických procesů těla, které jsou rozpouštědlem, katalyzátorem a médiem.
- Interakce s plyny při tvorbě klatrátů. Pravidelná tekutá voda může absorbovat i neaktivní chemické plyny a lokalizovat je uvnitř dutin mezi molekulami vnitřní struktury. Takové sloučeniny se nazývají klatráty.
- U mnoha kovů vytváří oxid vodíku krystalické hydráty, ve kterých je zabudován nezměněný. Například síran měďnatý (CuSO4 * 5H2O), stejně jako běžné hydráty (NaOH * H 2 O a další).
- Pro vodu jsou typickými reakcemi sloučeniny, u kterých dochází k tvorbě nových tříd látek (kyselin, zásad, zásad). Nejsou redoxní.
- Elektrolýza. Při působení elektrického proudu se molekula rozkládá na směsné plyny - vodík a kyslík. Jedním ze způsobů, jak je dostat do laboratoře a průmyslu.
Z pohledu Lewisovy teorie je voda slabou kyselinou a slabou základnou současně (amfolytem). To znamená, že můžeme říci o nějakém amfoterickém chemickém charakteru.
Ad

Voda a její prospěšné vlastnosti pro živé bytosti
Je těžké přecenit význam oxidu vodíku pro všechny živé věci. Koneckonců voda je zdrojem života. Je známo, že bez ní by člověk nemohl žít týden. Voda, její vlastnosti a hodnota jsou prostě kolosální.
- Je univerzální, tj. Schopná rozpouštět jak organické, tak i anorganické sloučeniny, rozpouštědlo působící v živých systémech. Proto je voda zdrojem a prostředkem pro tok všech katalytických biochemických transformací s tvorbou komplexních vitálních komplexních sloučenin.
- Schopnost vytvářet vodíkové vazby činí tuto látku univerzální při udržování teplot bez změny stavu agregace. Pokud tomu tak není, pak se při nejmenším poklesu stupňů změní na led v živých bytostech, což způsobí smrt buněk.
- Pro lidi je voda zdrojem všech základních potřeb a potřeb pro domácnost: vaření, mytí, čištění, koupání, koupání a koupání a tak dále.
- Průmyslové podniky (chemické, textilní, strojírenské, potravinářské, rafinérské a jiné) by nebyly schopny provádět svou práci bez účasti oxidů vodíku.
- Od starověku se věřilo, že voda je zdrojem zdraví. Používá se a dnes se používá jako léčebná látka.
- Rostliny ji používají jako hlavní zdroj výživy, kvůli které produkují kyslík - plyn, který dělá život na naší planetě.
Existují desítky dalších důvodů, proč je voda nejrozšířenější, důležitější a nezbytnou látkou pro všechny živé a uměle vytvořené objekty. Přinesli jsme jen ty nejzřetelnější, ty hlavní.

Hydrologický vodní cyklus
Jinými slovy je to její cirkulace v přírodě. Velmi důležitý proces, který vám umožňuje neustále doplňovat mizící zásoby vody. Jak to jde?
Hlavními účastníky jsou tři: podzemní vody (nebo podzemní vody), povrchové vody a oceány. Koncentrace atmosféry a vynikající srážky jsou také důležité. Aktivními účastníky procesu jsou také rostliny (zejména stromy), které mohou absorbovat obrovské množství vody denně.
Takže proces je následující. Podzemní vody plní podzemní kapiláry a hejny na povrch a Světový oceán. Poté je povrchová voda absorbována rostlinami a přepravována do životního prostředí. Odpařování také dochází z velkých oblastí oceánů, moří, řek, jezer a dalších vodních útvarů. Jakmile do atmosféry, co dělá voda? Kondenzované a rozlité zpět jako srážky (déšť, sníh, krupobití).
Pokud by tyto procesy nedošlo, zásoby vody, zejména sladké vody, by se dlouho vyčerpaly. To je důvod, proč lidé věnují velkou pozornost ochraně a normálnímu hydrologickému cyklu.
Pojem těžké vody
V přírodě existuje oxid vodíku jako směs isotopologů. To je dáno skutečností, že vodík tvoří tři typy izotopů: protium 1 N, deuterium 2 N, tritium 3 N. Kyslík naopak také nezůstává a tvoří tři stabilní formy: 16 O, 17 O, 18 O. Je to způsobeno není to jen obvyklá propiová voda složená z H 2 O ( 1 H a 16 O), ale také deuteria a tritia.

Současně je deuterium ( 2 N) stabilní ve struktuře a formě, které je obsaženo téměř ve všech přírodních vodách, avšak v malých množstvích. To je nazýváno těžké. To se mírně liší od obvyklých nebo snadných pro všechny indikátory.
Těžká voda a její vlastnosti jsou charakterizovány několika body.
- Krystalizuje při teplotě 3,82 ° C.
- Teplota varu je 101,42 ° C.
- Hustota je 1,1059 g / cm3.
- Jako rozpouštědlo je několikrát horší než lehká voda.
- Má chemický vzorec D 2 O.
Při provádění experimentů, které ukazují vliv takové vody na živé systémy, bylo zjištěno, že v ní mohou žít pouze určité druhy bakterií. Čas potřeboval kolonie k adaptaci a aklimatizaci. Ale po přizpůsobení zcela obnovili všechny životně důležité funkce (reprodukce, výživa). Kromě toho je ocel velmi odolná vůči záření. Experimenty na žábech a rybách neposkytly pozitivní výsledek.
Moderní oblasti použití deuteria a těžké vody, kterou tvoří, jsou atomová a jaderná energetika. V laboratorních podmínkách může být tato voda získána běžnou elektrolýzou - je vytvořena jako vedlejší produkt. Vlastní deuterium je tvořeno opakovaným destilací vodíku ve speciálních zařízeních. Jeho aplikace je založena na schopnosti zpomalit syntézu neutronů a protonové reakce. Právě těžké vodní a vodíkové izotopy jsou základem pro vytvoření jaderné a vodíkové bomby.
Pokusy o použití deuteriové vody lidmi v malých množstvích ukázaly, že dlouho nezůstává - po dvou týdnech je zaznamenáno úplné závěry. Používejte jej jako zdroj vlhkosti pro život je nemožné, ale technická hodnota je prostě obrovská.
Tavná voda a její aplikace
Vlastnosti takové vody od starověku byly definovány lidmi jako léčivé. Dlouho bylo zjištěno, že když se sněh roztaví, zvířata se pokoušejí vypít vodu z vytvořených kaluží. Později byla důkladně prozkoumána její struktura a biologické účinky na lidské tělo.

Tavná voda, její znaky a vlastnosti jsou uprostřed mezi normálním světlem a ledem. Zevnitř je tvořena nejen molekulami, ale soustavou klastrů tvořených krystaly a plynem. To znamená, že vodík a kyslík jsou uvnitř prázdných míst mezi konstrukčními částmi krystalu. Obecně platí, že struktura vody z taveniny je podobná struktuře ledu - konstrukce je zachována. Fyzikální vlastnosti takového oxidu vodíku se mírně liší oproti obvyklému. Biologické účinky na tělo jsou však vynikající.
Když je voda zmrazená první frakcí, těžší část se změní na led - to jsou izotopy deuteria, soli a nečistoty. Toto jádro by proto mělo být odstraněno. Ale zbytek je čistá, strukturovaná a zdravá voda. Jaký je účinek na tělo? Následující typy zlepšení byly jmenovány vědci Výzkumného ústavu v Doněcku:
- Zrychlení procesů obnovy.
- Posílení imunity.
- U dětí se po vdechnutí takovou vodou objevuje zotavení a vyléčení nachlazení, kašel, rýma a tak dále.
- Zlepšené dýchání, laryngeální a slizniční membrány.
- Obecné blaho člověka, aktivita se zvyšuje.
Dnes existuje řada příznivců léčby tavení vodou, kteří píší své pozitivní recenze. Existují však vědci, včetně lékařů, kteří tyto názory nepodporují. Věří, že z takové vody nedojde k žádnému úpadku, ale je málo výhod.
Energetika
Proč se vlastnosti vody mohou měnit a obnovit při přesunu do jiného stavu agregace? Odpověď na tuto otázku je následující: toto spojení má vlastní informační paměť, která zaznamenává všechny změny a vede k obnově struktury a vlastností ve správný čas. Oblast bioenergie, kterou prochází část vody (která pochází z vesmíru), nese silný náboj energie. Tento vzor se často používá při léčbě. Nicméně, z lékařského hlediska, ne každá voda může mít příznivý účinek, včetně informací.
Strukturovaná voda - co to je?
Jedná se o takovou vodu, která má mírně odlišnou strukturu molekul, umístění krystalových mřížek (jak je pozorováno u ledu), ale stále je to kapalina (rozmrazování se také vztahuje na tento typ). V tomto případě není složení vody a její vlastnosti vědecky odlišné od těch, které jsou typické pro obyčejný oxid vodíku. Proto strukturovaná voda nemůže mít tak široký terapeutický účinek, který se připisuje jejímu esoterickému a obhájcům alternativní medicíny.