Jaký vzorec má kyselinu jablečnou a jak ji získáváte?
Druhým názvem pro kyselinu jablečnou je kyselina hydroxytarová. Je členem třídy hydroxydikarboxylových kyselin. Sloučeninu nejprve získal Karl Scheele (švédský chemik) z nezralých jablek (který určil jeho jméno) v roce 1785. Také v přírodě se nachází v hroznech, borůvkách, horském popela, malinách atd. Ve formě solí nazývaných maláty je látka obsažena v tabáku. Maximální obsah hydroxycyklické kyseliny spolu s kyselinou citronovou v nezralých zelených jablkách dosáhne 1,2%.

Kyselina malicová: vzorec
Tato chemická sloučenina má následující vzorec:
HOOC-CH 2 -CH (OH) -COOH nebo C 4H 3O 2 (OH) 3
Za normálních podmínek je kyselina jablečná bezbarvý krystalický prášek, který se dobře rozpouští v alkoholu (ve 100 ml - 35,9 g) a ve vodě (ve 100 ml - 144 g). Molekulová hmotnost sloučeniny rovnající se 134,1 g / mol.
Obrázek níže ukazuje prostorovou strukturu molekuly kyseliny jablečné. Uhlíkové atomy jsou označeny černě, kyslík je v červené barvě, vodík je bílý.
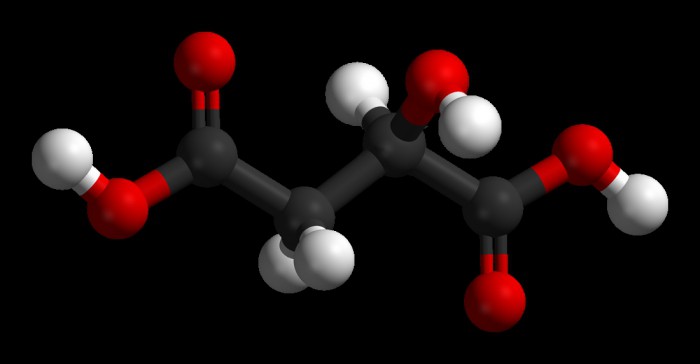
Kyselina jablečná existuje ve formě racemátu (opticky neaktivní sloučeniny) a dvou stereoizomerů. Posledně jmenované jsou takové sloučeniny, jejichž molekuly obsahují mezi atomy stejnou sekvenci chemických vazeb, ale existují rozdíly v uspořádání v prostoru vzhledem k sobě navzájem. Tento problém podrobně popisuje stereochemii. V kyselině jablečné existují dva stereoizomery, což je jejich příkladem, že P. Walden byl prvním, kdo v roce 1896 ukázal, že jsou možné interkonverze enantiomerů. Studium tohoto jevu sloužilo jako základ pro následné vytvoření teorie reakce tzv. Nukleofilní substituce na atomu uhlíku (nasycený).
Získání
Látka se získává dvěma způsoby: přírodní a chemická. První nabízí extrakci z ovoce a bobulí. Syntetická kyselina jablečná se získá několika reakcemi:
1. Hydratace kyseliny maleinové nebo kyseliny fumarové. Předpokladem je teplota 100-150 ° C. Reakční rovnice je následující:
HOOCCH = CHCOOH + H 2O → NOEP-CH 2 -CH (OH) -COOH
2. Hydrolýza kyseliny bromo- nebo chlor-jantarové. Kyselina jablečná se extrahuje etherem. Používá rostlinný materiál.
Kyselina jablečná. Interakční reakce

1. Oxidace koncentrované kyseliny sírové (H2SO4) s tvorbou kyseliny kumalínové. Reakce probíhá ve dvou fázích:
HOOC-CH2-CH (OH) -COOH + H2S04-> HOOC-CH2-CHO + HCOOH
Výsledkem je aldehyd malonický a kyseliny mravenčí. Tato druhá sloučenina se rozkládá oxid uhelnatý a voda:
HCOOH → CO + H2O
Aldehydová kyselina malonová se okamžitě převede na kyselinu kumalinovou.
2. Interakce s kyselina chlorovodíková :
HOOC-CH 2 -CH (OH) -COOH + HCl-HOOC-CH 2-CHCl-COOH
Výsledná látka se nazývá 2-chloranthin.
3. Kyselina jablečná je náchylná k oxidaci (zejména při použití KMnO4):
HOOC-CH 2 -CH (OH) -COOH + KMnO 4 → HOOC-CH 2-CO-COOH
Výsledná kyselina se nazývá 2-oxo-jantarová (oxy-octová).
4. Interakce s acetylchloridem za vzniku kyseliny 2-acetoxyjantarové:
HOOC-CH2-CH (OH) -COOH + CH3COCI-> HOOC-CH2-CH (OCOCH3) -COOH
Při postupném zahřátí se kyselina jablečná rozkládá, aby vytvořila řadu meziproduktů. Při teplotě 100 ° C nastává tvorba anhydridů (jsou podobné laktidům). Při zvýšení na 140-150 ° C se převedou na kyselinu fumarovou. Při rychlém zvýšení teploty na 180 ° C se získá anhydrid kyseliny maleinové.
Shrnutím všech údajů lze říci, že chemické vlastnosti kyseliny jablečné jsou stejné jako u jiných hydroxykyselin.
Biologická role
Kyselina jablečná je zapojena do Krebsova cyklu. Představuje hlavní fázi v dýchání všech buněk, které používají kyslík, a je mezilehlá vazba mezi glykolýzou a elektrickým dopravním řetězcem. Hlavním úkolem cyklu trikarboxylových kyselin (Krebs) je syntéza redukovaných koenzymů FAD * H2 a NAD * H. Následně se používají k výrobě ATP, ADP a fosfátu. Kyselina hydroxyvinná je tvořena hydratací fumarovou kyselinou. Jeho následná oxidace s NAD + doplňuje Krebsův cyklus. Katalyzujícím enzymem je malát dehydrogenasa.

Oblasti použití
Získaná komerčně kyselina jablečná je poměrně široce používána:
- V potravinářském průmyslu je známá pod kódem E296. Látka používaná jako konzervační látka. zesilovač chuti a regulátor kyselosti. Hlavní použití: nápoje sycené oxidem uhličitým, ovocné šťávy, cukrovinky, víno, konzervy. Je třeba zdůraznit, že v malých množstvích má kyselina jablečná pozitivní vliv na tělo.
- V kosmetologii. Oxycytová kyselina má antioxidační, bělící, exfoliační a zvlhčující vlastnosti, které jí umožňují používat jako součást anticelulitidového a bělicího činidla, peelingu. Kromě toho je přidávána do zubních past a výrobků pro péči o ústní dutinu.
- Ve farmakologii se kyselina jablečná (vzorec je uvedena výše) používá ve složení expektorantu a laxativ.