Aldehydy a ketony. Vzorec, příprava, aplikace
Mezi organickými sloučeninami obsahujícími kyslík jsou obzvlášť důležité dvě třídy látek, které jsou vždy studovány společně pro podobnost struktury a prokázaných vlastností. Jedná se o aldehydy a ketony. Tyto molekuly jsou základem mnoha chemických syntéz a jejich struktura je dostatečně zajímavá pro studium. Podívejme se podrobněji na to, jaké jsou tyto třídy sloučenin.

Aldehydy a ketony: obecné charakteristiky
Z hlediska chemie by měla skupina aldehydů zahrnovat organické molekuly obsahující kyslík ve funkční skupině -SON, nazývané karbonyl. Obecný vzorec v tomto případě vypadá takto: R-COH. Jejich povahou mohou být jak omezující, tak nenasycené sloučeniny. Mezi nimi jsou také aromatické zástupce spolu s alifatickými. Počet atomů uhlíku v radikálovém řetězci se pohybuje v poměrně širokém rozmezí, od jednoho (formaldehydu nebo methanu) až po několik desítek.
Ketony také obsahují karbonylovou skupinu -CO, ale nejsou spojeny s kationtem vodíku, ale s odlišným radikálem, který je jiný nebo identický s tím, co vstupuje do řetězce. Obecný vzorec je následující: R-CO-R. Je zřejmé, že aldehydy a ketony jsou podobné v přítomnosti funkční skupiny tohoto prostředku.
Ketony mohou být také omezující a nenasycené a projevené vlastnosti jsou podobné blízce příbuzné třídě. Existuje několik příkladů, které ilustrují složení molekul a odrážejí přijatelná označení vzorců uvažovaných látek.
- Aldehydy: methanal-HCl, butanal-CH3-CH2-CH2-COH, fenyloctová - C6H5-CH2-COH.
- Ketony: aceton nebo dimethylketon - CH3-CO-CH3, methylethylketon - CH3-CO-C2H5 a další.
Je zřejmé, že název těchto sloučenin je tvořen dvěma způsoby:
- podle racionální nomenklatury podle radikálů a přípony třídy -al (pro aldehydy) a -one (pro ketony);
- triviálně, historicky.
Pokud dáte obecný vzorec pro obě skupiny látek, bude jasné, že jsou navzájem izomery: C n H 2n O. Pro sebe jsou charakteristické následující typy isomerismu:
- pro ketony, strukturu uhlovodíkového řetězce radikálu a polohu skupiny -CO;
- pro aldehydy - pouze uspořádání atomů v řetězci.

Chcete-li rozlišovat mezi zástupci obou tříd, použijte kvalitativní reakce z nichž většina nám umožňuje identifikovat aldehyd. Vzhledem k tomu, že chemická aktivita těchto látek je poněkud vyšší kvůli přítomnosti kationtu vodíku.
Molekulární struktura
Zvažte, jak vypadají aldehydy a ketony ve vesmíru. Struktura molekul může být odrazena v několika bodech.
- Uhlíkový atom přímo obsažený ve funkční skupině má sp2 hybridizaci, která umožňuje, aby část molekuly měla plochý prostorový tvar.
- V tomto případě je polarita vazby C = O silná. Jako více elektrogativní, kyslík přebírá většinu své hustoty a koncentraci částečně negativního náboje na sebe.
- V aldehydech je vazba OH také vysoce polarizovaná, což činí atom vodíku mobilní.
Výsledkem je, že taková struktura molekul dovoluje, aby byly tyto sloučeniny oxidovány a sníženy. Vzorec aldehydu a ketonu s redistribuovanou elektronovou hustotou umožňuje předpovědět reakční produkty, v nichž se tyto látky účastní.
Dějiny objevu a studia
Stejně jako mnoho organických sloučenin to bylo teprve v 19. století, kdy se lidé podařilo izolovat a studovat aldehydy a ketony, když se vitální pohled zcela zhroutil a bylo zřejmé, že tyto sloučeniny mohou být tvořeny syntetickými, umělými prostředky bez účasti živých bytostí.
V roce 1661 se však R. Boyle podařilo získat aceton (dimethylketon), když podrobil octanu vápenatému zahřátí. Ale nemohl podrobně studovat tuto látku a pojmenovat ji, určit mezi ostatními systematickou pozici. Teprve v roce 1852 se Williamsonovi podařilo tuto záležitost ukončit, pak začala historie detailního vývoje a hromadění znalostí o karbonylových sloučeninách.

Fyzikální vlastnosti
Zvažte fyzikální vlastnosti aldehydů a ketonů. Začněme první.
- Podle stavu agregace je prvním zástupcem methan, další jedenáct jsou kapaliny, více než 12 atomů uhlíku je součástí pevných aldehydů normální struktury.
- Bod varu: závisí na počtu atomů C, čím více jsou, tím vyšší je. Navíc, čím větším řetězcem, tím nižší je hodnota teploty.
- Pro kapalné aldehydy, viskozita, hustota a refrakční indexy také závisí na počtu atomů. Čím víc, tím jsou vyšší.
- Plynné a kapalné aldehydy se velmi dobře rozpouštějí ve vodě, nicméně tuhé látky prakticky nemohou udělat.
- Vůně zástupců je velmi příjemná, často je to vůně květin, parfému, ovoce. Pouze ty aldehydy, jejichž počet atomů uhlíku je 1 až 5, jsou silně a nepříjemně voní kapaliny.
Pokud určíte vlastnosti ketonů, můžete také vybrat ty hlavní.
- Agregátní stavy: nižšími představiteli jsou kapaliny, čím větší jsou tuhé sloučeniny.
- Vůně je ostrá, nepříjemná pro všechny zástupce.
- Rozpustnost ve vodě je vhodná pro nižší, je vynikající pro všechny v organických rozpouštědlech.
- Prchavé látky, tento indikátor přesahuje obsah kyselin, alkoholů.
- Teplota varu a teplota tání závisí na struktuře molekuly, velmi se liší počtem atomů uhlíku v řetězci.
Jedná se o hlavní vlastnosti uvažovaných sloučenin, které patří do skupiny fyzikálních.
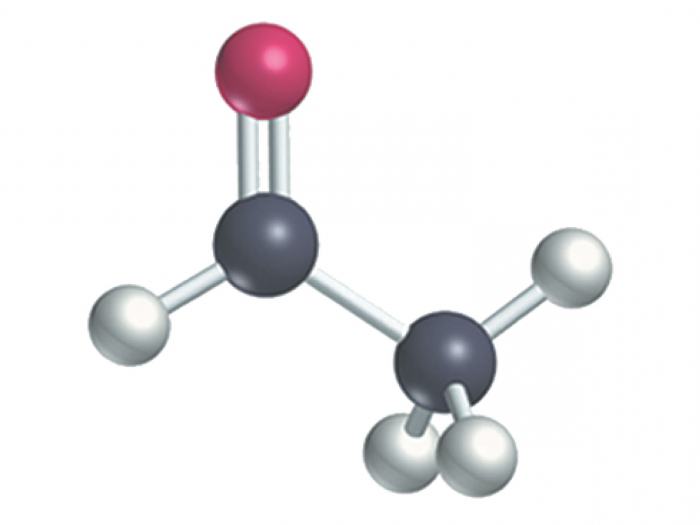
Chemické vlastnosti
Nejdůležitější je to, s čím reagují aldehydy a ketony, chemické vlastnosti těchto sloučenin. Proto je nutně považujeme. Nejprve řešit aldehydy.
- Oxidace na odpovídající karboxylové kyseliny. Obecný pohled na reakční rovnici: R-COH + [O] = R-COOH. Aromatická reprezentanti se ještě snadněji dostanou do takových interakcí a mohou také vytvářet estery průmyslového významu. Jako oxidační činidla se používají: kyslík, Tollensovo činidlo, hydroxid měďnatý a další.
- Aldehydy se projevují jako silné redukční činidla, přeměňují se na limitní monohydrické alkoholy.
- Interakce s alkoholy za vzniku produktů acetalů a hemiacetalů.
- Zvláštní reakce - polykondenzace. V důsledku toho se vytvářejí fenol-formaldehydové pryskyřice, které jsou důležité pro chemický průmysl.
- Několik specifických reakcí s následujícími činidly:
- vodné alkoholové alkálie;
- Grignardovo činidlo;
- hydrosulfity a další.
Kvalitní reakcí na tuto třídu látek je reakce "stříbrného zrcadla". Výsledkem je kovové stříbro a odpovídající karboxylová kyselina. Vyžaduje roztok amoniaku oxidu stříbrného nebo činidla Tollins.
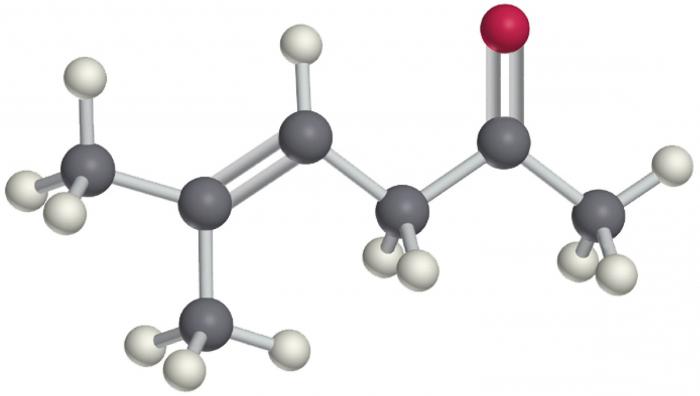
Chemické vlastnosti ketonů
Alkoholy, aldehydy, ketony jsou ve svých vlastnostech sloučenin podobné, neboť všechny obsahují kyslík. Nicméně již ve fázi oxidace je jasné, že alkoholy jsou nejaktivnější a snadno citlivé sloučeniny. Ketony jsou nejobtížnější oxidovat.
- Oxidační vlastnosti. V důsledku toho se tvoří sekundární alkoholy.
- Hydrogenace vede také k výše uvedeným produktům.
- Keto-enolová tautomérie je zvláštní specifickou vlastností ketonů, která mají bázi beta.
- Reakce aldolové kondenzace s tvorbou beta-ketospirtov.
- Také ketony jsou schopny komunikovat s:
- amoniak;
- kyselina kyanovodíková ;
- hydrosulfit;
- hydrazin;
- orthosilicová kyselina.
Je zřejmé, že reakce těchto interakcí jsou velmi složité, zejména ty, které jsou specifické. To jsou všechny hlavní rysy, které aldehydy a ketony vykazují. Chemické vlastnosti jsou základem mnoha syntéz důležitých sloučenin. Proto je známo povaha molekul a jejich charakter během interakcí je extrémně nutná v průmyslových procesech.
Aldehydové a ketonové adiční reakce
Tyto reakce jsme již přezkoumali, ale nedali jim takové jméno. Všechna interakce mohou být přičítána přidávání, v důsledku čehož karbonylová skupina vykazuje aktivitu. Nebo spíše, mobilní atom vodíku. Proto je v této věci vzhledem k jejich lepší reaktivitě dána přednost aldehydům.
Jaké látky jsou možné reakce aldehydů a ketonů na nukleofilní substituci? Toto je:
- Vzniká kyselina kyanovodíková, kyanhydriny - surovina pro syntézu aminokyselin.
- Amoniak, aminy.
- Alkoholy.
- Voda
- Hydrosulfát sodný.
- Grignardovo činidlo.
- Thiols a další.
Tyto reakce mají velký průmyslový význam, neboť produkty se používají v různých oblastech lidské činnosti.

Způsoby, jak se dostat
Existuje několik základních metod, kterými jsou syntetizovány aldehydy a ketony. Přístup do laboratoře a průmyslu lze vyjádřit následujícími způsoby.
- Nejběžnější metodou, včetně laboratoří, je oxidace odpovídajících alkoholů: primární na aldehydy, sekundární pro zástupce ketonů. Chromáty, ionty mědi, manganistan draselný mohou působit jako oxidační činidla. Obecný pohled na reakci: R-OH + Cu (KMnO4) = R-COH.
- V průmyslu často používáme metodu založenou na oxidaci alkenů - oxosyntézy. Hlavním prostředkem je syntézní plyn, směs CO 2 + H 2 . Výsledkem je aldehyd s velkým počtem atomů na řetězec uhlíku. R = RR + C02 + H2 = RRR-COH.
- Oxidace alkenů ozonem - ozonolýza. Výsledek také naznačuje aldehyd, ale kromě toho je keton také ve směsi. Pokud jsou produkty duševně propojeny a odstraňují kyslík, je zřejmé, jaký byl původní alken.
- Kucherovova reakce - hydratace alkinů. Povinná látka - soli rtuti. Jeden z průmyslových metod syntézy aldehydů a ketonů. R = RR + Hg 2+ + H 2 O = RR-COH.
- Hydrolýza dihalogenových derivátů uhlovodíků.
- Redukce karboxylových kyselin, amidů, nitrilů, chloridů kyselin, esterů. V důsledku toho vzniká jak aldehyd, tak keton.
- Pyrolýza směsí karboxylových kyselin přes katalyzátory na bázi oxidů kovů. Směs by měla být odpařena. Spodní čára je odstranění oxidu uhličitého a vody mezi molekulami. Výsledkem je aldehyd nebo keton.
Aromatické aldehydy a ketony se připravují jinými způsoby, protože tyto sloučeniny mají aromatický zbytek (například fenyl).
- Podle Friedel-Crafts: ve výchozích činidlech je aromatický uhlovodík a dihalogen-substituovaný keton. Katalyzátor - ALCL 3 . Výsledkem je aromatický aldehyd nebo keton. Dalším názvem procesu je acylace.
- Oxidace toluenu různými činidly.
- Rekuperace aromatických karboxylových kyselin.
Průmysl se samozřejmě snaží použít metody, při nichž jsou suroviny co nejlevnější a katalyzátory jsou méně toxické. Pro syntézu aldehydů je oxidace alkenů s kyslíkem.

Průmyslové aplikace a význam
Použití aldehydů a ketonů se provádí v průmyslových odvětvích jako:
- farmaceutické prostředky;
- chemická syntéza;
- lékařství;
- oblast parfumerie;
- potravinářský průmysl;
- výroba barev a laků;
- syntéza plastů, tkanin a další.
Můžete označit více než jednu oblast, protože každoročně se syntetizuje pouze formaldehyd přibližně 6 milionů tun ročně! Jeho 40% roztok se nazývá formalin a slouží k ukládání anatomických objektů. Navštěvuje také výrobu léků, antiseptik a polymerů.
Acetaldehyd, nebo ethanal, také hromadně vyráběný produkt. Množství roční spotřeby na světě činí zhruba 4 miliony tun. Je základem mnoha chemických syntéz, při kterých se tvoří důležité výrobky. Například:
- kyselina octová a její anhydrid;
- acetát celulózy;
- léky;
- butadien - základ gumy;
- ethylalkoholu ;
- acetátové vlákno.
Aromatické aldehydy a ketony jsou nedílnou součástí mnoha příchutí, jak potravin, tak parfémů. Většina z nich má velmi příjemné květinové, citrusové, bylinné aroma. To vám umožní vytvořit na jejich základě:
- Osvěžovače vzduchu různých druhů;
- toaletní a parfémová voda;
- různé čistící prostředky a detergenty.
Některé z nich jsou ochucené potravinářské přídatné látky povolené ke spotřebě. Jejich přírodní obsah v éterických olejích, ovoci a pryskyřicích dokazuje možnost takového použití.
Jednotliví zástupci
Takový aldehyd, jako citrál, je kapalina s vysokou viskozitou a silnou vůní citronu. V přírodě je obsažena ve svých éterických olejích. Také ve složení eukalyptu, čiroku, kebabu.
Známé oblasti použití:
- pediatrie - snížení intrakraniálního tlaku;
- normalizace krevního tlaku u dospělých;
- složka léku pro zrakové orgány;
- část mnoha vonných látek;
- protizánětlivé a antiseptické;
- suroviny pro syntézu retinolu;
- příchuť pro potravinářské účely.