Chemické vlastnosti kovů alkalických zemin. Seznam kovů alkalických zemin
Druhá skupina periodického systému DI Mendeleev obsahuje skupinu prvků, které jsou velmi podobné svým vlastnostem alkalických kovů nicméně mají nižší aktivitu. Obsahuje beryllium a hořčík, stejně jako vápník, stroncium, baryum a rádio. Jsou známé pod obecným názvem - prvky alkalické zeminy. V našem článku se seznámíme s jejich rozložením v povaze a použití v průmyslu a budeme studovat i hlavní chemické vlastnosti kovů alkalických zemin.

Obecné charakteristiky
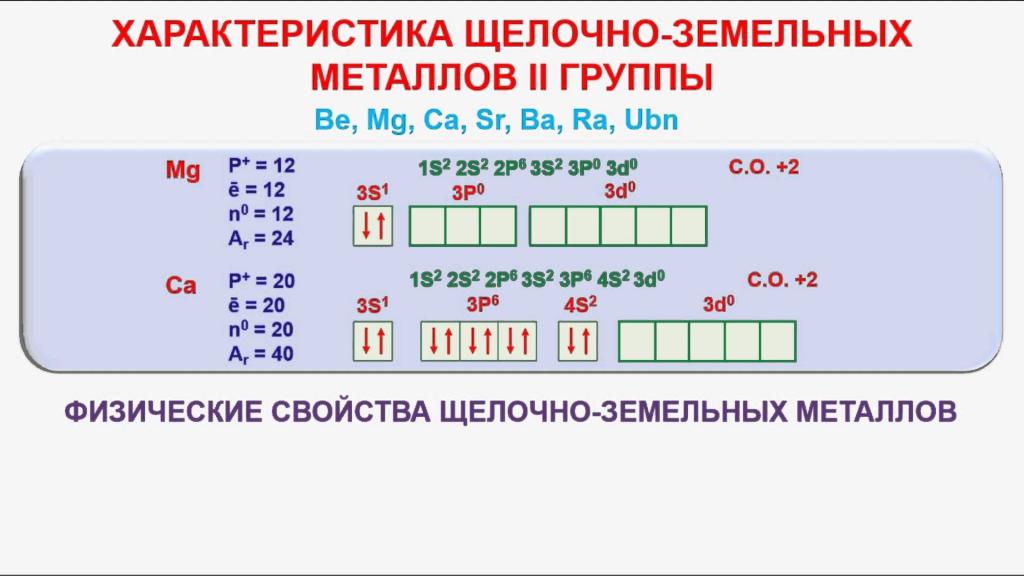
Všechny atomy nad uvedenými prvky obsahují dva elektrony ve vnější vrstvě energie. V interakci s jinými látkami se vždy vzdali svých negativních částic, přecházejí do stavu kationtů s nábojem 2 +. Při redoxních reakcích se prvky chovají jako silné redukční činidla. Jak se zvyšuje jaderný náboj, zvyšují se chemické vlastnosti kovů alkalických zemin a jejich aktivita. Rychle oxidují na vzduchu a vytvářejí oxidový film na jejich povrchu. Obecný vzorec pro všechny oxidy je RO. Odpovídají hydroxidům vzorce R (OH) 2 . Jejich základní vlastnosti a rozpustnost ve vodě se také zvyšují s rostoucím sériovým číslem prvku.
Zvláštní vlastnosti berylia a hořčíku
V některých svých vlastnostech se první dva zástupci hlavní podskupiny druhé skupiny poněkud liší od jiných prvků alkalických zemin. To se projevuje zejména při jejich interakci s vodou. Například chemické vlastnosti berylia jsou takové, že vůbec nereagují s H 2 O. Hořčík interaguje s vodou pouze při zahřátí. Ale všechny prvky alkalické zeminy snadno reagují s ním při běžné teplotě. Jaké látky se tvoří současně?

Podklady alkalických zemin
Vápenec, bárium a další členové skupiny rychle nahrazují vodík z vody, což vede k jejich hydroxidům. Interakce kovů alkalických zemin s vodou teče rychle a uvolňuje teplo. Roztoky základů vápníku, bária, stroncia, uklidňující na dotek, při styku s kůží a sliznicí očí, způsobují těžké popáleniny. První pomoc v takových případech bude ošetření povrchu rány slabým roztokem kyseliny octové. Neutralizuje alkálie a snižuje riziko nekrózy poškozených tkání.
Chemické vlastnosti kovů alkalických zemin
Interakce s kyslíkem, vodou a nekovy je hlavní seznam vlastností kovů zařazených do druhé skupiny periodického systému chemických prvků. Například vápník reaguje i za normálních podmínek s halogeny: fluorem, chlorem, bromem a jodem. Při zahřátí se kombinuje se sírou, uhlíkem a dusíkem. Tvrdá oxidace - hoření, končí formací oxid vápenatý: 2Ca + 02 = 2 CaO. Interakce kovů s vodíkem vede k vzhledu hydridů. Jsou to bílé žáruvzdorné látky s iontovými krystalovými mřížkami. Mezi důležité chemické vlastnosti kovů alkalických zemin patří jejich interakce s vodou. Jak již bylo uvedeno výše, produktem této substituční reakce je hydroxid kovu. Všimněte si také, že v hlavní podskupině druhé skupiny vápník zaujímá nejvýznamnější místo. Proto se zabýváme jejími vlastnostmi podrobněji.
Vápník a jeho sloučeniny
Obsah prvku v kůře je až 3,5%, což naznačuje jeho široké rozložení v složení takových minerálů, jako je vápenec, křída, mramor a kalcit. Složení přírodního vápníku zahrnuje šest typů izotopů. To je také nalezeno v přírodních vodních zdrojích. Sloučeniny alkalických kovů jsou podrobně studovány v průběhu anorganické chemie. Například ve třídě 9 se studenti dozví, že vápník je lehký, ale silný stříbrně bílý kov. Jeho teploty tání a varu jsou vyšší než teploty alkalických prvků. Hlavní metodou získání - elektrolýzy směsi roztavených solí chloridu a fluoridu vápenatého. Hlavními chemickými vlastnostmi jsou jeho reakce s kyslíkem, vodou a nekovy. Ze sloučenin alkalických kovů jsou oxidy a vápník nejdůležitější pro průmysl. První sloučenina se získává z křídy nebo vápence spálením.

Dále se hydroxid vápenatý tvoří z oxidu vápenatého a vody. Jeho směs s pískem a vodou se nazývá stavební malta. Používá se jako omítka a pro spojování cihel při pokládce stěn. Roztok hydroxidu vápenatého, nazývaný vápenná voda, se používá jako činidlo pro detekci oxidu uhličitého. Při průchodu oxidu uhličitého čirým vodným roztokem Ca (OH) 2 se pozoruje jeho zákal kvůli tvorbě nerozpustné sraženiny. uhličitan vápenatý.
Hořčík a jeho charakteristika
Chemie kovů alkalických zemin zkoumá vlastnosti hořčíku se zaměřením na některé jeho vlastnosti. Je to velmi lehký, stříbřitě bílý kov. Hořčík roztavený v atmosféře s vysokou vlhkostí aktivně absorbuje molekuly vodíku z vodní páry. Při ochlazení se kov téměř úplně uvolní zpět do vzduchu. Reaguje velmi pomalu s vodou kvůli tvorbě špatně rozpustné sloučeniny, hydroxidu hořečnatého. Alkálie neúčinkují na hořčíku vůbec. Kov nereaguje s některými kyselinami: koncentrovaným sulfátem a fluorovodíkem, díky pasivaci a tvorbě ochranného filmu na povrchu. Většina minerálních kyselin rozpouští kov, který je doprovázen rychlým uvolňováním vodíku. Hořčík je silné redukční činidlo, nahrazuje mnoho kovů ze svých oxidů nebo solí:
BeO + Mg = MgO + Be.
Kov společně s berylliem, manganem a hliníkem se používá jako legovací prostředek pro ocel. Zvláště cennými vlastnostmi jsou slitiny obsahující hořčík - elektrony. Používají se v letecké a automobilové výrobě, stejně jako v detailech optické techniky.
Úloha prvků v životně důležité činnosti organismů
Uveďte příklady kovů alkalických zemin, jejichž sloučeniny jsou běžné u volně žijících živočichů. Hořčík je centrálním atomem molekul chlorofylu v rostlinách. Podílí se na procesu fotosyntézy a je součástí aktivních center zeleného pigmentu. Atomy hořčíku fixují světelnou energii a přeměňují ji na energii chemických vazeb organických sloučenin: glukózu, aminokyseliny, glycerin a mastné kyseliny. Důležitou roli hraje prvek jako nezbytná složka enzymů, které regulují metabolismus v lidském těle. Vápník je makronutrient, který zajišťuje efektivní průchod elektrických impulzů nervovou tkání. Přítomnost fosfátových solí ve složení kostí a zubní skloviny jim dává tvrdost a pevnost.
Beryllium a jeho vlastnosti
Mezi kovy alkalických zemin patří také berýlium, baryum a stroncium. Zvažte berýlium. Prvek není v přírodě široce rozšířen a nachází se hlavně ve složení minerálů, například beryl. Jeho odrůdy obsahující vícebarevné nečistoty tvoří drahokamy: smaragdy a akvamaríny. Vlastností fyzikálních vlastností je křehkost a vysoká tvrdost. Charakteristickým znakem atomu prvku je přítomnost na druhé úrovni vnější energie, nikoliv osm, stejně jako u všech ostatních kovů alkalických zemin, ale pouze dva elektrony.

Proto je poloměr atomu a iontu nepřiměřeně malý, ionizační energie je velká. To způsobuje vysokou pevnost. krystalová mřížka kovu. Chemické vlastnosti berýlií se odlišují od ostatních prvků druhé skupiny. Reaguje nejen s kyselinami, ale také s alkalickými roztoky, které nahrazují vodík a vytvářejí hydroxoberyláty:
Be + 2NaOH + 2H20 = Na2 [Be (OH) 4 ] + H2.
Kov má řadu jedinečných vlastností. Vzhledem k možnosti přeskakování rentgenových paprsků se používá při výrobě okenních rentgenových trubek. V jaderném průmyslu je tento prvek považován za nejlepší moderátor a reflektor neutronů. V metalurgii se používá jako cenná legovací přísada, která zvyšuje antikorozní vlastnosti slitin.
Stroncium a baryum
Prvky jsou docela obyčejné v přírodě a stejně jako hořčík kovů alkalických zemin jsou součástí minerálů. Říkáme jim: je barit, celestina, stroncium. Barium má vzhled plastového kovu stříbrně bílé barvy. Stejně jako vápník je reprezentován několika izotopy. Ve vzduchu působí aktivně se svými složkami - kyslíkem a dusíkem - za vzniku oxidu barnatého a nitridu. Z tohoto důvodu je kov uložen pod vrstvou parafínu nebo minerálního oleje, čímž se zabrání jeho kontaktu se vzduchem. Oba kovy vytvářejí peroxidy při zahřívání na 500 ° C.

Z těchto, peroxid barya, používaný jako bělící tkáň, má praktickou aplikaci. Chemické vlastnosti kovů alkalických zemin, bária a stroncia jsou podobné vlastnostem vápníku. Nicméně jejich interakce s vodou je mnohem aktivnější a výsledné báze jsou silnější než hydroxid vápenatý. Baryum se používá jako přísada do tekutých kovových chladicích plynů, snižuje koroze, v optice, při výrobě vakuových elektronických zařízení. Stroncium je požadováno při výrobě fotovoltaických článků a fosforů.
Kvalitativní reakce za použití iontů kovů alkalických zemin
Sloučeniny barya a stroncia jsou příklady kovů alkalických zemin, které se v pyrotechnice široce používají kvůli jasnému zbarvení plamene ionty. Tudíž síran nebo uhličitan strontnatý vytváří karmínově červenou záři plamene a odpovídající sloučeniny barya poskytují žlutozelenou barvu. Pro detekci vápenatých iontů v laboratoři se na plamen hořáku nalije několik pelet chloridu vápenatého, plamen je namalován v cihlově červené barvě.

Roztok chloridu barnatého se používá v analytické chemii ke zjištění kyselého zbytku kyseliny sírové v roztoku. Pokud vznikne bílá sraženina síranu barnatého při vyčerpání roztoků, znamená to, že v něm jsou částice SO 4 2- .
V našem článku jsme studovali vlastnosti kovů alkalických zemin a ukázali jejich použití v různých průmyslových odvětvích.