Uhlovodíky jsou sloučeniny uhlíku s vodíkem, které neobsahují jiné prvky. Klasifikace uhlovodíků
Co jsou uhlovodíky? Jak jsou klasifikovány? Jaké funkce mají? Pokusíme se společně najít odpovědi na otázky.
Uhlovodíky jsou organických sloučenin které obsahují vodík a uhlík. Jsou považovány za organické sloučeniny v základní chemii.
Klasifikace
V závislosti na stavu vazby mezi uhlíkem hlavního řetězce je běžné rozdělit všechny C x H y na několik typů. Jednotlivé sloučeniny uhlíku s vodíkem jsou charakteristické pro nasycené uhlovodíky.
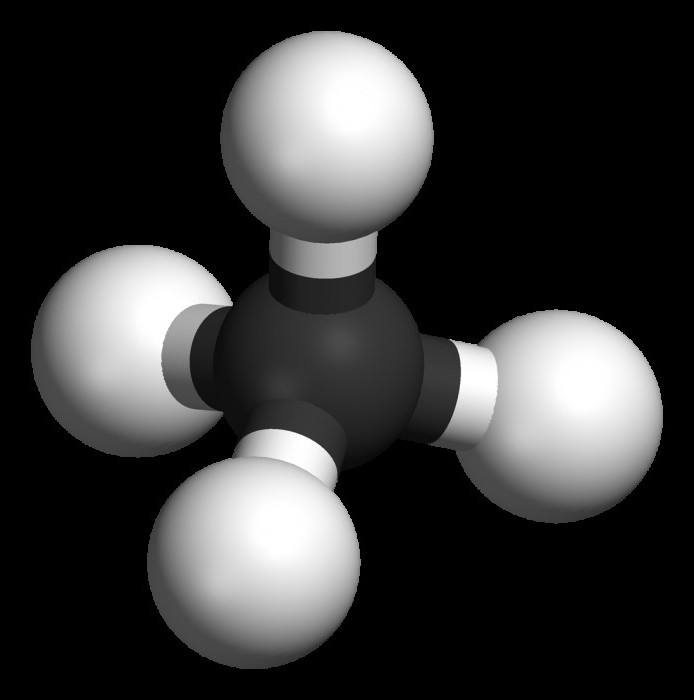
Alkanes
Limitní uhlovodíky jsou sloučeniny obecného vzorce CnH2n + 2 . Mezi jejich rysy můžeme zmínit nepřítomnost uzavřené struktury a jednoduché vazby. Jsou nazývány acyklickými sloučeninami v organické chemii.
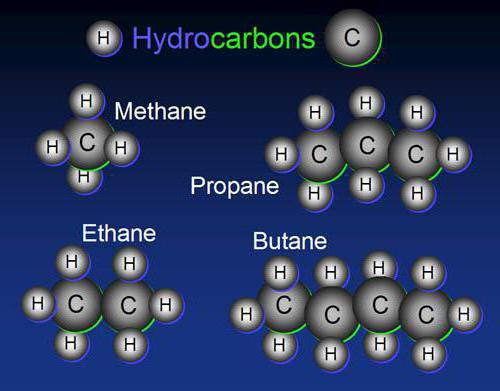
Typickým představitelem této třídy je metan - CH 4 . Je to ten, kdo zahajuje homologní řadu alkánů, má všechny vlastnosti, které jsou vlastní ostatním zástupcům parafinů.
Prvním představitelem této skupiny uhlovodíků jsou plynné látky s nízkou rozpustností ve vodě, specifický zápach.
Mezi základní chemické vlastnosti, které mají zástupci homologní řady alkanů, vymezujeme radikální substituci.
Halogenace nastává při zvýšených teplotách nebo za přítomnosti ultrafialového záření. Reakce probíhá v několika stupních, charakterizovaných postupnou výměnou atomů vodíku za halogen. Vlastnosti uhlovodíků řady metanu jsou vysvětleny saturací vazby mezi atomy uhlíku. Nejsou schopné vstoupit do reakcí navíc, zatímco dobře vypalují v kyslíku ze vzduchu, čímž vytvářejí oxid uhličitý, vodní páru a uvolňují dostatečnou tepelnou energii.
Mezi hlavní oblasti působnosti zástupců této skupiny uhlovodíků je vymezeno použití jako palivo, jakož i možnost surovin pro výrobu mnoha dalších organických sloučenin.
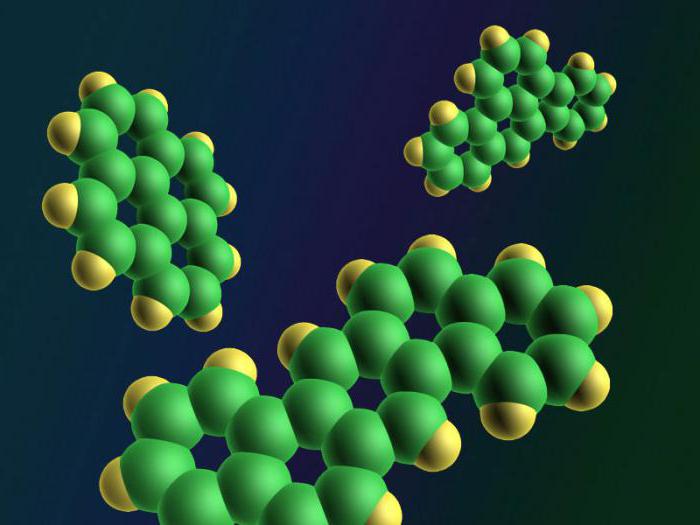
Alkenes
Nenasycené uhlovodíky jsou sloučeniny, které mají jednu nebo více nenasycených vazeb mezi atomy uhlíku. Alkeny mají obecný vzorec CnH2n . Typickým představitelem této třídy je ethylen.
Tyto přírodní uhlovodíky jsou součástí oleje. Vzhledem k tomu, že molekula obsahuje dvojnou vazbu, adiční reakce jsou charakteristické pro alkény. Mohou například vstoupit do halogenace, hydratace.
Pokud je dvojná vazba umístěna v první poloze, například v butenu-1, postupuje přídavek halogenovodíku a hydratace (reakce s vodou) podle Markovnikova pravidla. Jeho podstatou je skutečnost, že během hydrohalogenace a hydratace je vodík připojen k atomu uhlíku, který je maximálně nasycen.
Hydroxyskupina nebo atom halogenu jsou připojeny k atomu C, který není nasycen vodíkem. Kvalitativní reakce na nenasycené (dvojité) vazbě je bělení bromové vody nebo manganistan draselný.

Cykloalkany
Takové uhlovodíky jsou cyklické sloučeniny, které jsou meziplastické izomery pro alkény. Mají obecný vzorec CnH2n , jednoduché vazby. Vzhledem k tomu, že tato třída je charakterizována uzavřenou strukturou, vstupují do dalších reakcí, které jsou doprovázeny ničením uzavřeného cyklu a přeměnou na nasycené alkány. Hlavními zdroji těchto sloučenin jsou přírodní a související plyny a oleje. Navzdory cyklické struktuře v hybridizačních molekulách sp3 je úhel valence 109 ° 28 '.
Alkadiens
Co ještě charakterizuje organická chemie? Uhlovodíky této třídy mají obecný vzorec CpH2n-2 . Všichni zástupci dienových uhlovodíků mají dvě dvojné vazby. Nenasycení dienů určuje jejich základní chemické vlastnosti. Analogicky s alkeny vstupují dienové sloučeniny do adiční reakce.
Jako ty chemické reakce které jsou charakteristické pro tyto sloučeniny, zaznamenáváme polymerizaci. Počátečním monomerem v procesu je reprezentant dienů a interakčním produktem je syntetický kaučuk. Když se k výslednému polymeru přidá síra, dochází k vulkanizaci spolu s tvorbou kaučuku.
Alkyny
U těchto nenasycených organických sloučenin charakterizovaných obecným vzorcem CnH2n-2 můžeme pozorovat přítomnost trojné vazby mezi atomy uhlíku. Pokud je umístěn po prvním atomu uhlíku, kvalitativní reakce na jeho přítomnost je nahrazení komplexní sloučeninou stříbra.
Stejně jako pro alkény, dieny, alkiny snadno spojují trojnou vazbu. Jsou charakterizovány hydrogenací, hydrohalogenací, halogenací, hydratačními reakcemi.

Aromatické sloučeniny
Benzen je prvním zástupcem této třídy. Má obecný vzorec CnH2n-6 . Na rozdíl od všech ostatních uhlovodíků má tato sloučenina aromatický kruh. V jeho tvorbě se podílejí volné elektrony z každého atomu uhlíku. Tři elektrony C tvoří hybridní mraky a čtvrtý elektron neprojeví hybridizaci. Vytváří aromatický kruh, který je rovnoměrně rozložen po molekule. Rovnoměrné rozložení kruhu strukturou vysvětluje jeho chemickou stabilitu. Benzen samotný vstupuje do nahrazení a přidávání pouze v drsných podmínkách.
Toluen, který je jeho homolog, je charakterizován určitým posunem v elektronové hustotě, a proto má vyšší substituční kapacitu. Uhlovodíkový radikál je orientován na typ 1, vstupující substituenty (halogen, nitroskupina) zaujímají orto, para pozice.
Závěr
Bez ohledu na to, které vlastnosti struktury jsou různými zástupci uhlovodíků, mají v jejich složení určitý počet atomů uhlíku a vodíků. Existuje určitá tendence změnit fyzikální vlastnosti zástupců C x H y . První zástupci každé třídy mají plynný stav, jelikož vzrůstá relativní molekulová hmotnost, je pozorován systematický přechod v kapalině, pak v pevné formě.