Teorie elektrolytické disociace - jedna z hlavních v chemii
Při rozpuštění ve vodě se elektrolytické látky rozkládají na nabité částice - ionty. Opačný je molarizace nebo asociace. Tvorba iontů vysvětluje teorii elektrolytické disociace (Arrhenius, 1887). Mechanismus rozkladu chemických sloučenin během tavení a rozpouštění je ovlivněn charakteristikami typů chemických vazeb, strukturou a povahou rozpouštědla.
Elektrolyty a nevodiče
Zničení se vyskytuje v roztocích a roztavuje se krystalové mřížky a molekuly - elektrolytická disociace (ED). Rozklad látek je doprovázen tvorbou iontů, vzhledu vlastností jako elektrická vodivost. Ne každá sloučenina je schopna disociovat, ale pouze látky, které se zpočátku skládají z iontů nebo vysoce polárních částic. Přítomnost volných iontů vysvětluje vlastnost elektrolytů pro vedení proudu. Základ, sůl, mnoho anorganických a některé organické kyseliny mají tuto schopnost. Nevodiče sestávají z molekul nízké polarity nebo nepolarizovaných molekul. Nevšimují se na ionty, jsou neelektrolyty (mnoho organických sloučenin). Nosníky náboje jsou pozitivní a negativní ionty (kationty a anionty).
Ad
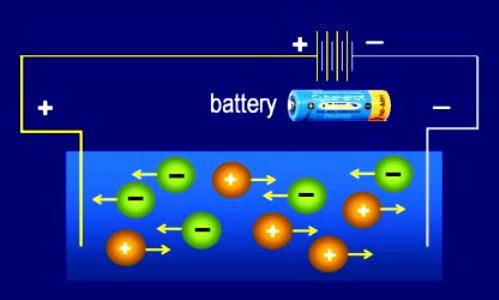
Úloha S. Arrheniova a dalších chemiků ve studiu disociace
Teorie elektrolytické disociace dokázala v roce 1887 vědec ze Švédska S. Arrhenius. První rozsáhlé studie vlastností řešení však provedl ruský vědec M. Lomonosov. Přispěl ke studiu nabitých částic vznikajících při rozpouštění látek, T. Grotgus a M. Faraday, R. Lenz. Arrhenius prokázal, že mnoho anorganických elektrolytů a některé organických sloučenin. Švédský vědec vysvětlil elektrickou vodivost roztoků rozkladem látky do iontů. Teorie elektrolytické disociace Arrhenius nepřipojovala k přímé účasti molekul vody v tomto procesu význam. Rusové vědci Mendelejev, Kablukov, Konovalov a další věřili, že dochází k rozpuštění - vzájemné působení rozpouštědla a rozpuštěné látky. Pokud jde o vodní systémy, používá se název "hydratace". Jedná se o komplexní fyzikálně-chemický proces, o čemž svědčí formace hydrátů, tepelných jevů, zbarvení hmoty a vzhled sedimentu.
Ad

Hlavní ustanovení teorie elektrolytické disociace (TED)
Mnoho vědců pracovalo na objasnění teorie S. Arrheniova. Bylo nutné ho zlepšit s přihlédnutím k moderním datům o struktuře atomu, chemické vazbě. Jsou formulována hlavní ustanovení TED, která se liší od klasických tezí konce XIX století:
- Proces tavení nebo rozpouštění je doprovázen disociací elektrolytu na ionty. Takže (na návrh Faradaye) nazývali částice s nábojem ("+" nebo "-"), které se liší od neutrálních atomů ve struktuře valenčních skořepin a stability, jsou barvené a bezbarvé. Iony mohou být jednoduché: Na + , Cl - , S 2- , Al 3+ . Nabité částice se skládají ze skupin atomů: CO 2 , NH 4+ . Z řeckého jazyka je název "ion" překládán jako "putování", což naznačuje náhodnost šíření těchto částic.
- Vliv vnějšího elektrického pole způsobuje, že se ionty pohybují uspořádaným způsobem uvnitř prostoru elektrolytu. Každá negativní částice je směrována na anodu (kladná elektroda). Iony se znaménkem "+" začínají pohybovat směrem k katodě (záporná elektroda).
- Zároveň dochází k rozkladu na ionty a kombinaci těchto částic v roztoku, proto se disociace týká reverzibilních fyzikálně chemických procesů.
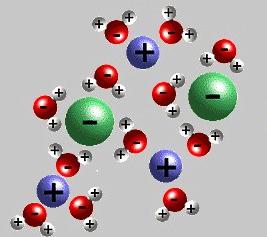
Při sestavování rovnic je třeba vzít v úvahu vzniklé jevy: aplikovat speciální znak reverzibilního procesu, vypočítat negativní a kladné náboje: musí se shodovat shodně.
Mechanismus ED iontových látek
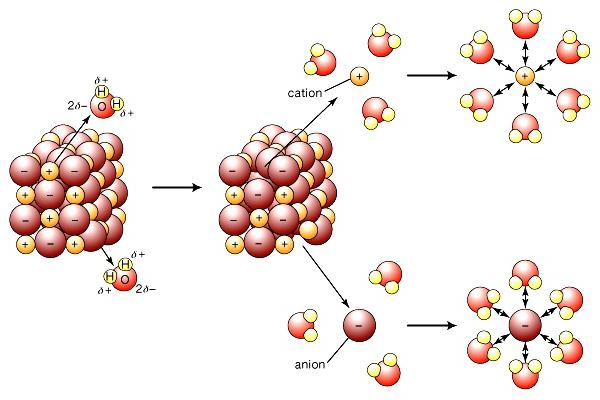
Moderní teorie elektrolytické disociace zohledňuje strukturu elektrolytických látek a rozpouštědel. Když se rozpustí, vazby mezi protilehle nabitými částicemi v iontových krystalech jsou zničeny působením polárních molekul vody. Doslova "vytáhnou" ionty z hmoty do roztoku. Rozpad je doprovázen tvorbou solvátu (ve vodě - hydratace) kolem iontů. Kromě vody mají ketony, nižší alkoholy vyšší dielektrickou konstantu. Během disociace chlorid sodný Na + a Cl - iony registrují počáteční stupeň, který je doprovázen orientací vodních dipolů vzhledem k povrchovým iontům v krystalu. V konečné fázi se uvolňují hydratované ionty a difundují do kapaliny.
Ad
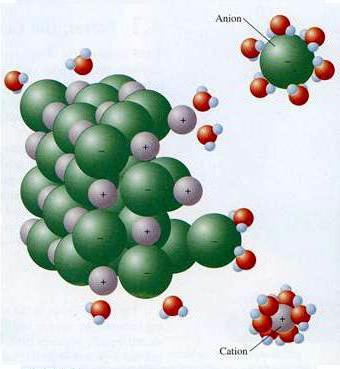
Mechanismus ED sloučenin s kovalentní silnou polární vazbou
Molekuly rozpouštědla ovlivňují krystalickou strukturu neiontových látek. Například účinek vodních dipolů na kyselinu chlorovodíkovou vede ke změně typu vazby v kovalentní polární molekule na iontovou. Substance disociuje, hydratovaný vodík a chlorové ionty vstupují do roztoku. Tento příklad dokládá důležitost procesů, které se vyskytují mezi částicemi rozpouštědla a rozpuštěnou sloučeninou. To je tato interakce, která vede k tvorbě iontů elektrolytů.
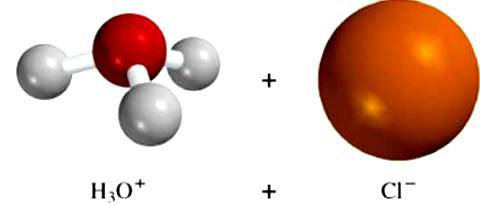
Teorie elektrolytické disociace a hlavní třídy anorganických sloučenin
Ve světle hlavních ustanovení TED, kyselina může být nazývána elektrolytem, během rozpadu kterého z pozitivních iontů může být detekován pouze proton H + . Disociace báze je doprovázena tvorbou nebo uvolněním pouze krystalické mřížky OH anionu a kovového kationtu. Normální sůl při rozpuštění poskytuje kladný kovový iont a negativní - zbytek kyseliny. Hlavní sůl se vyznačuje přítomností dvou typů aniontů: skupina OH a zbytky kyseliny. V kyselé soli kationtů je přítomen pouze vodík a kov.
Ad
Síla elektrolytu
Pro charakterizaci stavu látky v roztoku se používá fyzikální množství - stupeň disociace (α). Najděte jeho hodnotu z poměru počtu zlomených molekul k jejich celkovému počtu v roztoku. Hloubka disociace je určena různými podmínkami. Významné dielektrické ukazatele rozpouštědla, struktura rozpuštěných sloučenin. Typicky se stupeň disociace s rostoucí koncentrací snižuje a zvyšuje se zvyšující se teplotou. Často je stupeň disociace určité látky vyjádřen ve zlomcích jednotky.
Klasifikace elektrolytů
Teorie elektrolytické disociace na konci 19. století neobsahovala ustanovení o interakci iontů v roztoku. Účinky molekul vody na distribuci kationtů a aniontů se zdály být pro Arrhenius nevýznamné. Arrheniovy představy o silných a slabých elektrolytech byly formální. Na základě klasických pozic lze získat silné elektrolyty α = 0,75-0,95. Pokusy prokázaly nezvratnost jejich disociace (α → 1). Rozpustné soli, sírové a kyselina chlorovodíková alkálie. Částečně disociují síru, dusík, fluorovodík, kyselina fosforečná. Slabými elektrolyty jsou kyselina křemičitá, kyselina octová, hydrogensíranová a uhličitá, hydroxid amonný, nerozpustné báze. Voda je také označována jako slabý elektrolyt. Malá část molekuly H2O se oddělí a ionty se současně molarizují.