Vanadium: vlastnosti, atomová hmotnost, vzorec, aplikace
Vanad je chemický prvek označený symbolem "V". Atomová hmotnost vanadu je 50,9415 a. m., atomové číslo - 23. Je to masivní stříbrošedý, tvárný a tavitelný kov, zřídka se vyskytující v přírodě. Je součástí více než 60 minerálů a může být dokonce obsaženo v fosilních palivech.

Nerozpoznaný objev
Vanadium metal byl poprvé objeven mexickým mineralogistou španělského původu, Andresem Manuel Del Rio, v roce 1801. Vědec odstranil nový prvek ze vzorku hnědé olověné rudy těžené v Mexiku. Jak se ukázalo, kovové soli mají širokou paletu barev, a proto se Del Rio původně nazývalo "panchromium" (z řečtiny "παγχρώμιο" - "vícebarevné").
Ad
Později mineralogička přejmenovala na element erythronium (z řečtiny "erythron" - "červená"), protože většina solí získala při zahřátí červený odstín. Zdálo se, že neuvěřitelné štěstí se usmívalo na málo známého vědce v Evropě. Objev nového chemického prvku vanadu slíbil, ne-li slávu, a přinejmenším uznání kolegy. Nicméně kvůli nedostatku přísné autority ve vědeckém světě nebylo dosaženo mexického úspěchu.
V roce 1805 navrhl francouzský chemik Hippolytus Victor Colle-Decotils, že nový prvek zkoumaný společností Del Rio byl jen vzorkem olovnatého chromátu s nečistotami. Nakonec mexický badatel, aby nedošlo k úplnému ztrátě tváře před vědeckým bratrstvím, přijal souhlas Colle-Decotyle a odmítl ji otevřít. Jeho úspěch však nezapadl do zapomnění. Dnes je Andrés Manuel Del Río uznáván jako objevitel vzácného kovu.
Ad
Znovu otevřete
V roce 1831 znovu objevil švédský Nils Gabriel Sefström chemický prvek vanad v oxidu, který získal při práci s železnou rudou. Jako jeho označení vědec vybral písmeno "V", které ještě nebylo přiděleno žádnému prvku. Sefström volal nový kov kvůli své krásné a bohaté barvě na počest norské bohyně krásy Vanadis.
Zprávy způsobily zvýšený zájem o vědeckou komunitu. Okamžitě si vzpomněl na práci mexického mineraloga. Ve stejném roce 1831 Friedrich Wöhler znovu zkontroloval a potvrdil předchozí objev Del Rio. A geolog George William Featherstonhup dokonce navrhl zavolat kovu "Rionium" na počest objevitele, ale iniciativa nebyla podporována.

Nerozumné
Izolace kovu vanadu v jeho čisté formě se ukázala jako obtížná. Před tím vědci pracovali pouze se svými solemi. To je důvod, proč jsou skutečné vlastnosti vanadu neznámé. V roce 1831 Berzelius oznámil, že dostal metalizovanou látku, ale Henry Enfield Roscoe dokázal, že Berzelius vlastně produkoval nitrid vanadu (VN). Nakonec Roscoe vyrobil kov v roce 1867 tím, že snížil chlorid vanadu (VCl 2 ) pod účinkem vodíku. Od roku 1927 se čistý vanád získává redukcí oxidu vanadičného za účasti vápníku.
Ad
První sériové průmyslové využití prvku pochází z roku 1905. Do ocelových slitin byl přidán kov pro výrobu podvozek závodních automobilů a později - v modelu Ford Model T. Vanadium může snížit hmotnost konstrukce a zároveň zvýšit pevnost v tahu. Mimochodem, německý chemik Martin Khenze objevil v roce 1911 vanadium v krvinkách (nebo coelomických buňkách) mořských obyvatel - excizie.

Fyzikální vlastnosti
Vanadium je tvárný šedo-modrý kov střední tvrdosti s ocelovým leskem a hustotou 6,11 g / cm ³. Některé zdroje popisují materiál jako měkký, s ohledem na jeho vysokou plasticitu. Krystalová struktura prvku je složitější než většina kovů a ocelí.
Vanadium má dobrou odolnost proti korozi, zásadám, síře a kyselina chlorovodíková. Oxiduje na vzduchu při teplotě asi 660 ° C (933K, 1220 ° F), i když pasivace oxidu nastává dokonce i při pokojové teplotě. Tento materiál se roztaví, když teplota dosáhne 1920 ° C a teplota varu je 3400 ° C.
Chemické vlastnosti
Vanada pod vlivem kyslíku tvoří čtyři typy oxidů:
Barva | Hustota | Vařte | Tavení | |
VO (II) | Černá | 5,76 g / cm3 | 3100 ° C | 1830 ° C |
V2O3 (III) | Černá | 4,87 g / cm3 | 3000 ° C | 1967 ° C |
VO 2 (IV) | Navy blue | 4,65 g / cm3 | 2700 ° C | 1542 ° C |
V 2 O 5 (V) | Orange | 3,357 g / cm3 | 2030 ° C | 670 ° C |
Sloučeniny typu (II) vanadu jsou redukční činidla a sloučeniny typu (V) jsou oxidační činidla. Sloučeniny (IV) často existují jako deriváty vanadylového kationtu.
Oxid
Nejvíce komerčně důležitou sloučeninou je oxid vanadičný. Je to hnědo-žlutá pevná látka, i když je čerstvě zabalena z vodného roztoku, její barva je tmavě oranžová.
Ad

Oxid se používá jako katalyzátor k výrobě kyseliny sírové. Tato sloučenina oxiduje oxid siřičitý (SO 2 ) na oxid křemičitý (SO 3 ). Při této redoxní reakci se síra oxiduje z +4 na +6 a vanad se snižuje z +5 na +4. Vzorec pro vanadu je následující:
V 2 O 5 + SO 2 → 2VO 2 + SO 3
Katalyzátor se regeneruje oxidací kyslíku:
2VO 2 + O 2 → V 2 O 5
Podobné oxidační procesy se používají při výrobě anhydridu kyseliny maleinové, anhydridu kyseliny ftalové a několika dalších organických sloučenin.
Tento oxid se také používá při přípravě ferkonadia. Zahřívá se železem a ferosilikonem s přídavkem vápna. Při použití hliníku se vyrábí slitina železa a vanadu společně s oxidem hlinitým jako vedlejším produktem. Kvůli vysokému koeficientu tepelné odolnosti se jako detekční materiál v bolometrech a mikrobolometrických polích v zařízeních pro tepelné zobrazování používá oxidu vanadičitého (V).
Charakteristiky
Vzácný kov má tyto vlastnosti:
- Křišťálová struktura: kubické tělo na střed.
- Zvuková vodivost: 4560 m / s (při 20 ° C).
- Vanadová valencie: V (zřídka IV, III, II).
- Teplotní roztažnost: 8,4 μm / (m · K) (při 25 ° C).
- Tepelná vodivost: 30,7 W / (m · K).
- Elektrický odpor: 197 nΩ · m (při 20 ° C).
- Magnetismus: paramagnetický.
- Magnetickou citlivost: + 255 · 10 -6 cm3 / mol (298K).
- Modul pružnosti: 128 GPa.
- Modul smyku: 47 GPa.
- Hromadný modul pružnosti: 160 GPa.
- Poissonův poměr: 0,37.
- Mohsova tvrdost: 6.7.
- Tvrdost Vickers: 628-640 MPa.
- Tvrdost podle Brinella: 600-742 MPa.
- Kategorie zboží: přechodový kov.
- Elektronická konfigurace: 3d 3 4s 2 .
- Teplota tání: 21,5 kJ / mol.
- Teplo odpařování: 444 kJ / mol.
- Molární tepelná kapacita: 24,89 J / (mol · K).
Vanadium v periodické tabulce je v 5. skupině (podskupina vanadu), 4. perioda, d-blok.
Spread
Vanadium v měřítku vesmíru je přibližně 0,0001% celkového objemu hmoty. To se šíří tak často jako měď a zinek. Kov se nalézá ve spektrální záři Slunce a dalších hvězd.
Ad
Prvek je 20. nejvíce obyčejný v kůře. Krystalický vanad v krystalické formě je poměrně vzácný, ale sloučeniny tohoto materiálu se nacházejí v 65 různých minerálech. Ekonomicky významný z nich je patronit (VS 4 ), vanadinit (Pb 5 (VO 4 ) 3 Cl) a karnotit (K 2 (UO 2 ) 2 (VO 4 ) 2 · 3 H 2 O).
Vanadylové ionty jsou hojně distribuovány v mořské vodě a mají průměrnou koncentraci 30 nMa. Některé zdroje minerální vody také obsahují tyto ionty ve vysokých koncentracích. Například zdroje v blízkosti Mount Fuji obsahují až 54 μg / l.
Těžba
Většina tohoto vzácného kovu se získává z vanadia magnetitu, který se nachází v ultrabazických magmatických horninách gabbro. Suroviny se těží hlavně v Jižní Africe, severozápadní Číně a ve východním Rusku. V roce 2013 vyrobily tyto země více než 97% veškerého vanadu (79 000 tun váhových).
Kov je také přítomen v bauxitu a ložiskách ropy, uhlí, ropných břidlic a dehtových písků. V ropě byly zaznamenány koncentrace až do 1200 ppm. Vzhledem k oxidačním vlastnostem vanadu (některých jeho oxidů) po spálení těchto ropných produktů mohou zbytky prvku způsobit korozi v motorech a kotlích.
Odhaduje se, že 110 000 tun látky se každoročně vypouští do atmosféry spalováním fosilních paliv. Dnes se vyvíjejí technologie na získávání cenných látek z uhlovodíků.
Výroba
Vanad se používá hlavně jako přísada do slitin z oceli nazývaných feroslitiny. Ferrovanadium se získá přímo redukcí směsi oxidu vanadia s valencí (V), oxidy železa a čistého železa v elektrické peci.
Kov je vyráběn s použitím vícestupňového procesu, který začíná spálením drcené vanadové magnetitové rudy přidáním chloridu sodného (NaCl) nebo uhličitanu sodného (Na2CO3) při teplotě asi 850 ° C za vzniku sodného metavanadátu (NaVO 3 ). Vodný extrakt této látky se okyselí za vzniku polyvanadátové soli, která se redukuje vápníkem. Jako alternativa k malosériové výrobě je oxid vanadičný redukován vodíkem nebo hořčíkem.
Používá se také mnoho dalších metod, u nichž se vana vyrábí jako vedlejší produkt jiných procesů. Jeho čištění je možné pomocí jodidové metody, kterou vyvinul Anton Edouard van Arkel a Jan Hendrik de Bohr v roce 1925. Zahrnuje tvorbu jodidu vanadičného a jeho následný rozklad na čistý kov:
2 V + 3I 2 ⇌ 2 VI 3
Poměrně exotický způsob získání tohoto prvku byl vynalezen Japoncem. Chovají se na ascidských podvodních plantážích (typu akordů), které absorbují vanadium z mořské vody. Pak se shromažďují a spálí. Cenný kov se extrahuje z vytvořeného popela. Mimochodem, jeho koncentrace v tomto případě je mnohem vyšší než u nejbohatších ložisek.

Slitiny
Co jsou slitiny vanadu? Přibližně 85% vyráběných vzácných kovů se používá k výrobě ferovanadia nebo jako přísady do oceli. Na počátku 20. století bylo zjištěno, že i malé množství vanadu výrazně zvyšuje pevnost oceli. Tento prvek tvoří stabilní nitridy a karbidy, což vede ke zlepšení výkonu ocelí a slitin.
Od té doby se vanád používal v nápravách, rámech, klikových hřídelích, ozubených převodech a dalších důležitých součástech kolových vozidel. Existují dvě skupiny slitin:
- Vysoký obsah uhlíku je od 0,15% do 0,25% vanadu.
- Rychlé řezání nástrojové oceli (HSS) od 1% do 5% tohoto prvku.
U ocelí HSS může být dosažena tvrdost vyšší než HRC 60. Používají se chirurgické nástroje. V práškové metalurgii mohou slitiny obsahovat až 18% vanadu. Vysoký obsah karbidů těchto slitin výrazně zvyšuje odolnost proti opotřebení. Dělají nástroje a nože.
Díky svým vlastnostem vanad stabilizuje beta formu titanu, zvyšuje jeho pevnost a teplotní stabilitu. Směs s hliníkem v slitinách titanu se používá v proudových motorech, vysokorychlostních letadlech a zubních implantátech. Nejběžnější slitina pro bezešvé trubky je titan 3 / 2,5, obsahující 2,5% vanadu. Tyto materiály jsou široce distribuovány v leteckém, obranném a cyklistickém průmyslu. Další běžná slitina, vyrobená převážně z plechu, je titan 6AL-4V, kde je 6% hliníku a 4% vanadu.
Několik slitin vanadu vykazuje supravodivé vlastnosti. První supravodič A15 v první fázi byl sloučenina V 3 Si vanadu, která byla získána v roce 1952. Vanadium-galliová páska se používá v supravodivých magnety. Struktura supravodivé fáze A15 V3 Ga je podobná struktuře běžnějších supravodičů: stannide triniobium (Nb 3 Sn) a niobium-titan (Nb 3 Ti).
Nedávno vědci zjistili, že ve středověku bylo do některých vzorků damaškové a damaškové oceli přidáno malé množství vanadu (od 40 do 270 dílů na milion). To zlepšilo vlastnosti čepelí. Nicméně není jasné, kde a jak se těžil vzácný kov. Možná byl součástí některých rud.
Aplikace
Kromě metalurgie se pro jiné úkoly používá vanád. Průřez zachycování tepelných neutronů a krátký poločas rozpadu izotopů vzniklých zachycením neutronů činí tento kov vhodným materiálem pro použití uvnitř reaktoru s jádrem.
Nejvíce obyčejný oxid vanadičitý, oxid pentoxid V 2 O 5, se používá jako katalyzátor při výrobě kyselina sírová a jako oxidační činidlo při výrobě maleinanhydridu. Oxid vanadu se používá při výrobě keramických výrobků.
Kov je důležitou složkou směsných katalyzátorů oxidů kovů používaných při oxidaci propanu a propylenu na akrolein, kyselinu akrylovou nebo ammoxidaci propylenu na akrylonitril. Další oxid kysličník vanadičný VO 2 - se používá při výrobě skleněných povlaků, které blokují infračervené záření při určité teplotě.
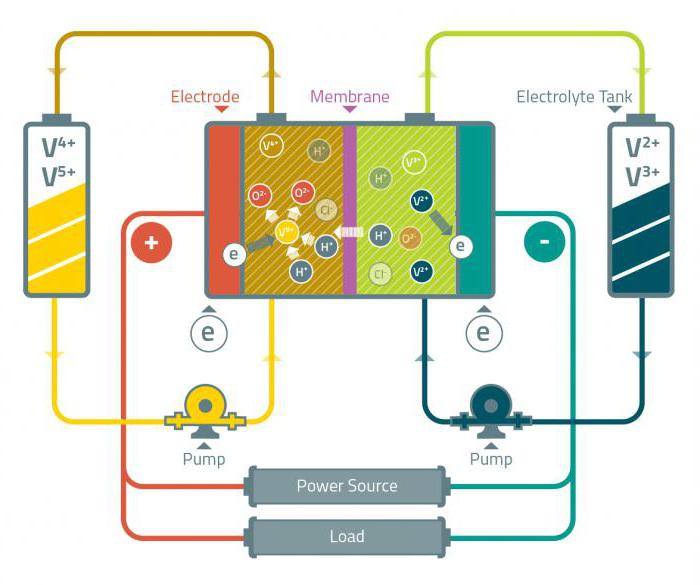
Vanadový redox akumulátor je galvanická buňka sestávající z vodných vanadových iontů v různých oxidačních stavech. Baterie tohoto typu byly poprvé navrženy ve třicátých letech minulého století a komerční použití začalo v osmdesátých letech. Vanadát lze použít k ochraně oceli proti korozi.
Vanad je důležitý pro lidské zdraví. Pomáhá regulovat metabolismus uhlíku a lipidů, podílí se na výrobě energie. Za den se doporučuje konzumovat 6 až 63 mcg (data WHO) látky pocházející z potravy. Je to dost obtížné u obilovin, luštěnin, zeleniny, bylin, ovoce.