Glycerin: strukturní vzorec, vlastnosti a aplikace
Jedná se o nejjednodušší triatomický alkohol. Chemický vzorec glycerolu je C3H5 (OH) 3 . Je to čirá viskózní kapalina. Bez zápachu, sladká chuť. Není to jedovatý, proto je široce používán v každodenním životě, potravinářském průmyslu, kosmetice a lékařství. Strukturní vzorec glycerolu je uveden na obrázku. Ale jak je to těženo?
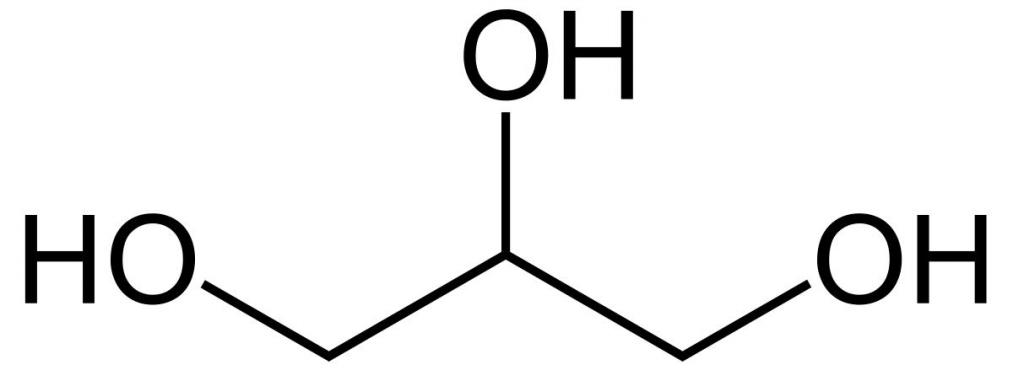
Způsoby, jak získat glycerin
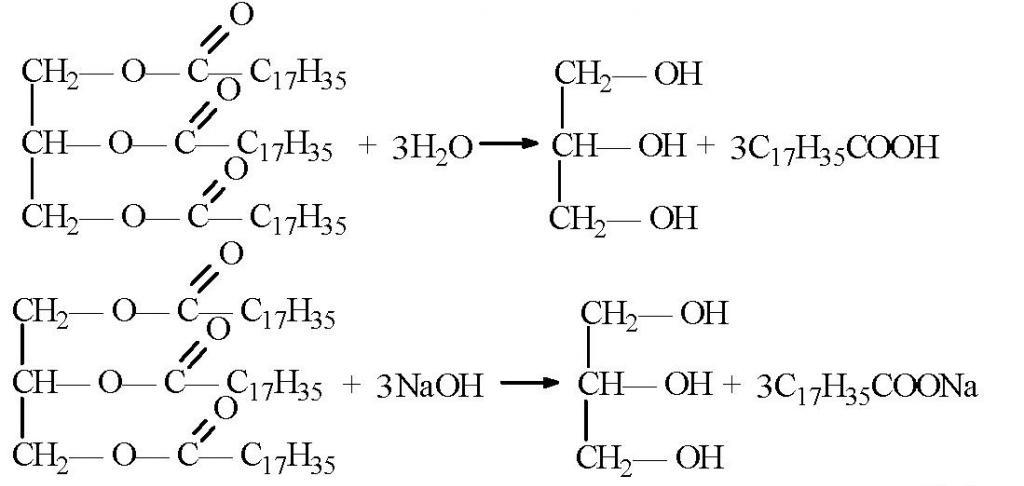
Téměř veškerý průmyslový glycerol pochází z tuku. Z chemického hlediska jsou to estery glycerolu. Během zmýdelnění těchto tuků (mýdla) se tvoří glycerin jako vedlejší produkt. Pak je velmi snadné vystupovat z reakční směsi.
Syntetizovat glycerin je možné jinými způsoby. Například z acetonu. V tomto případě se redukuje vodíkem za získání isopropylalkoholu. V dalším stupni se molekula vody štěpí dehydratací za vzniku propylenu, který se pak chloruje. Výsledný dichlorpropan se znovu chloruje, čímž se získá trichlorpropan. Posledním stupněm výroby glycerolu je zahřívání hydratací. V této fázi jsou všechny tři molekuly chloru nahrazeny hydroxylovými skupinami. Stejně jako nyní v průmyslu získáte syntetickou látku. Pouze jako surovina se používá propylen, který se uvolňuje z bočních plynů během destilace oleje.
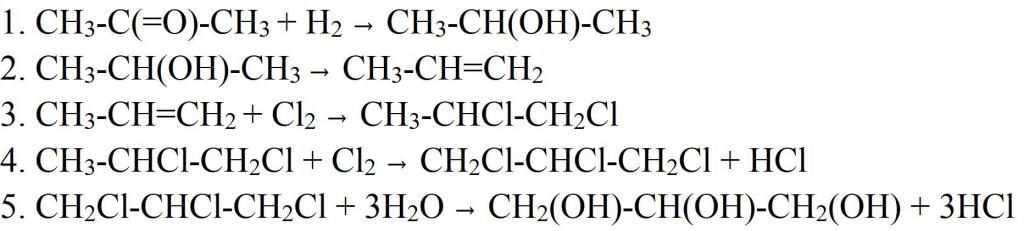
Ale z propylenu získat glycerin může být jiný způsob. K tomuto účelu se propylen oxiduje na akrolein. Oxidace se provádí vzduchem kyslíkem za přítomnosti katalyzátoru (mědi) a zvýšené teploty. Dále se k ní přidá peroxid vodíku, čímž se získá aldehydalkohol dvojsodný. Jako katalyzátor pro tuto reakci se používá oxid osmičitý (VIII). Aldehydová skupina ve výsledné sloučenině se hydrogenuje a stává se třetí hydroxylovou skupinou. Tak se ukázalo glycerin.
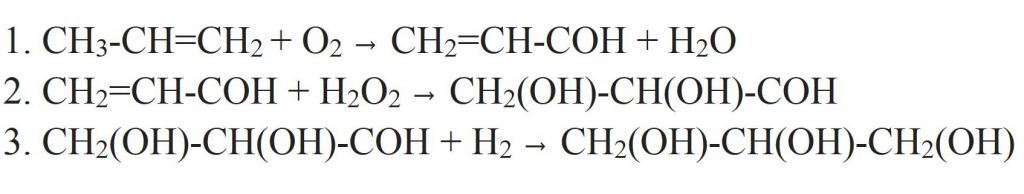
Další verze syntézy najednou navrhla EE Wagnera. Oxidací allylalkoholu s manganistanem draselným v alkalickém prostředí lze získat glycerol v jednom stupni.
Fyzikální vlastnosti
Glycerin je bezbarvá kapalina bez zápachu se sladkou chutí. Je hygroskopický, tj. Má tendenci absorbovat vodu. Při teplotě 20 ° C se roztaví a při teplotě 290 ° C dochází k částečnému rozkladu. Směs s vodou a alkoholy v jakémkoliv poměru. Důvodem je chemický vzorec. Hydroxylové skupiny dovolují, aby glycerol vytvářel mnoho vodíkových vazeb s molekulami vody. To vede k rozpuštění.
Ad
Rozpusťme glycerin také v acetonu a některých dalších organických látkách. Nerozpustný v benzenu a éterech. On sám může být takový pro mnoho organických a anorganických sloučenin. Hustota v kapalném stavu je 1,26 g / cm3. Je také třeba poznamenat, že glycerin je velmi viskózní kapalina. Nemovitost je 1474 krát víc než voda.
Chemické vlastnosti
Pochází z strukturální vzorec glycerin obsahuje tři hydroxylové skupiny. Proto jsou pro ni charakteristické chemické reakce monohydrických alkoholů. Kromě toho jsou kyselé vlastnosti glycerolu mnohem silnější než jiné monohydricky. Takže může interagovat s kovy, oxidy nebo zásadami. Rovnice chemických reakcí glycerolu jsou uvedeny níže.
Ad
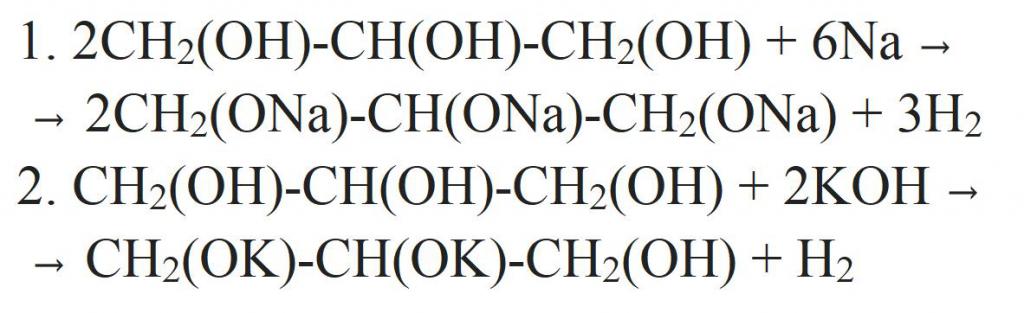
Může také proniknout do dehydratačních reakcí, které tvoří mnoho různých produktů. Takže získáte akrolein.
Samostatně by mělo být řečeno o nahrazení hydroxylové skupiny pro atom halogenu. To může nastat, když glycerin interaguje s halogenovodíkem. Jak je zřejmé ze strukturního vzorce glycerolu, mohou být v důsledku reakce vytvořeny mono-, di- a tri-deriváty. Úplnější substituce může být dosaženo, pokud je interakce provedena s halogenidy fosforu.
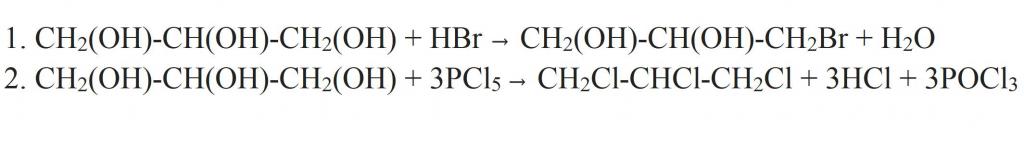
Ale glycerin má specifické vlastnosti, které jsou jedinečné vícemocným alkoholům. Například interaguje s hydroxidem měďnatým za vzniku komplexní sloučeniny modré barvy - glycerátu mědi. Tato reakce je kvalitativní pro všechny vícesytné alkoholy.
Znaky pro něj a esterifikační reakce. To je reakce interakce s kyselinami, která vede k esteru. Kromě toho je glycerin esterifikován s organickými i minerálními kyselinami. Například dusičnan. Tato reakce se také nazývá nitrace. Výsledkem je velmi užitečný, ale extrémně výbušný produkt - nitroglycerin. Opět ze strukturního vzorce glycerolu lze vidět, že ne všechny hydroxylové skupiny mohou být erifikovány. Vše závisí na reakčních podmínkách.
Ad
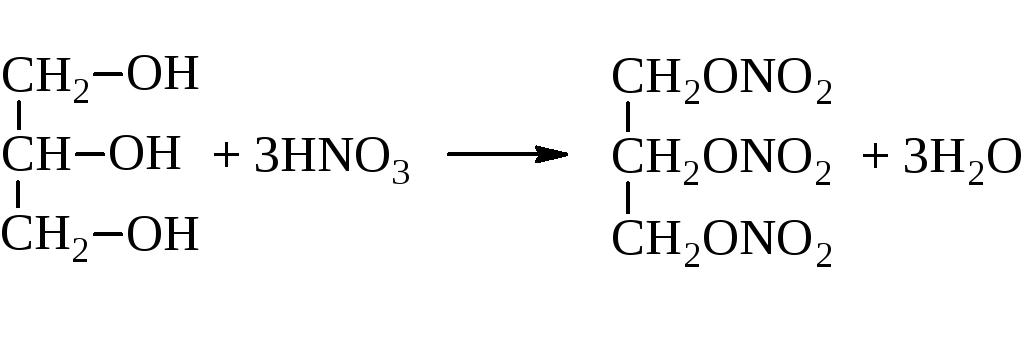
Při interakci s vodíkem při vysokém tlaku a za přítomnosti katalyzátorů je jedna z hydroxylových skupin snížena. V důsledku reakce se získá dvojsýtný alkohol - propylenglykol.
Glycerin může také vstoupit do polykondenzačních reakcí, čímž vznikne směs polyglycerolů. Za tímto účelem se ohřívá velmi dlouho na téměř 300 ° C ve slabém alkalickém prostředí. Chemický vzorec glycerinu je přezkoumán.
Oxidace
Glycerin má mnoho možností oxidace. Konečný produkt závisí na povaze oxidačního činidla, katalyzátorů a dalších reakčních podmínkách. Tak může být glycerin oxidován silnými oxidačními činidly, například dichromanem draselným v kyselém prostředí. V důsledku této reakce se veškerý glycerin rozloží na oxid uhličitý a vodu.
Ad
Oxidace může nastat jemněji. Například reakcí s peroxidem vodíku se získá aldehyd nebo keton. Jako katalyzátor se používají soli železa (II).
Oxidace může být provedena, aby se získala kyselina glycerová. V tomto případě se interakce provádí koncentrovaným způsobem kyselina dusičná. Jedna z hydroxylových skupin je jednoduše oxidována na karboxylovou skupinu. Další exotické kyseliny se také získávají z glycerinu. Při interakci s roztokem manganistanu draselného vzniká kyselina tartronová a kyselina mezoxalová. A když se oxiduje vzdušným kyslíkem za zahřívání v přítomnosti hydroxidu barnatého, získá se směs kyseliny šťavelové a kyseliny mravenčí. Glycerin kyseliny jodové lze oxidovat na mravenčí a formaldehyd.
Průmyslové aplikace
Vzhledem k jeho složení a vlastnostem je glycerin používán v průmyslu.
- V textilním průmyslu se používá pro výrobu měkkých a elastických látek, stejně jako pro syntézu barviv a syntetických vláken.
- Používá se při výrobě některých druhů papíru.
- V kožedělném průmyslu se jeho roztoky používají pro opalování a výkrm kůže.
- V zemědělství se semena ošetřují glycerinem, aby se zajistila stabilnější klíčivost.
- V oblasti nátěrových hmot se glycerin používá pro syntézu leštících směsí a laků.
- Při výrobě obalových materiálů, jako je celofán, se používá jako plastifikátor.
- Na balení se používají polymery na bázi glycerolu. Papír impregnovaný glycerinem získává ohnivzdorné vlastnosti.
Použití v potravinářském průmyslu
Glycerin je výživový doplněk E422. Používá se jako stabilizátor pro zachování a zvýšení viskozity výrobků. Používá se při výrobě pekařských a cukrářských výrobků (zejména čokolády) jako zahušťovadla a činidla udržujícího vlhkost. Pomáhá přidávat objem do hotových výrobků. Díky tomuto doplňku může chléb zůstat čerstvější.
Ad
Výtažky na bázi glycerinu jsou často přidávány do nápojů. Umožňují vám, abyste chuti méně ostrý. Používá se také při výrobě alkoholu. Přidejte tabák a upravte vlhkost, odstraňte dráždivou chuť.
Lékařské aplikace
Glycerin je součástí některých léků, které se používají při léčbě kožních onemocnění. Má antiseptické vlastnosti, zabraňuje infekci ran. Pomáhá také snížit intrakraniální a nitrooční tlak, a proto se používá při léčbě otoků mozku.
Vzhledem k tomu, že glycerin je dobré rozpouštědlo, je aktivně používán ve farmakologickém průmyslu. S touto látkou lze dosáhnout velmi vysoké koncentrace účinné látky. Může také poskytnout požadovanou konzistenci léků. Často se přidává k masti a krémům, protože brání odpařování vlhkosti a sušení.
Aplikace v kosmetologii
Glycerin je součástí mnoha kosmetických přípravků: mýdla, šampony, krémy, zvlhčující masky. Při styku s pokožkou v malých množstvích zachovává vlhkost v horních vrstvách pokožky. Někteří však tvrdí, že časté používání přípravků s glycerinovou bází zbavuje kůži přirozené vlhkosti a jen zhoršuje sucho. Také glycerin se často používá jako přísada do mýdla. Takže jeho schopnost praní se zvyšuje.
Účinky na lidské tělo
Glycerin je dobře vstřebáván tělem, protože je snadno přeměněn na tuk trávicí systém. Z tohoto důvodu se nepovažuje za toxický. Denní spotřeba této látky není omezena. Ale nezapomeňte, že glycerin je hygroskopický, takže vede k velkému uvolnění volů v těle, to znamená, že existuje riziko dehydratace. Z tohoto důvodu je jeho použití v potravinářských výrobcích přísně regulováno. Při styku s pokožkou má také sušicí účinek. Stále existují diskuse o potřebě používání látek v kosmetice.
Takže článek zkoumal složení a vlastnosti glycerinu a jeho použití.