Izotopy jsou ... Radioaktivní izotopy, jejich rozklad a poločas
Pravděpodobně ne na zemi takový člověk, který by neslyšel o izotopích. Ale ne každý ví, co to je. Výraz "radioaktivní izotopy" zní obzvlášť děsivě. Tyto nepochopitelné chemické prvky děsí lidstvo, ale ve skutečnosti nejsou tak hrozné, jak se na první pohled může zdát.
Definice
Porozumět pojetí radioaktivní prvky je třeba nejprve říci, že izotopy jsou vzorky stejného chemického prvku, ale s různou hmotností. Co to znamená? Otázky zmizí, pokud si nejprve pamatujeme strukturu atomu. Skládá se z elektronů, protonů a neutronů. Počet prvních dvou elementárních částic v jádru atomu je vždy konstantní, zatímco neutrony, které mají svou vlastní hmotu, se mohou vyskytovat ve stejné látce v různých množstvích. Tato okolnost vytváří řadu chemických prvků s různými fyzikálními vlastnostmi. 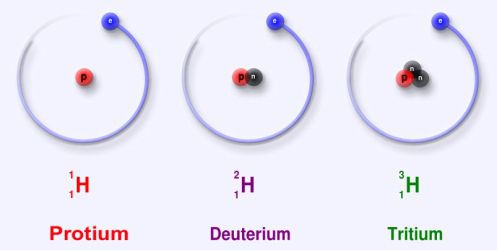
Nyní můžeme dát vědeckou definici studovaného konceptu. Izotopy jsou tedy kumulativní sadou chemických prvků s podobnými vlastnostmi, ale s různými hmotnými a fyzikálními vlastnostmi. Podle modernější terminologie se nazývají pleádou nukleotidů chemického prvku.
Ad
Trochu historie
Na začátku minulého století vědci zjistili, že stejná chemická sloučenina v různých podmínkách může vykazovat různé hmotnosti elektronových jader. Z čistě teoretického hlediska by takové prvky mohly být považovány za nové a začaly se s nimi plnit prázdné buňky v periodické tabulce D. Mendelejeva. Ale v něm je jen devět volných buněk a vědci objevili desítky nových prvků. Navíc matematické výpočty ukázaly, že zjištěné sloučeniny nemohly být považovány za dosud neznámé, protože jejich chemické vlastnosti plně odpovídaly vlastnostem stávajících.
Po dlouhých diskusích bylo rozhodnuto nazvat tyto prvky izotopy a dát je do stejné buňky jako ty, jejichž jádra obsahují stejný počet elektronů s nimi. Vědci se podařilo zjistit, že izotopy jsou jen některé variace chemických prvků. Nicméně jejich příčiny a dlouhověkost byly studovány téměř sto let. Dokonce ani na počátku 21. století není možné tvrdit, že lidstvo ví absolutně všechno o izotopích.
Ad
Trvalé a nestabilní varianty
Každý chemický prvek má několik izotopů. Vzhledem k tomu, že ve svých jádrech jsou volné neutrony, nevstupují do stabilních vazeb s ostatními složkami atomu. Po nějaké době opouští volné částice jádro, čímž se mění jeho hmotnost a fyzikální vlastnosti. Tímto způsobem se vytvářejí další izotopy, které nakonec vedou k tvorbě látky se stejným počtem protonů, neutronů a elektronů.
Ty látky, které se velmi rychle rozpadají, se nazývají radioaktivní izotopy. Uvolňují do vesmíru velké množství neutronů a vytvářejí silné ionizující záření gama, které je známé svou silnou pronikavou silou a které negativně ovlivňuje živé organismy.
Ad
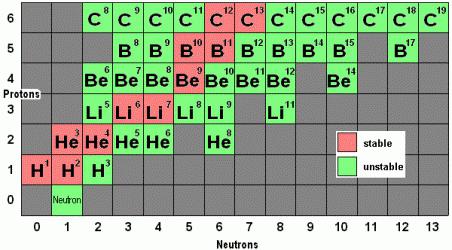
Více stabilních izotopů není radioaktivní, jelikož množství volných neutronů vysílaných jimi není schopno generovat záření a významně ovlivnit jiné atomy.
Po dlouhou dobu vědci vytvořili jeden důležitý vzor: každý chemický prvek má své vlastní izotopy, perzistentní nebo radioaktivní. Je zajímavé, že mnoho z nich bylo získáno v laboratoři a jejich přítomnost v přirozeném stavu je malá a ne vždy fixovaná nástroji.
Rozložte se v přírodě
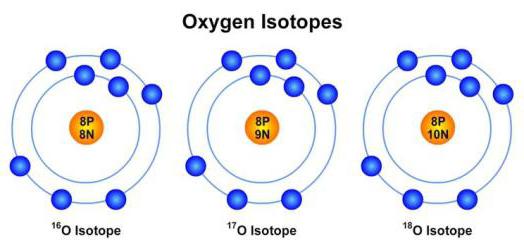
V přírodních podmínkách se nejčastěji vyskytují látky, jejichž hmotnost izotopu je přímo určena podle pořadového čísla v tabulce D. Mendeleeva. Například vodík označený symbolem H má sekvenční číslo 1 a jeho hmotnost se rovná jedné. Jeho izotopy, 2H a 3H, jsou extrémně vzácné.
Dokonce i lidské tělo má určité množství radioaktivních izotopů. Dostávají se do potravy ve formě izotopů uhlíku, které jsou zase absorbovány rostlinami z půdy nebo vzduchu a stávají se součástí organické látky v procesu fotosyntézy. Proto člověk, zvířata a rostliny vyzařují určité pozadí záření. Pouze je tak nízký, že nezasahuje do normálního fungování a růstu.
Zdroje, které přispívají k tvorbě izotopů, jsou vnitřní vrstvy zemského jádra a záření z vesmíru.
Jak víte, teplota na planetě závisí převážně na horkém jádru. Jen nedávno však bylo jasné, že zdrojem tohoto tepla je složitá termonukleární reakce, v níž jsou zapojeny radioaktivní izotopy.
Ad
Izotopní rozklad
Jelikož izotopy jsou nestabilní formace, lze předpokládat, že nakonec se rozpadají na stálé jádra chemických prvků. Toto tvrzení je pravdivé, protože vědci nebyli schopni rozpoznat v povaze obrovského množství radioaktivních izotopů. Ano, a většina z těch, které byly v laboratořích těžena, existovala pár minut až několik dní a pak se znovu změnila na obyčejné chemické prvky.
Ale v přírodě existují izotopy, které jsou velmi odolné vůči rozkladu. Mohou existovat miliardy let. Takové prvky se utvářely v těch vzdálených časech, kdy se země stále formovala, a dokonce ani pevná kůra nebyla na povrchu.
Radioaktivní izotopy se velmi rychle rozpadají a re-formují. Proto, aby se usnadnilo hodnocení odporu izotopu, se vědci rozhodli zvážit kategorii svého poločasu.
Poločas
Ne všichni čtenáři mohou okamžitě pochopit, co se myslí tímto konceptem. Dejme to. Poločas rozpadu izotopu je doba, po kterou podmíněná polovina odebraných látek přestane existovat.

To neznamená, že zbytek spojení bude zničen ve stejném čase. Ve vztahu k této polovině je třeba zvážit další kategorii - dobu, po kterou zmizí druhá část, tedy čtvrtina počátečního množství látky. A tato úvaha pokračuje na dobu neurčitou. Lze předpokládat, že doba úplného rozpadu počátečního množství látky je prostě nemožné počítat, protože tento proces je téměř nekonečný.
Ad
Vědci, s vědomím poločasu života, však mohou určit, kolik látek na začátku existovalo. Tato data se úspěšně používají v příbuzných vědách.
V moderním vědeckém světě se koncept úplného rozpadu prakticky nepoužívá. Pokud jde o každý izotop, je obvyklé uvést jeho poločas, který se pohybuje od několika sekund do mnoha miliard let. Čím je poločas nižší, tím více radiace je od látky a tím vyšší je radioaktivita.
Minerální opevnění
V některých odvětvích vědy a techniky je použití relativně velkého množství radioaktivních látek považováno za povinné. Současně však v přírodních podmínkách existuje jen velmi málo těchto sloučenin.
Je známo, že izotopy nejsou běžnými variantami chemických prvků. Jejich počet je měřen několika procenty nejvíce odolné odrůdy. To je důvod, proč vědci potřebují uměle obohatit fosilní materiály.
Během let výzkumu bylo zjištěno, že rozpad izotopu je doprovázen řetězovou reakcí. Uvolněné neutrony jedné látky začínají ovlivňovat jiné. Výsledkem je, že těžké jádro se rozpadlo na lehčí a získaly se nové chemické prvky.

Tento jev se nazývá řetězová reakce, v důsledku čehož je možné získat více perzistentních, ale méně běžných izotopů, které se později používají v národním hospodářství.
Aplikace rozpadové energie
Také vědci zjistili, že během rozpadu radioaktivního izotopu je uvolněno velké množství volné energie. Jeho množství je obvykle měřeno jednotkou Curie, která odpovídá době štěpení 1 g radonu 222 za 1 sekundu. Čím vyšší je tento indikátor, tím více energie se uvolní.
To byl důvod pro rozvoj způsobů využití volné energie. Takže tam byly atomové reaktory, ve kterých je umístěn radioaktivní izotop. Většina uvolněné energie se shromažďuje a přeměňuje na elektřinu. Na základě těchto reaktorů se budují jaderné elektrárny, které poskytují nejlevnější elektřinu. Zmenšené verze takových reaktorů na samohybných mechanismech. Vzhledem k riziku nehody jsou nejčastěji tyto stroje ponorky. V případě selhání reaktoru bude počet obětí na ponorce snazší minimalizovat.

Další velmi děsivá možnost využití poločasu energie je atomová bomba. Během druhé světové války byli testováni na lidstvo v Čechách Japonské města Hirošimu a Nagasaki. Důsledky byly velmi smutné. Proto se svět dohodl na nepoužití těchto nebezpečných zbraní. Na místě s velkými státy se zaměřením na militarizaci a dnes pokračovat v průzkumu v tomto odvětví. Mnoho z nich tajně vyrábí atomové bomby ze světové komunity, které jsou tisíckrát nebezpečnější než ty, které byly používány v Japonsku.
Izotopy v medicíně
Pro mírové účely se naučil užívání radioaktivních izotopů v medicíně. Směr radiace do postižené oblasti těla můžete zastavit průběh onemocnění nebo pomoci pacientovi, aby se plně zotavil.
Ale častěji se používají radioaktivní izotopy pro diagnostiku. Faktem je, že jejich pohyb a povaha hvězdokupy jsou nejsnadněji zaznamenávány zářením, které produkují. Tímto způsobem se do lidského těla vstříkne určité množství radioaktivní látky, které není nebezpečné, a lékaři používají nástroje k tomu, aby sledovali, jak a kam jde.
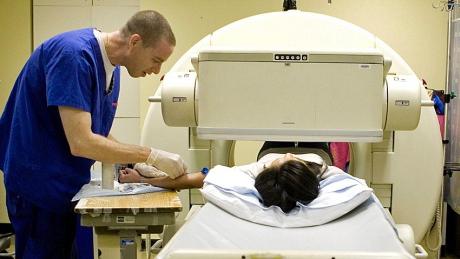
Práce je tedy diagnostikována mozku, povaha rakovinových nádorů, zejména fungování žláz vnitřní a vnější sekrece.
Aplikace v archeologii
Je známo, že v živých organizmech je vždy radioaktivní uhlík-14, poločas rozpadu izotopu je 5570 let. Navíc vědci vědí, kolik z tohoto prvku je obsaženo v těle až do jeho smrti. To znamená, že všechny řezané stromy vyzařují stejné množství záření. Časem intenzita záření klesá.
To pomáhá archeologům určit, jak dlouho zemře strom, z něhož stavěli kuchyň nebo jakoukoli jinou loď, a tím i samotný stavební čas. Tato výzkumná metoda se nazývá analýza radioaktivního uhlíku. Díky němu je vědcům snadnější vytvořit chronologii historických událostí.